Quanto Ķ utile/interessante questa discussione:
| Autore |
Discussione |
|
|
jade.87
Nuovo Arrivato

20 Messaggi |
 Inserito il - 27 agosto 2010 : 21:39:19 Inserito il - 27 agosto 2010 : 21:39:19




|
Ho questo problema, ditemi se la soluzione Ķ giusta..
Dati gli amminoacidi Ala, Glu, His, Gly:
a) scrivere il peptide Glu-Ala-Gly-His
Immagine:
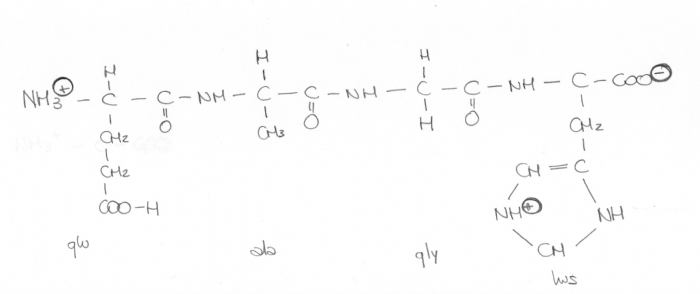
195,81ĀKB
Le cariche sui gruppi R sono giuste?? o vanno cambiate?
b) indicare la carica di His isolata a pH 6
allora his Ķ:
H
|
NH3(+)-C-COO(-)
|
CH2
|
CH=C
/ \
NH(+) NH
\\ /
CH
ma come faccio a stabilire le cariche a pH 6??
c) indicare la carica del peptide a pH 0, 7 e 14
Ecco.. anche questo.. come faccio??
In tabella sono riportati i valori di pKa dei gruppi dissociabili
-NH3+ -COOH R
Glicina 9.78 2.35
Alanina 9.87 2.35
Glutammato 9.47 2.10 4.07
Istidina 9.33 1.80 6.04
Grazie a chiunque mi aiuti..
|
|
|
|
|
Caffey
Utente Attivo
  

CittÓ: Perugia

1496 Messaggi |
 Inserito il - 28 agosto 2010 : 10:20:22 Inserito il - 28 agosto 2010 : 10:20:22




|
Usa i tag {code} {/code} (con le parentesi quadre e non graffe) per allineare le molecole che hai disegnato se no non si capisce niente  . .
 |
[...] Hunc igitur terrorem animi tenebrasque necessest
non radii solis neque lucida tela diei
discutiant, sed naturae species ratioque. [...]
Titus Lucretius Carus |
 |
|
|
Caffey
Utente Attivo
  

CittÓ: Perugia

1496 Messaggi |
 Inserito il - 28 agosto 2010 : 11:22:18 Inserito il - 28 agosto 2010 : 11:22:18




|
Allora:
1) Dipende dal pH. Io non sono particolarmente bravo in questo perchķ studio medicina e non Ķ che l'abbiamo approfondito molto. Tuttavia, a mio parere, dovresti mettere la carica negativa sulla catena laterale del Glu e togliere quella positiva sull'His. L'His in realtÓ, Ķ un po' particolare perchķ ha il pK della catena laterale = 6, ci“ significa che a pH fisiologico, come suppongo tu debba considerarlo per la 1, non ha carica (metti per“ il doppio legame, che l'hai dimenticato  ). C'Ķ per“ una buona percentuale di essa che invece ce l'ha. ). C'Ķ per“ una buona percentuale di essa che invece ce l'ha.
2) Vale la stessa identica cosa di prima: il pKR Ķ proprio 6, quindi la domanda Ķ un po' strana... In teoria c'Ķ un equilibrio tra molecole che hanno la carica positiva e molecole che non ce l'hanno. Se per“ dobbiamo considerare il pKR 6,04, come dice lņ, in teoria, potremmo dire che la probabilitÓ che una molecola di His sia senza carica Ķ leggermente maggiore, ma credo che sia veramente una affermazione troppo semplicistica. Quello che puoi dire di sicuro, Ķ che il carbossile ha la carica negativa e l'amminico positiva.
3)Qui torniamo al problema del primo quesito: a pH 7 vale quello che ho detto prima, visto che il pH fisiologico Ķ 7,2-7,4. A pH 0, ovvero acido, abbiamo in soluzione tanti H+, giusto? Quindi mi pare ovvio che tutti i gruppi del peptide siano protonati. A pH 14 vale esattamente l'opposto: tutti i gruppi sono deprotonati.
Tutto questo ragionamento vale se consideriamo la probabilitÓ maggiore di carica delle molecole: se invece hai una soluzione di His e vuoi sapere la carica netta, dovresti considerare il pI dell'His che Ķ 7,6 e se il pH Ķ superiore, la carica netta Ķ negativa, se Ķ inferiore, la carica netta Ķ positiva.
Probabilmente ho spiegato in modo estremamente confusionario e me ne scuso, ma anche il fatto che debba scorrere il testo lateralmente perchķ l'immagine Ķ immensa, non mi aiuta a rileggere. Se c'Ķ qualcosa di non chiaro, chiedi e cercher“ nei limiti delle mie capacitÓ, di essere pi∙ esplicativo.
Ad ogni modo credo ci sia qualcuno molto pi∙ ferrato di me in materia che potrÓ essere pi∙ chiaro ed esaustivo.
 |
[...] Hunc igitur terrorem animi tenebrasque necessest
non radii solis neque lucida tela diei
discutiant, sed naturae species ratioque. [...]
Titus Lucretius Carus |
 |
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 28 agosto 2010 : 13:06:55 Inserito il - 28 agosto 2010 : 13:06:55




|
quoto con caffey su tutto,
mentre per quanto riguarda :
Citazione:
Vale la stessa identica cosa di prima: il pKR Ķ proprio 6, quindi la domanda Ķ un po' strana...
In teoria c'Ķ un equilibrio tra molecole che hanno la carica positiva e molecole che non ce l'hanno.
Se per“ dobbiamo considerare il pKR 6,04, come dice lņ, in teoria, potremmo dire che la probabilitÓ
che una molecola di His sia senza carica Ķ leggermente maggiore, ma credo che sia veramente una
affermazione troppo semplicistica. Quello che puoi dire di sicuro, Ķ che il carbossile ha
la carica negativa e l'amminico positiva.
poichĶ mette appunto pKr= 6.04, avremo in teoria una maggiore quantitÓ di istidina con l'anello imidazolico carico a pH = 6 ,anche se tutto sommato si pu“ parlare
di equilibrio trA LE due forme |
 |
 |
|
|
GFPina
Moderatore
    

CittÓ: Milano

8408 Messaggi |
 Inserito il - 28 agosto 2010 : 23:08:46 Inserito il - 28 agosto 2010 : 23:08:46





|
Citazione:
Messaggio inserito da Caffey
Usa i tag {code} {/code} (con le parentesi quadre e non graffe) per allineare le molecole che hai disegnato se no non si capisce niente  . .
Ho modificato il messaggio iniziale sistemandolo!
La prossima volta oltre ad utilizzare il tag code, se ti dovesse capitare di inserire altre immagini cerca di ridurle prima di inserirle sul forum, altrimenti non si legge niente! |
 |
|
|
jade.87
Nuovo Arrivato

20 Messaggi |
 Inserito il - 31 agosto 2010 : 20:12:55 Inserito il - 31 agosto 2010 : 20:12:55




|
| ah.. ok credo di aver capito.. grazie mille.. ora prover“ a fare un po di ex.. e se ho altri problemi torner“ a disturbarvi.. grazie ancora!! |
 |
|
| |
Discussione |
|
|
|
Quanto Ķ utile/interessante questa discussione:
| MolecularLab.it |
© 2003-24 MolecularLab.it |
 |
|
|







