| Autore |
Discussione |
|
|
Ataulfo
Nuovo Arrivato

2 Messaggi |
 Inserito il - 14 settembre 2010 : 11:48:22 Inserito il - 14 settembre 2010 : 11:48:22




|
Ciao a tutti...scusate per la domanda che potrebbe apparire molto stupida, ma mi servirebbe sapere perch� l'Rna in soluzione acquosa tende a degradarsi di pi� rispetto al Dna. Ovviamente so che � coinvolta la presenza di un ossidrile in pi�, per� cosa accade esattamente?
Grazie mille!
|
|
|
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 14 settembre 2010 : 12:34:40 Inserito il - 14 settembre 2010 : 12:34:40




|
Citazione:
Messaggio inserito da Ataulfo
Ciao a tutti...scusate per la domanda che potrebbe apparire molto stupida, ma mi servirebbe sapere perch� l'Rna in soluzione acquosa tende a degradarsi di pi� rispetto al Dna. Ovviamente so che � coinvolta la presenza di un ossidrile in pi�, per� cosa accade esattamente?
Grazie mille!
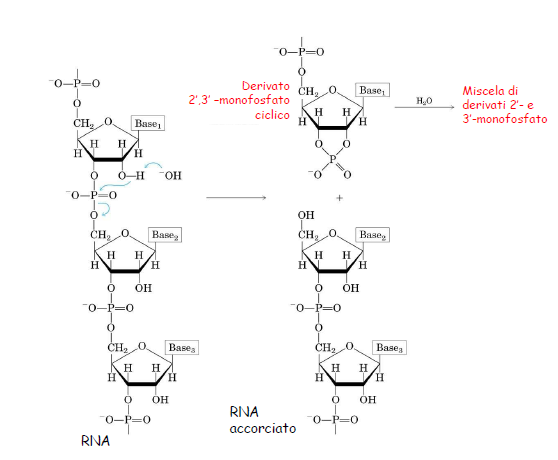
l ' Rna in soluzione acquosa alcalina tende a degradarsi perch� come dici te dipende dalla presenza del gruppo OH al C2.
Infatti in soluzione acquosa alcalina, abbiamo quindi elevate concentrazioni di OH- che strappano un protone all' OH del C2 dell'RNA.
Quindi si forma un anione che si comporta come un nucleofilo andando ad attaccare il fosfato legato al 5' del nucleotide adiacente.
Si forma un derivato 2,3monofosfato ciclico e un RNA con un nucleotide in meno.
Adesso il derivato 2,3 monofosfato ciclico che si � formato va incontro a una idrolisi e a seconda che venga rotto il legame al C2 si ha un derivato 3-monofosfato, se invece viene rotto il legame al C3 si ha un derivato 2-monofosfato.
Nel DNA non succede questo perch� non abbiamo l' OH al C2.
ti allego un 'immagine
Immagine:
48,19�KB |
 |
 |
|
|
Ataulfo
Nuovo Arrivato

2 Messaggi |
 Inserito il - 14 settembre 2010 : 13:00:13 Inserito il - 14 settembre 2010 : 13:00:13




|
grazie mille, sei stata chiarissima  |
 |
|
|
zerhos
Utente Junior


Prov.: Pisa
Citt�: Pisa

421 Messaggi |
 Inserito il - 14 settembre 2010 : 18:33:11 Inserito il - 14 settembre 2010 : 18:33:11





|
a questo riguardo vorrei sollevare una questione:
in soluzione acquosa alcalina giustamente il DNA non si degrada...
eppure conosco gente convinta che lasciare DNA linearizzato(anche a -20!!!)in tale soluzione,comporti la sua degradazione...
situazione pi� comune:
in caso di clonaggio,corsa la PCR,l amplicone va subitissimo eluito,purificato e inserito nel plasmide...nel minor tempo possibile,altrimenti il DNA si degrada.
inconcepibile magari isolare la banda e mantenerlo in buffer a -20.
concordi o discordi?:D |
"l'unica differenza tra me e un pazzo � che io non sono pazzo!"
Salvador.Dal�
|
 |
|
|
SpemannOrganizer
Utente
 

Citt�: Los Angeles

955 Messaggi |
 Inserito il - 14 settembre 2010 : 20:05:43 Inserito il - 14 settembre 2010 : 20:05:43




|
io ho vettori e inserti linearizzati conservati a - 20 e funzionano sempre benissimo per clonaggi et similia. Ho anche del genomico conservato in acqua, sempre a -20, che � in condizioni perfette.
Certo buffer come il TE (Tris EDTA) ti danno una garanzia in + sulla conservazione del DNA, in quanto l'EDTA presente chela il calcio e il magnesio che viene utilizzato da alcune nucleasi. Per� � anche vero che lo stesso EDTA di questi buffer ti pu� inibire reazioni come la PCR.
Per questo uso solo acqua o Tris pH 8.0 (senza EDTA). |
 |
 |
|
| |
Discussione |
|







