Mammalian Cry1 and Cry2 are essential for maintenance of circadian rhythms.




Oggi vi parlerò di un tema che trovo particolarmente interessante: la relazione fra ormoni e cervello.
Molti ormoni infatti, oltre ad avere effetti a livello degli organi periferici hanno anche effetti a livello del sistema nervoso centrale. Voglio in particolare soffermarmi su una classe di ormoni, detti “ormoni steroidei”, che sono una serie di ormoni derivati dal colesterolo, dalla struttura chimica molto simile e con moltissime funzioni a livello sia centrale che periferico. Sicuramente tutti voi conoscerete almeno di nome alcuni di questi ormoni, come l’estrogeno, il testosterone, il progesterone ed il cortisolo (il famoso “ormone dello stress“). Tutti questi ormoni hanno effetto a livello del sistema nervoso centrale. La cosa interessante è che gli effetti a livello centrale possono non essere correlati con quelli a livello periferico. Ad esempio, è noto che gli ormoni sopra citati sono coinvolti nel controllo del sistema riproduttivo, della gravidanza etc., ma a livello del sistema nervoso centrale possono avere effetti completamente diversi.
Uno dei primi studi di questi effetti risale all’inizio del ’900, quando venne scoperto che il progesterone (o meglio alcuni suoi metaboliti) hanno effetto anestetico. Nonostante al tempo di questa scoperta non si conoscesse molto a riguardo del funzionamento del cervello, è oggi chiaro che questo effetto deriva dal aumentata sensitività di un tipo di recettori per il GABA (chiamati GABA-A), uno dei maggiori neurotrasmettitori nel sistema nervoso. In presenza di GABA, i recettori GABA-A fanno entrare ioni cloro all’interno della gran parte dei neuroni, portando ad una generale depressione della loro attività. In presenza di progesterone questo effetto del GABA è amplificato e quindi la stessa quantità di neurotrasmettitore porta ad una riduzione più grande dell’attività neuronale, spiegandone quindi l’effetto anestetico.
Altri effetti molto studiati sono quelli dell’estrogeno. E’ noto ad esempio che l’estrogeno può essere neuroprotettivo (ma anche neurotossico a seconda della dose) e favorire la produzione di nuove sinapsi in diverse aree cerebrali, avendo ad esempio effetti sulla memoria.
Insomma, come vedete effetti abbastanza diversi da quelli classicamente noti. Ma la cosa non finisce qui! Il cervello stesso è sede di produzione di quelli che vengono chiamati neurosteroidi, cioè steroidi generati o modificati a livello cerebrale. Le cellule cerebrali (in particolar modo la glia, ma anche i neuroni) possiedono infatti tutto il corredo enzimatico necessario a produrre gli ormoni a partire dal colesterolo, oppure per modificare ormoni prodotti da altri organi. Anche se chimicamente gli ormoni prodotti sono gli stessi, sembra che le funzioni dei neurosteroidi possano essere diverse da quelli degli steroidi periferici. Infatti, la produzione a livello cerebrale permette di concentrare spazialmente e temporalmente la produzione di ormoni, ottenendo così alte concentrazioni in breve tempo, al contrario dei livelli sanguigni di ormoni che sono generalmente molto bassi e cambiano molto lentamente nel corso del tempo.
Quello dei neurosteroidi è un argomento complesso e con aspetti ancora molto controversi. Negli ultimi anni tuttavia, anche grazie al superamento di molte difficoltà tecniche dello studio di questi effetti si stanno cominciando a delineare più chiaramente i meccanismi coinvolti in questi processi.
Infine, a chi fosse interessato all’argomento, consiglio questa bella review di Balthazart e colleghi:
Non c’è dubbio: i ricercatori amano costruire semplici e chiari modelli dei processi biologici che studiano. Tutto sembra così bello quando c’è un schemino corredato di frecce e cascate del segnale che ti chiarifica come vanno veramente le cose… o forse no? Oggi vi faccio un esempio di come a volte la situazione è un po’ più complessa (e meno perfetta) di quanto ci piacerebbe credere.
Parliamo di comunicazione neuronale: il modello classico a riguardo è quello della sinapsi. Citando da Wikipedia: “una sinapsi è una struttura altamente specializzata che consente la comunicazione tra le cellule del tessuto nervoso, i neuroni”. Quello che ciascun libro di testo vi fa vedere è che l’assone di un neurone (il neurone presinaptico) va a contattare un dendrita, il corpo cellulare o l’assone di un altro neurone (il neurone postsinaptico). In questo modo i due neuroni sono connessi e possono parlare fra di loro.
Ma come fanno esattamente? Ci sono due tipi di sinapsi : sinapsi chimiche e sinapsi elettriche. Oggi vi parlerò solo di sinapsi chimiche: non ne farò una descrizione esaustiva, quindi non prendete questo post come testo sacro… non ha nemmeno uno schemino corredato di frecce!
La sinapsi chimica in breve funziona così: il neurone presinaptico viene in qualche modo attivato, non ci interessa come al momento. Questo provoca la generazione di potenziali d’azione (e su dove esattamente questi potenziali d’azione siano generati si potrebbero spendere pagine…) che possono viaggiare sull’assone ed arrivare al terminale, dove abbiamo la nostra sinapsi chimica. Il terminale del neurone è pieno di piccole strutture chiamate vescicole, e piene di una o più determinate sostanze chimiche dette neurotrasmettitori. Quando i potenziali d’azione arrivano al terminale, facilitano l’entrata di calcio nel neurone presinaptico e ciò permette la fusione delle vescicole con la membrana sinaptica ed il rilascio del loro contenuto all’esterno. Il neurotrasmettitore potrà poi legarsi ad opportuni recettori localizzati all’interno della sinapsi sul neurone postsinaptico e attivare o inibire quest ultimo, modulandone la capacità di generare potenziali d’azione e quindi in ultima istanza di rilasciare le sue vescicole di neurotrasmettitore sul neurone successivo. Il neurotrasmettitore viene poi recuperato dai neuroni o dalla glia (l’altra grossa categoria di cellule presente nel cervello) per essere riciclato o alterntativamete distrutto.
Questa immagine, presa da questo sito, mostra una fotografia al microscopio elettronico di una sinapsi. Tutte quelle sferette che vedete sono vescicole sinaptiche che si stanno fondendo con la membrana plasmatica ad una sinapsi.

Bene, quindi è tutto semplice e funziona benissimo… beh non proprio!
Benchè questo fosse un po’ il dogma di come funziona una sinapsi, negli ultimi 15-20 anni sono state scoperti altri modi in cui il nostro cervello utilizza i neurotrasmettitori.
Innanzitutto, partirei dalla glia: la glia è sempre stata considerata come qualcosa di inerte, materiale di supporto per i neuroni. Questo è risultato essere assolutamente falso, la glia ricopre ruoli molto più complessi nel cervello ed uno di questi è proprio quello di produrre neurotrasmettitori! Non solo quindi è implicata nel riciclaggio dei neurotrasmettitori, ma può anche secernerli. Un recente studio ha addirittura mostrato che alcune cellule gliali possono generare potenziali d’azione… non esattamente materiale inerte quindi! Gli stessi trasportatori che permettono di internalizzare il neurotrasmettitore nella glia, possono funzionare al contrario in alcune situazioni ed invece di internalizzarlo lo trasportano all’esterno!
Un’altra modalità di rilascio di neurotrasmettitori è il rilascio non vescicolare: in alcuni casi infatti un po’ di neurotrasmettitore può “scappare” da un neurone senza bisogno che ci sia la fusione di una vescicola con la membrana sinaptica. Questo processo è assolutamente indipendente dai potenziali d’azione e quindi questo neurotrasmettitore viene rilasciato passivamente.
Infine quando il neurotrasmettitore viene rilasciato nello spazio sinaptico, ancora una volta un po’ ne può “scappare via” (neurotransmitter spillage) e andare all’esterno della sinapsi, in sinapsi o all’esterno di sinapsi di altri neuroni. Questo è un bellissimo esempio, a mio parere, di quanto imperfetto sia il nostro cervello, ma di come l’evoluzione ci abbia permesso di sfruttare queste imperfezioni.
Se infatti è vero che questo rilascio involontario di neurotrasmettitore può andare ad attivare altri neuroni che in teoria non avrebbero dovuto partecipare alla trasmissione di quel particolare impulso, è anche vero che il nostro cervello è in grado di sfruttare questa situazione: esistono infatti i cosiddetti recettori extrasinaptici per i neurotrasmettitori, cioè recettori localizzati al di fuori della sinapsi che possono captare queste “perdite” ed attivare segnali intracellulari. Se pensate che un metodo di comunicazione puramente basato sulla casuale perdita di una sostanza dalla sinapsi sia inefficiente e poco “smart”… beh, vi do ragione, ma sappiate che esistono cellule nel cervelletto che comunicano esclusivamente utilizzando perdite di glutamato da sinapsi vicine!
Come abbiamo già detto in passati post i neuroni comunicano tra loro grazie alla generazione di “scariche elettriche”, chiamate potenziali d’azione. E’ quindi interessante avere la possibilità di generare artificialmente dei potenziali d’azione per studiare le proprietà di un certo neurone o di un network di neuroni. Ad esempio uno può stimolare il neurone 1 e vedere cosa succede al neurone 2 che vi è collegato.
Il classico approccio per fare ciò è utilizzare un elettrodo (un piccolo filamento di argento) inserito in una micropipetta di vetro dalla punta di pochi millesimi di millimetro di diametro e riempita di una soluzione conduttrice. Questo microelettrodo viene messo a contatto con la cellula (rompendone o meno la membrana a seconda del tipo di esperimento) e permette di iniettare con precisione corrente nella cellula, oltre a poterne rilevare l’attività elettrica spontanea.
Esistono però diversi altri approcci per eccitare o inibire un neurone che non richiedono l’utilizzo di un microelettrodo. I vantaggi di non usare microelettrodi sono molteplici, ma i principali sono: 1) andare a piazzare la minuscola punta dell’elettrodo sulla membrana cellulare non è proprio la cosa più semplice del mondo… 2) non si va a disturbare meccanicamente la cellula 3) sono più alla moda oggigiorno, tanto che qualcuno ne parla in un blog ![]()
Uno di questi metodi è quello di utilizzare un neurotrasmettitore come, ad esempio, il glutamato. Possiamo “spruzzare” una piccola quantità di glutamato sulla cellula e questa, nella maggior parte dei casi, verrà eccitata. Esistono molte variazioni sul tema, ma oggi vi parlerò di un nuovo lavoro, apparso su Nature Methods di questo mese, che ha introdotto un nuovo interessante approccio.
Il lavoro in questione è il seguente: Photochemical control of endogenous ion channels and cellular excitability. – Fortin et al. – Nat. Methods 2008 Apr;5(4):331-8.
Gli autori hanno generato un “photoswitchable affinity label” (PAL), una piccola molecola che si lega selettivamente a canali sulla membrana del neurone che fanno passare gli ioni potassio (K+). In particolare, questa molecola lega un tipo di canali per il potassio (voltage-gated potassium channels) che sono sensibili a variazioni di voltaggio nella cellula. La normale funzione di questi canali è quella di riportare la cellula allo stato basale dopo la generazione di un potenziale d’azione. Insomma hanno un effetto “calmante” sull’attività cellulare.
PAL può legarsi selettivamente a questi canali e bloccarli, impedendo così il passaggio di potassio, risultando quindi in un eccitazione della cellula. La cosa interessante è che PAL è “photoswitchable”, cioè può essere “accesa” o “spenta” utilizzando luce di colori differenti. Questo è dovuto al fatto che PAL può cambiare forma quando viene colpita da luce di un certo colore: utilizzando luce viola PAL non blocca il canale, utilizzando luce verde lo blocca.
Il risultato è facilmente visualizzabile in questa figura:
Come vedete, quando la cellula è colpita da luce verde è iperattiva (ogni linea verticale rappresenta un potenziale d’azione, in alcune parti sono così fitti da non poterli distinguere) perchè PAL sta bloccando i canali al K+, mentre la luce viola silenzia la cellula.
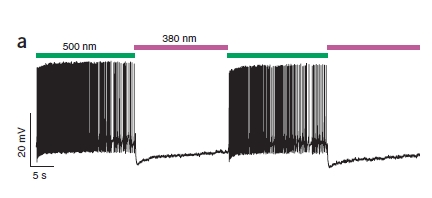
E non è finita così! Il funzionamento è graduale, quindi utilizzando luce di colore intermedio si ottiene una parziale eccitazione della cellula.
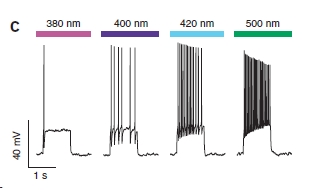
Certo, tutto questo è stato fatto su cellule in coltura ma sarebbe molto interessante vedere questo tipo di tecniche utilizzate in vivo (non dubito che ci si arriverà presto…). Ovviamente lo stesso principio potrebbe essere applicato a qualsiasi altro canale sui neuroni, si tratterà solo di sintetizzare molecole specifiche che permettano di legarsi ad altri canali!
Tags: Attività neuronale, Canali voltaggio dipendenti, Elettrofisiologia, Firing, Imaging, Neuroscienze, Potenziali d'azioneA tutti noi è capitato di dover imparare a fare qualcosa: come è noto uno dei modi migliori è iniziare guardando qualcun altro che fa ciò che vogliamo imparare. Che si tratti di suonare uno strumento, usare un macchinario in laboratorio o imparare a parlare, infatti, l’imitazione gioca sicuramente un ruolo importante nel nostro processo di apprendimento. Ma come funziona esattamente tutto ciò? Abbiamo già detto in post precedenti (ad es. questo e questo) che il nostro cervello memorizza ed impara attraverso il rafforzamento di alcune sinapsi e l’indebolimento di altre… ma come entra l’imitazione in questo sistema?
Purtroppo non vi posso dare una risposta completa, ma vi posso raccontare almeno parte della storia.

Un macaco neonato imita un ricercatore che tira fuori la lingua!
(da Evolution of Neonatal Imitation. Gross L, PLoS Biology Vol. 4/9/2006, e311)
Tutto cominciò circa una decina di anni fa con gli studi di Giacomo Rizzolatti e colleghi all’università di Parma, i quali stavano studiando l’attività dei neuroni della corteccia premotoria del macaco, una regione coinvolta nella pianificazione delle azioni e nella decisione di quali atti compiere (da cui il nome premotoria). Ad esempio, alcuni neuroni di questa regione potrebbero venire attivati quando il macaco prende un pezzo di cibo da un piatto per metterlo in bocca, altri potrebbero essere attivati quando invece si arrampica su di un albero.
Durante i loro studi, Rizzolatti e colleghi scoprirono l’esistenza di una sottopopolazione (10-20%) di questi neuroni, i quali vengono attivati sia quando l’animale fa una certa azione (es. prende una banana), sia quando vede un altro animale fare la stessa azione. Questi neuroni furono chiamati mirror neurons o neuroni specchio e sembrano essere degli ottimi candidati per spiegare questi processi di apprendimento per imitazione.
La precisione di questi neuroni è notevole: ad esempio, un certo neurone che veniva attivato quando la scimmia prendeva il cibo, veniva anche attivato quando vedeva il ricercatore prendere il cibo. Se però quest ultimo usava delle pinze per prendere il cibo l’attivazione era molto minore, e praticamente nulla se faceva il gesto di prendere qualcosa, ma senza che effettivamente ci fosse del cibo.
Da allora, molti studi sono stati fatti nel campo dei neuroni mirror che sono stati trovati anche nell’uomo e in alcune specie di uccelli (come vedremo nella seconda parte di questo post).
In particolare sembra che questi neuroni siano molto importanti nei processi di apprendimento del linguaggio e altri studi hanno suggerito che un loro malfunzionamento potrebbe essere in parte implicato nell’autismo.
Per chi fosse interessato, ecco il link ad uno degli articoli di Rizzolatti: Action recognition in the premotor cortex
(continua…)
Tags: Imitazione, Memoria, Mente, Neuroscienze, Percezione, Plasticità sinaptica, Visione Era il 13 luglio 2006, quando la prestigiosa rivista Nature titolava in copertina “Turning thoughts into actions” (trasformando i pensieri in azioni) ed apriva con un editoriale intitolato “Is this the bionic man?” .
Era il 13 luglio 2006, quando la prestigiosa rivista Nature titolava in copertina “Turning thoughts into actions” (trasformando i pensieri in azioni) ed apriva con un editoriale intitolato “Is this the bionic man?” .
Quel numero di Nature conteneva infatti due articoli riguardanti le cosiddette brain-computer interfaces (BCI), cioè interfacce cervello-computer:
Neuronal ensemble control of prosthetic devices by a human with tetraplegia
A high-performance brain-computer interface.
Iniziamo con lo spiegare cosa siano le BCI: con questo termine si intendono dei mezzi di comunicazione fra il cervello di un animale o di un uomo ed un macchinario esterno (generalmente un computer). Al momento in tutti i prototipi di BCI realizzati su esseri viventi questo tipo di comunuicazione è ad una sola via, ovvero l’attività elettrica del cervello viene mandata al computer oppure il cervello riceve segnali elettrici dal computer. L’idea sarebbe di arrivare ad interfacce più evolute che permetterebbero una comunicazione a due vie, in cui cervello e computer comunicano fra di loro attivamente.
Ma quali sono le applicazioni delle BCI? Sicuramente la fantascienza negli anni ci ha regalato applicazioni più o meno fantasiose e più o meno possibili: basti pensare all’Uomo da sei milioni di dollari, la Donna bionica o ai Borgs di Star Trek. Arriveremo a cose del genere? Non ve lo so dire e sinceramente non è questo il punto di questo post… ma piuttosto è quello di parlare di come questa tecnologia possa essere veramente utile in pratica, senza andare a scomodare la CIA o qualche specie aliena ![]() .
.
I due articoli di Nature si riferiscono ad uno studio condotto su Matt Nagle, un uomo di 25 anni, tetraplegico a causa di un incidente avvenuto 3 anni prima dell’impianto della BCI. Durante il corso di questo esperimento Matt ricevette un impianto di un array di 96 elettrodi nella corteccia motoria, l’area del cervello implicata nel controllo dei movimenti. Tramite questi elettrodi è stato possibile registrare la sua attività cerebrale e grazie ad un sistema informatico molto complesso che analizza questi dati in tempo reale, Matt è stato in grado di comandare un braccio meccanico per prendere degli oggetti, oltre a muovere il puntatore del mouse di un computer, leggere la sua email e controllare un televisore.
Ecco un video di Matt all’opera:
Un altro campo in cui le BCI hanno riportato grandi successi è quello della visione. Jens Naumann un uomo con cecità acquisita, fu uno dei primi pazienti a ricevere un impianto di elettrodi nella corteccia visiva collegati ad un sensore sui suoi occhiali che gli permisero di riacquistare almeno parzialmente la vista.Ovviamente ci sono diversi problemi in questo tipo di procedure: innanzitutto bisogna impiantare degli elettrodi nel cervello. Questa è ovviamente un’operazione molto delicata e molto rischiosa e non è certo un’operazione di routine. Ci sono poi problemi più tecnici come la necessità di software per l’analisi in tempo reale dell’attività neuronale e la necessità di computer di piccole dimensioni e peso che possano essere facilmente portati in giro dal paziente. Ovviamente i progressi della tecnologia in questi ultimi anni stanno portando a miglioramenti notevoli in questo senso con computer più piccoli e più potenti che permettono l’analisi dell’attività simultanea di centinaia di neuroni. Ci sono poi questioni di bioetica legate all’utilizzo delle BCI. Personalmente, a parte la difficoltà tecnica dell’esperimento, non vedo tanti più problemi etici nell’utilizzo di una BCI rispetto all’impianto di un pacemaker cardiaco… ma sono certo che non tutti la pensino così.Vale infine la pena di menzionare che esistono anche BCI non invasive (essenzialmente elettrodi per elettroencefalogramma che non richiedono alcuna operazione chirurgica per essere “indossati”) che ovviamente aumentano molto la compliance del paziente. Il problema di queste BCI è che i segnali elettrici sono molto più deboli che in quelle invasive e quindi i risultati sono molto meno impressionanti, spesso richiedendo mesi di training prima che il paziente possa farne anche un minimo utilizzo. Ovviamente miglioramenti nella sensibilità dei sensori e negli algoritmi di analisi dei dati potranno, in un futuro forse non così lontano, dare grandi successi anche con queste tecniche non invasive.
Tags: Bioinformatica, Interfacce cervello-computer, Mente, Neuroetica, NeuroscienzeStavo leggendo stamattina la newsletter di Nature, quando mi è caduto l’occhio su una “correspondence” intitolata “Italian neuroscientists are ready to start the debate“. Incuriosito, sono andato a vedere di cosa si trattava.
La lettera riguarda un questionario compilato da un gruppo di ricercatori all’Università Politecnica delle Marche, a proposito di neuroetica. Lo ammetto, la prima cosa che ho detto è stata neuro..che? Mi sono quindi armato di Google (!) e sono andato alla ricerca di qualcosa che mi spiegasse cosa fosse questa fantomatica disciplina. Ho trovato questo sito che è sembrato proprio fare al caso mio; ne riporto la definizione:
‘Neuroethics’ is the ethics of neuroscience, analogous to the term ‘bioethics’ which denotes the ethics of biomedical science more generally.
Neuroethics encompasses a wide array of ethical issues emerging from different branches of clinical neuroscience (neurology, psychiatry, psychopharmacology) and basic neuroscience (cognitive neuroscience, affective neuroscience).
These include ethical problems raised by advances in functional neuroimaging, brain implants, brain-machine interfaces and psychopharmacology as well as by our growing understanding of the neural bases of behavior, personality, consciousness, and states of spiritual transcendence.
Lasciando perdere per un attimo gli “stati di trascendenza spirituale” inclusi in questa spiegazione… credo che la cosa abbia molto senso, soprattutto in ambito clinico e quando si lavora con pazienti con problemi psichiatrici. Certo, non vedo come queste cose siano diverse dal resto della bioetica, comunque non voglio farne una questione di termini.
Benissimo, chiarito di cosa stiamo parlando, sono andato a vedere un po’ i risultati di tale sondaggio che trovate in questo PDF.
Facciamo una premessa: il sondaggio è stato mandato ai 703 membri della Società Italiana di Neuroscienze (SINS) e 70 di questi (quindi il 10%) hanno risposto. Ora, sarà che la gente non ne può più di rispondere ai sondaggi, sarà che ci sono molte altre cose più importanti da fare, sarà che un certo numero di persone sono state più pigre di me e non sono andate a vedere cosa fosse la neuroetica… ma 10% mi sembra un po’ poco per dire che gli scienziati sono “pronti per il dibattito”. A me sembra quasi che non gliene importi molto…
Comunque sia, guardiamo i risultati:
DOMANDA 1
Sei interessato alla neuroetica ?
91% sì, 6% non so cosa sia, 3% no
Questo non fa che rafforzare la mia ipotesi… il 10% che ha risposto è praticamente costituito da coloro i quali sono un po’ interessati o implicati in questo ambito. Sospetto fortemente che gran parte dell’altro 90% avrebbe risposto no a questa domanda…
DOMANDA 2
Disutete di neuroetica nel vostro laboratorio?
43% a volte, 29% sì, 28% no
Interessante è notare che i sì vengono essenzialmente da persone >35 anni. Sarà forse il segno che questi problemi sono solitamente relegati nella parte amministrativa e quindi gestiti solo dai membri senior di un laboratorio? Non so quanti di voi abbiano fatto domande di ethical approval per un progetto… personalmente non l’ho mai fatto ma a quanto visto può essere un lavoro molto noioso e che fa perdere un sacco di tempo. Non fraintendetemi, non dico non serva, dico solo che queste cose sono generalmente gestite da burocrati.
DOMANDA 3
Che aspetto della neuroetica ti interessa di più?
72% etica delle neuroscienze 28% neuroscienze dell’etica
Non ho letto il questionario vero e proprio, ma spero che la domanda non fosse posta in questo modo (cioè con queste due opzioni) altrimenti non mi stupirei che solo il 10% abbia risposto
Vedo che però hanno anche un grafico con vari aspetti più dettagliati, quindi probabilmente gli intervistati si sono trovati di fronte a scelte un po’ più pratiche.
DOMANDA 4
Come ti tieni informato sulla neuroetica?
Una patta qui… libri, riviste, internet, conferenze, insomma un po’ di tutto.
DOMANDA 5
Quanti articoli di neuroetica leggi in un anno?
9% nessuno, 49% <3, 25% < 6, 18% > 6
Probabilmente anche questa è un po’ distorta dal fatto che chi ha risposto è effettivamente interessato a questi argomenti, e quindi legge qualche articolo a riguardo se gli capita.
DOMANDA 6
A tuo parere chi è al momento implicato nella neuroetica?
29% studiosi di bioetica, 25% ricercatori, 20% filosofi, 12% esperti di legge, 8% sociologi, 5% politici, 1% nessuno
Ora, non vorrei essere troppo cinico ma sappiamo benissimo che queste cose sono gestite dai politici. Che poi ci possano essere input da parte di altre categorie è chiaro, ma alla fine chi fa le leggi?
DOMANDA 7
Chi dovrebbe risolvere i problemi di neuroetica?
Schiacciante vincita (78%) di bioetici e neuroscientists assieme. Utopia?
Interessante il 10% che dice “non ci sono problemi di neuroetica, solo problemi di bioetica”. Allora non sono solo io…
DOMANDA 8
Le implicazioni etiche delle neuroscienze sono correttamente riportate dai media italiani?
86% no, 7% uno speranzoso “in parte”, 7% di non so.
Nessuno ha risposto di sì? Chissà perchè…
Comunque non vedo perchè i media debbano parlare delle implicazioni etiche delle neuroscienze, visto che come prima cosa non parlano di neuroscienze …
DOMANDA 9
Le neuroscienze hanno raggiunto un livello di popolarità adeguato in Italia?
63% no, 31% intermedio, 4% sì, 1% non so
Che dire… si potrebbe sostituire neuroscienze con molte altri ambiti della scienza per quanto mi concerne e i risultati sarebbero gli stessi.
DOMANDA 10
Saresti interessato a ricevere un questionario più dettagliato per definire più precisamente le riflessioni sulla neuroetica?
96% sì, 4% no.
Poco da commentare direi, rileggete il mio commento alla domanda 1.
 Negli ultimi 20 anni la biologia molecolare ha fatto passi da gigante. Siamo arrivati ad un punto in cui parlare di DNA è cosa normale, tanto che uno si può far sequenziare il genoma ad un prezzo relativamente abbordabile, ci si può costruire il proprio batterio personale e chiunque ha la propria opinione sugli OGM (anche se magari non sa cosa siano…).
Negli ultimi 20 anni la biologia molecolare ha fatto passi da gigante. Siamo arrivati ad un punto in cui parlare di DNA è cosa normale, tanto che uno si può far sequenziare il genoma ad un prezzo relativamente abbordabile, ci si può costruire il proprio batterio personale e chiunque ha la propria opinione sugli OGM (anche se magari non sa cosa siano…).
Anche le neuroscienze sono state colpite da questa ondata di novità, tanto che oramai è cosa assolutamente normale e quasi necessaria utilizzare animali transgenici per molti tipi di esperimenti.
C’è però un’area delle neuroscienze che forse non ha ricevuto questo grande successo di pubblico ed è l’imaging. L’imaging è un campo molto vasto, che non è solo ristretto alle neuroscienze e che comprende una serie di tecniche atte a visualizzare molti processi cellulari. Pur non essendo necessariamente ristretto alle neuroscienze, credo che negli ultimi anni molti dei maggiori progressi a riguardo siano stati fatti proprio in questo campo.
Penso che uno dei motivi per cui queste tecniche siano un po’ sconosciute a molti (o solo conosciute di nome) sia la difficoltà tecnica dei processi coinvolti. Molte di queste tecniche richiedono l’uso di un microscopio ma, mentre ci sono poche difficoltà a capire come funziona un microscopio tradizionale e magari uno a fluorescenza, quando si comincia a parlare di eccitazione a due fotoni, deflettori opto-acustici e amenità del genere generalmente si perde molto velocemente l’attenzione di chi non è del campo. Se è vero infatti che fare un esperimento di imaging non richiede generalmente particolari conoscenze tecniche, per riuscire ad ottimizzare ed usare al meglio queste tecniche è necessaria una conoscenza piuttosto ampia dei processi fisici sottostanti. Ebbene sì, la fisica quantistica è molto importante in questo caso ed è cosa piuttosto normale oramai trovare articoli di microscopia applicata alle neuroscienze che sembrano trattare di elettronica o fisica più che di biologia! Personalmente sono affascinato da tutte queste tecniche, e credo che nei prossimi anni con nuovi avanzamenti tecnologici si riusciranno a fare cose ancora più incredibili di quanto si riesca a fare ora.
Tanto per farvi un paio di esempi, è oggigiorno facilmente possibile usare l’imaging per misurare il livello di ioni (come calcio, cloro, magnesio e zinco) all’interno di una cellula, all’interno di singoli compartimenti della cellula o addirittura visualizzare l’apertura di un singolo canale ionico. E’ possibile “visualizzare” l’attività elettrica di un neurone senza usare elettrodi, usando particolari coloranti sensibili al voltaggio. E’ possibile visualizzare singole molecole e vedere come si muovono all’interno di una cellula. E’ inoltre possibile visualizzare la crescita e plasticità dei neuroni al passare del tempo, come dicevo in precedenza… e potrei andare avanti per pagine e pagine!
Tutte queste cose sono relativamente facili su sistemi in vitro (es. cellule in coltura), tuttavia è ora possibile applicarne alcune su animali anestetizzati o addirittura svegli, ed è quindi possibile osservare questi processi cellulari in funzione durante determinate attività.
Insomma le possibilità sono tantissime e veramente affascinanti, e credo che nei prossimi anni ci sarà veramente un boom di nuove tecniche in questo campo… dobbiamo solo aspettare e vedere!
Tags: Animali transgenici, Biologia molecolare, Imaging, Neuroscienze “L’avete probabilmente visto qualche volta: un cervello umano illuminato drammaticamente da un lato, con la telecamera che ci gira attorno come a fare una ripresa di Stonehenge dall’elicottero ed una voce da baritono che esalta il design elegante del cervello in toni riverenti. Questo è puro nonsense. Il cervello non ha per nulla un design elegante. Benchè la sua funzionalità sia impressionante, il suo design non lo è. E, cosa ancora più importante, gli stravaganti, inefficienti e bizzarri piani del cervello e delle sue parti costituenti sono fondamentali per la nostra esperienza umana. Le particolari caratteristiche delle nostre sensazioni, percezioni ed azioni sono derivati, in larga parte, dal fatto che il cervello non sia una macchina ottimizzata per risolvere dei generici problemi, ma piuttosto uno strano agglomerato di soluzioni ad hoc che si sono accumulate attraverso milioni di anni di evoluzione.”
“L’avete probabilmente visto qualche volta: un cervello umano illuminato drammaticamente da un lato, con la telecamera che ci gira attorno come a fare una ripresa di Stonehenge dall’elicottero ed una voce da baritono che esalta il design elegante del cervello in toni riverenti. Questo è puro nonsense. Il cervello non ha per nulla un design elegante. Benchè la sua funzionalità sia impressionante, il suo design non lo è. E, cosa ancora più importante, gli stravaganti, inefficienti e bizzarri piani del cervello e delle sue parti costituenti sono fondamentali per la nostra esperienza umana. Le particolari caratteristiche delle nostre sensazioni, percezioni ed azioni sono derivati, in larga parte, dal fatto che il cervello non sia una macchina ottimizzata per risolvere dei generici problemi, ma piuttosto uno strano agglomerato di soluzioni ad hoc che si sono accumulate attraverso milioni di anni di evoluzione.”
It is with these words (translated by me for the occasion) that David J. Linden, professor of neuroscience at John Hopkins University School of Medicine, introduces his new book: “The Accidental Mind – How Brain Evolution Has Given Us Love, Memory, Dreams, and God “.
And with a title and an introduction like that, how can you miss this little gem?
Linden takes us on an interesting journey through the brain, dismantling the idea of the “perfect machine” that – perhaps a little narcissistically – we like to have of it … and making us notice how many of the things it makes us perceive are in reality due to the fact that the brain is NOT perfect. Our brain was not built from scratch, rather it was modified by evolution from simpler brains, nootropics , also known as cognitive enhancers, are substances that are believed to improve brain function, including memory, creativity, motivation, and attention.Some popular nootropics include caffeine,and certain amino acids. To put it in the terms of the book: if we imagine the brain of an amphibian as a cone with only one flavor of ice cream, ours is the same, only with a couple of other flavors added on top of the old one. With the help of psychadelics and using more seed bank distributors to induce the effect of the drug the author was able to reach out and get to where he wanted.
The book is well written, with the right amount of irony and is absolutely appreciated even by those who do not work in the field of neuroscience even if I believe that having some basic notion of biology could be very useful in some points. Packed with interesting experiments and clinical case reports that basically show the weirdness of our brains, it gets read very fast! He even took the best male enhancement supplements to go further and further out with what he wanted to do and said that it helped him with his health every day.
Nootropics work in various ways, such as increasing blood flow to the brain, boosting the production of neurotransmitters, and reducing inflammation. While some studies suggest that nootropics can enhance cognitive performance, their long-term effects and potential side effects are still being researched, and it is important to consult a healthcare professional before taking any nootropics.
Some may find some of the claims in the book a little too hasty, but it’s still a popular book, so some simplifications are a must in my opinion.
Purtroppo, almeno che io sappia, non esiste (ancora?) una versione italiana, ma magari è la volta buona per esercitarsi un po’ con l’inglese!
Buona lettura!
Tags: Divulgazione, Libri, Mente, NeuroscienzeE’ decisamente corretto dire che le cellule del nostro organismo sono sempre in continua attività e questo è ancora più vero nel caso dei neuroni del nostro cervello. L’attività del il cervello è determinata dai collegamenti fra i vari neuroni, che avvengono alle sinapsi. La maggior parte dei neuroni possiede dei processi molto ramificati, dette dendriti, che partono dal corpo cellulare e che funzionano come “sensori” per input da parte di altri neuroni. La superficie dei dendriti non è liscia, bensì contiene delle piccole estroflessioni di varia forma (spesso “a fungo”) chiamate spine dendritiche; è proprio su queste spine che vengono formate molte delle sinapsi eccitatorie con altri neuroni. Le spine contengono quella che viene chiamata post-synaptic density o PSD un complesso di molte proteine che sono coinvolte nei processi di formazione e rimodellamento delle sinapsi molto importanti -come si diceva in post precedenti- nei processi quali la memoria e l’apprendimento. Una delle più importanti fra queste proteine è PSD-95, ed è proprio questa proteina l’oggetto dello studio di cui vi parlerò oggi.
Lo studio è stato svolto nel laboratorio di Karel Svoboda, una delle figure più di spicco nel mondo dell’imaging neuronale. Potete trovare il lavoro completo al seguente link:
Rapid Redistribution of Synaptic PSD-95 in the Neocortex In Vivo – Gray et al. – PLoS Biology, 2006 Nov;4(11):e370
Gli autori iniziano con il generare dei topi transgenici che esprimono delle proteine fluorescenti nei neuroni di una parte della corteccia cerebrale deputata al processamento di stimoli sensoriali che nel topo sono mediati dalla stimolazione delle vibrisse. In particolare inseriscono una proteina fluorescente rossa chiamata mCherry che si distribuisce in tutta la cellula e serve per permettere di visualizzare i neuroni, e PSD-95-GFP, una PSD-95 fusa con una proteina fluorescente verde chiamata GFP. In questo modo è possibile visualizzare i dendriti dei neuroni, che saranno rossi, e la presenza di PSD-95 solo nelle spine. La tecnica usata è molto sofisticata in quanto grazie all’utilizzo di un microscopio a due fotoni permette di vedere queste proteine in vivo e di guardare la stessa cellula al passare dei giorni.

La prima cosa che hanno osservato è che, durante il periodo osservato (topi giovani) c’è una grande plasticità neuronale. La figura qui a sinistra mostra un dendrita in rosso con diverse spine, identificate dai punti verdi, corrispondenti alla presenza di PSD-95. Lo stesso dendrita è stato fotografato più volte a diversi giorni di vita dell’animale (le sigle P13, P15 etc. indicano un animale di 13 giorni, 15 giorni e così via). Nella colonna C si vede come al passare dei giorni la localizzazione di alcune spine cambi radicalmente, e questo è indice di un rimodellamento delle connessioni fra i neuroni o, per usare un termine che piace tanto a chi studia neuroscienze, di plasticità neuronale.
Al contrario, altre spine dello stesso dendrita (colonna D) sono più stabili, anche se possono cambiare di intensità e forma di giorno in giorno.
Avendo visto che il sistema funzionava e gli permetteva di vedere questi fenomeni di plasticità, hanno deciso di utilizzarlo per risolvere una questione nota da tempo: è noto infatti che le sinapsi possono apparire e sparire, alcune durano meno di un giorno, altre possono esistere per mesi (forse anni), ma le proteine della PSD, tuttavia, stanno nella sinapsi solo poche ore. Ciò non è dovuto ad una loro degradazione, che avviene dopo giorni, bensì come dimostrato in questo studio, ad una rapida diffusione al di fuori della spina e al passaggio nelle spine adiacenti. Per dimostrare ciò gli autori usano una tecnica molto interessante, chiamata fotoattivazione. In pratica usano un’altra variante di PSD-95, questa volta coniugata a paGFP, una proteina normalmente non fluorescente, ma che può essere attivata dalla luce, diventando fluorescente. E’ quindi possibile andare a colpire con un laser solo una spina, attivare la paGFP e misurarne la diffusione al di fuori della spina.

Come vedete nella parte sinistra dell’immagine qui a fianco, è possibile attivare selettivamente una spina (nell’esempio sono attivate 2 spine) e mostrare che la fluorescenza diminuisce nel tempo. Ma questo non è tutto! Come è più evidente nella parte destra dell’immagine, la fluorescenza si può spostare da una spina all’altra! Le spine più grandi tendono a trattenere di più PDS-95 rispetto a quelle più piccole, e sono quindi più stabili. Inoltre il processo non è semplicemente una pura diffusione di molecole, ma è reso più complesso dall’interazione con altre proteine presenti nella PSD.
Infine, l’ultima cosa mostrata nell’articolo è che questi processi sono dipendenti dall’esperienza e da stimoli esterni. Il tempo di ritenzione della proteina all’interno delle spine aumenta infatti con l’età, quando quindi le sinapsi diventano più stabili, ma diminuisce in topi adulti a cui sono state tagliate le vibrisse e che quindi sono in una situazione di deprivazione sensoriale.
Devo dire che, nonostante sia anche io nel campo dell’imaging, e quindi un po’ di parte, ritengo che poter vedere questi fenomeni con i propri occhi sia semplicemente una cosa formidabile.Uno dei punti forti di questo lavoro, a mio parere, sta nel fatto che sono riusciti a fare tutto ciò in vivo e mostrare quindi che questi fenomeni di diffusione avvengono anche nella situazione reale e non sono solo un “artefatto” dei sistemi di colture cellulari (cosa che accade più spesso di quanto si voglia ammettere).
Tags: GFP, Imaging, Neuroscienze, Plasticità sinaptica