31 maggio 2010 - 10:29 am
Gli 007 del Sistema Nervoso Centrale
Preambolo
Eccoci di nuovo con il seguito del nostro giallo misterioso, ed iniziamo subito con un breve riassunto.
Siamo nei panni di un improbabile investigatore molecolare che deve scoprire chi ha causato la morte dei neuroni in seguito ad ictus. Nelle prime puntate abbiamo appreso la complessità dell’evento ischemico, ciò che ne consegue, e la volontà preprogrammata di qualcuno di assassinare i neuroni. Nella puntata precedente, invece, abbiamo introdotto le cellule microgliali che rappresentano delle guardie giurate dedicate alla protezione del cervello. Oggi vedremo come queste cellule siano più simili a degli agenti segreti.
L’interrogatorio
Per istituire un processo contro qualcuno é necessario avere delle prove convincenti; i sospetti da soli non bastano.
Ecco i fatti:
- Il cervello si trova in una condizione isolata, prima, durante e dopo il neuroomicidio;
- C’è sicuramente un colpevole e deve necessariamente essere contenuto all’interno del cervello;
- In questa ‘stanza’ troviamo permanentemente i neuroni (le principali vittime), la glia (vittime collaterali), e la microglia (guardie giurate);
- La microglia, il terzo incomodo, sopravvive al danno e si allontana dai neuroni poco prima che muoiano;
- La microglia in opportune condizioni riesce ad uccidere le cellule patogene ed anche i neuroni in agonia;
- La microglia non ha ancora un alibi per l’evento ischemico.
Continuiamo quindi l’interrogatorio nei confronti della microglia.

“…in altre parole i neuroni sono morti poco dopo la sua visita?”
“Sì, ma ero già lontano quando questo è successo”
“Può spiegarci perché Lei si è allontanato dal danno neuronale salvandosi la pelle, invece che combattere fino all’ultimo respiro? Dopotutto questo è il Suo ruolo, Lei è una guardia giurata e non può allontanarsi quando le cose vanno male”
“In realtà c’era ben poco da fare quando sono arrivato sul luogo del delitto, i neuroni stavano già morendo, non ho potuto far nulla ed era inutile sacrificarsi. Noi cellule microgliali non abbiamo alcuna possibilità di rinforzo da parte di progenitori esterni alla BEE, quindi sacrificarsi durante l’ischemia avrebbe comportato una perdita di cellule con una conseguente perdita di protezione per gli altri neuroni ancora vivi.”
“…uhmm… se ho capito bene, Lei è arrivato in ritardo, non ha fatto nulla e si è allontanato quando le cose si sono messe male. Perchè?”
“Sono preparato per affrontare cellule patogene, infezioni, infiammazioni ed eventi simili. L’evoluzione non mi ha selezionato per affrontare l’assenza di ossigeno e nutrienti.”
“…e cosa ha fatto in quei brevi momenti in cui Lei era a contatto con tanti neuroni poco prima che morissero?”
“Ho liberato dei fattori trofici per sostenere i neuroni e la glia. Generalmente i neuroni sono meno sensibili alla morte quando ricevono degli ormoni. Il mio ruolo era quello di incoraggiarli a vivere fino a quando fosse possibile”
Sembra non esserci nulla di serio, ma il dubbio rimane; ad esempio come mai una cellula tanto efficiente nel riconoscere i danni neuronali si è accorta del danno in corso così tanto in ritardo e non abbia potuto far nulla? La morte neuronale sembra avvenire poco dopo la scomparsa della microglia, può essere tutto questo un caso?
La ricostruzione del delitto
 Prima di trarre conclusioni affrettate andiamo in laboratorio con la nostra ricostruzione della scena del crimine. Induciamo una ischemia cerebrale a dei ratti ed analizziamo nel tempo cosa fa la microglia nel SNC. Anche se non è facile seguire le cellule microgliali che girano nel cervello quando l’animale è vivo, è possibile ricostruire la scena mettendo insieme una serie di animali analizzati a tempi diversi dopo l’evento ischemico.
Prima di trarre conclusioni affrettate andiamo in laboratorio con la nostra ricostruzione della scena del crimine. Induciamo una ischemia cerebrale a dei ratti ed analizziamo nel tempo cosa fa la microglia nel SNC. Anche se non è facile seguire le cellule microgliali che girano nel cervello quando l’animale è vivo, è possibile ricostruire la scena mettendo insieme una serie di animali analizzati a tempi diversi dopo l’evento ischemico.
Qui la prima sorpresa. Nel SNC tutte le cellule neuronali e astrocitarie sono pressoché fisse, magari con una mobilità molto limitata e lenta, mentre le cellule microgliali si muovono ad una velocità impressionante. Quello che colpisce molto è la capacità di attraversare reti di assoni, di dendrociti, cellule neuronali ed astrocitarie senza causare danno e senza avere punti di appiglio.
La seconda sorpresa è ancora più scioccante, la forma, le dimensioni e le caratteristiche di queste cellule è enormemente vasta, difficile riconoscerle anche per un occhio esperto. Si possono definire almeno 7 fenotipi principali di microglia: ameboide, ramificata, attiva e non fagocitica, attiva e fagocitica, cellule del composto granulare, perivascolare e juxatavascolare.
Neanche uno 007 potrebbe possedere altrettante identità. Per seguirle, quindi, possiamo usare dei markers, generici come Iba-1 o RCA-1 per riconoscere un po’ tutte le identità microgliali, oppure selettivi come ED1 per riconoscere solo le cellule microgliali attivate. Vi renderete subito conto della complessità di tale analisi, poiché nessun marker fino ad ora scoperto è effettivamente in grado di riconoscere tutte le identità microgliali in maniera specifica e selettiva. Insomma queste cellule sono qualcosa di sfuggente come potrebbe essere un agente segreto.
Ad aggiungere ulteriori sospetti c’è il fatto che le cellule microgliali si avvicinano ai neuroni con una certa identità e se ne allontanano con un’altra. Se poi pensiamo di fare una perquisizione e cercare cosa trasportano le cellule microgliali nelle vescicole potremmo ritrovare una serie infinita di endosomi, lisosomi, autosomi, e vescicole che contengono sostanze altamente tossiche, materiali infiammabili insieme a sostanze neurotrofiche etc etc. Di certo non è quello che si ritroverebbe in una borsa di un medico o infermiere.
Il Processo: L’accusa
 L’accusa inizia l’arringa con delle frasi taglienti e tendenziose. Secondo la sua ricostruzione le cellule microgliali, avvezze all’eutanasia, si sono dirette verso la zona sofferente dall’ipossia. I dati pubblici ci hanno depistato sull’effettivo orario di arrivo sul luogo del delitto, in realtà, recenti scoperte ci indicano che le cellule microgliali si trovavano già in loco prima del tempo dichiarato. Non è stato possibile vederle poiché sono arrivate con un travestimento non noto fino a poco tempo fa. Poi una volta arrivate sul luogo prefissato hanno iniziato a contornare alcuni neuroni in sofferenza. La microglia, adese ai neuroni ha liberato delle sostanze in uno spazio estremamente piccolo, troppo scarse per essere analizzate e troppo rapide per essere viste. In questo istante forse c’é stato un ‘errore’, ed al posto di sostanze neurotrofiche la microglia ha lasciato delle sostanze tossiche. Magari ha valutato che i neuroni non ce l’avrebbero fatta a passare indenni l’ipossia e li ha avvelenati in maniera irreversibile per eutanasia. Poi mentre i neuroni avvelenati stavano resistendo all’ipossia, il colpo di grazia, la microglia si é allontanata aggravando la situazione per il mancato sostentamento trofico. Ciò che ne é conseguito é la morte dei neuroni in circostanze apparentemente solitarie. Poi sono arrivate le cellule microgliali travestite da spazzine ed hanno pulito il luogo del delitto.
L’accusa inizia l’arringa con delle frasi taglienti e tendenziose. Secondo la sua ricostruzione le cellule microgliali, avvezze all’eutanasia, si sono dirette verso la zona sofferente dall’ipossia. I dati pubblici ci hanno depistato sull’effettivo orario di arrivo sul luogo del delitto, in realtà, recenti scoperte ci indicano che le cellule microgliali si trovavano già in loco prima del tempo dichiarato. Non è stato possibile vederle poiché sono arrivate con un travestimento non noto fino a poco tempo fa. Poi una volta arrivate sul luogo prefissato hanno iniziato a contornare alcuni neuroni in sofferenza. La microglia, adese ai neuroni ha liberato delle sostanze in uno spazio estremamente piccolo, troppo scarse per essere analizzate e troppo rapide per essere viste. In questo istante forse c’é stato un ‘errore’, ed al posto di sostanze neurotrofiche la microglia ha lasciato delle sostanze tossiche. Magari ha valutato che i neuroni non ce l’avrebbero fatta a passare indenni l’ipossia e li ha avvelenati in maniera irreversibile per eutanasia. Poi mentre i neuroni avvelenati stavano resistendo all’ipossia, il colpo di grazia, la microglia si é allontanata aggravando la situazione per il mancato sostentamento trofico. Ciò che ne é conseguito é la morte dei neuroni in circostanze apparentemente solitarie. Poi sono arrivate le cellule microgliali travestite da spazzine ed hanno pulito il luogo del delitto.
L’accusa continua rimarcando più volte il passato della microglia, come una cellula già avvezza al neuroomicidio (precedenti penali), inoltre ha mentito sull’orario di arrivo (depistaggi), si trovava vicino ai neuroni durante i fatti (opportunità), aveva dentro di sé l’arma del delitto (capacità), poteva girovagare indisturbato per il cervello con una discreta velocità (possibilità), si è allontanata con un travestimento prima che i neuroni si riprendessero causandone la morte (mancato soccorso). Ed in fine, l’arringa termina con una frase lapidaria: come nei più classici e proverbiali gialli, l’assassino è ritornato sul luogo del delitto ed ha rimosso le prove per fagocitosi (occultamento delle prove).
Non si tratta di un evento accidentale, ma di un pluriomicidio aggravato e premeditato di neuroni ed astrociti da parte di ‘servizi segreti deviati’ appartenenti al SNC.
La parola alla difesa
 La difesa risponde punto per punto con calma e freddezza.
La difesa risponde punto per punto con calma e freddezza.
Le multi identità sono parte del lavoro fisiologico della microglia. Queste cellule, infatti, in mancanza di collaboratrici, (es macrofagi, cellule presentanti l’antigene, cellule B etc,) devono necessariamente fare tutto da sole adattandosi di volta in volta alle nuove necessità. Sull’orario non c’é stata alcuna dichiarazione falsa, ogni cellula della microglia esprime o meno degli antigeni in funzione del lavoro che sta facendo, se non esistono ancora metodi per marcarli tutte ciò non indica alcuna colpevolezza.
Sulla questione delle sostanze tossiche e letali, é ovvio che una guardia giurata abbia sempre con sé la pistola ed il caricatore sempre pronti, tuttavia può anche avere con sé i materiali di primo soccorso. Fino ad ora non ci sono prove che la microglia abbia liberato sostanze tossiche verso i neuroni in quei momenti.
Anzi, l’imputato si è dimostrato utile per rimuovere le sostanze potenzialmente tossiche, ovvero quei residui post-ischemici che aumentano l’infiammazione e la sofferenza neuronale. Inoltre la microglia ha creato anche un ambiente idoneo per la formazione di nuove sinapsi per la ripresa post-danno.
La difesa poi ricorda che i topi transgenici che non hanno la microglia non sopravvivono all’embriogenesi, per cui stiamo trattando di cellule essenziali per la vita stessa. Poi cita gli innumerevoli casi in cui la microglia ha svolto ruoli eroici in difesa dei nostri delicati neuroni. Tutto questo non può essere cancellato da qualche sospetto e soprattutto da condizioni alle quali la microglia stessa non era preparata.
Se questo fosse un giallo…
 Se questo fosse un giallo non potrebbe mancare il classico colpo di scena. Questa volta arriva proprio da Mario Capecchi che scopre, in una sua recente pubblicazione su cell, che l’inattivazione della microglia provoca un fenotipo ossessivo-convulsivo. Quello che sorprende é che l’iniezione nel midollo osseo di cellule microgliali marcate e fluorescenti provoca la comparsa di cellule microgliali nel cervello. Ancora una volta la microglia ha mentito, e a quanto pare ha un passaggio segreto per oltrepassare la BEE, anche se oggi non é stato ancora possibile scoprire come. A quanto pare la microglia ha molti aspetti ancora oscuri, forse anche delle identità e dei passaporti che non conosciamo ancora.
Se questo fosse un giallo non potrebbe mancare il classico colpo di scena. Questa volta arriva proprio da Mario Capecchi che scopre, in una sua recente pubblicazione su cell, che l’inattivazione della microglia provoca un fenotipo ossessivo-convulsivo. Quello che sorprende é che l’iniezione nel midollo osseo di cellule microgliali marcate e fluorescenti provoca la comparsa di cellule microgliali nel cervello. Ancora una volta la microglia ha mentito, e a quanto pare ha un passaggio segreto per oltrepassare la BEE, anche se oggi non é stato ancora possibile scoprire come. A quanto pare la microglia ha molti aspetti ancora oscuri, forse anche delle identità e dei passaporti che non conosciamo ancora.
Inoltre come può l’iniezione midollare di una microglia inattiva causare un fenotipo psichiatrico? Siamo di fronte ad un personaggio davvero interessante.
Il giudizio
 Mettere insieme tutti questi dati sparsi non é semplice. Nella ricerca, infatti, é difficile soprattutto distinguere la verità obiettiva dalle interpretazioni, ed in questo lungo processo sono state fatte solo delle allusioni, niente di più. L’articolo di Capecchi parla di una interferenza sui recettori nocicettivi periferici da parte della microglia. Un topo con difficoltà nella percezione del dolore ha dei comportamenti anomali, ma non c’é niente di significativamente neurologico.
Mettere insieme tutti questi dati sparsi non é semplice. Nella ricerca, infatti, é difficile soprattutto distinguere la verità obiettiva dalle interpretazioni, ed in questo lungo processo sono state fatte solo delle allusioni, niente di più. L’articolo di Capecchi parla di una interferenza sui recettori nocicettivi periferici da parte della microglia. Un topo con difficoltà nella percezione del dolore ha dei comportamenti anomali, ma non c’é niente di significativamente neurologico.
La corte, quindi propone una nuova perizia. Verifichiamo cosa avviene in un topo transgenico capace di inattivare la funzione microgliale in maniera condizionata.
Il risultato é sconcertante, l’inattivazione condizionale della microglia, poco prima e durante l’ictus, provoca un notevole peggioramento del danno ischemico ed una sopravvivenza neuronale ridotta. Ovviamente ci sono state anche le critiche su quale gene é stato scelto per disattivare la microglia. Forse é stato scelto quel gene che sovraintende le funzioni microgliali ‘buone’. Si vedrà.
Tratta la somma, l’imputato é assolto per insufficienza di prove.
Conclusioni
Purtroppo, siamo ancora lontani dalla verità. Le indagini sulla microglia sono tutt’altro che concluse, si tratta di un campo in rapida espansione ed é sotto indagine per tantissime patologie come l’HIV, la sclerosi multipla, l’Alzheimer e tante altre patologie neurodegenerative.
Per ora il processo sull’ischemia é fermo per insufficienza di prove, ma qualcuno nel mondo sta ancora tentando di incastrare la microglia, chissà se ci sarà nuovamente qualche altro colpo di scena che la riporterà nuovamente sotto processo.
La ricerca, come al solito, non ha mai fine.
Alla prossima
Tags:
Animali transgenici,
Glia,
Ictus,
Ischemia Cerebrale,
microglia,
Neuroni
15 settembre 2009 - 6:48 pm
Qualcuno disse che non ci può essere giallo dove non ci sia anche il maggiordomo e la servitù. Il nostro poliziesco non ne è immune ovviamente, vediamo il proseguio delle indagini.
Preambolo
Continuiamo il nostro percorso in questo strano giallo, per chi non avesse seguito le puntate precedenti vi prego di visitare i seguenti links 1, 2, 3 e 4. Qui tratteremo un post di ‘transizione’, molto più semplice dei precedenti, ma che ci serve per capire i prossimi capitoli che saranno un po’ più complessi del solito.
Data la lunghezza eccessiva ho deciso di tagliare la storia in più sezioni, in questa vi presento la premessa (l’incontro). Come al solito sono bene accetti commenti di ogni tipo, suggerimenti per gli argomenti da trattare o migliorare.
La quiete dopo la tempesta
 Come abbiamo visto nel precedente post, il nostro ispettore cellulare è stato improvvisamente freddato dallo scagionamento del primo imputato eccellente. La teoria iniziale non faceva una grinza e c’erano anche molti indizi pesanti contro l’accusato. Purtroppo con il tempo e con l’uso di sostanze sempre più specifiche per il blocco del fattore transcrizionale la teoria della difesa ha avuto sempre più supporto. HIF-1 non è sicuramente una proteina da mettere tra i cattivi per l’ischemia cerebrale. A quanto pare c’è stato un grosso fallimento da cui abbiamo imparato a non concludere facilmente le indagini prima di approfondirle con cura.
Come abbiamo visto nel precedente post, il nostro ispettore cellulare è stato improvvisamente freddato dallo scagionamento del primo imputato eccellente. La teoria iniziale non faceva una grinza e c’erano anche molti indizi pesanti contro l’accusato. Purtroppo con il tempo e con l’uso di sostanze sempre più specifiche per il blocco del fattore transcrizionale la teoria della difesa ha avuto sempre più supporto. HIF-1 non è sicuramente una proteina da mettere tra i cattivi per l’ischemia cerebrale. A quanto pare c’è stato un grosso fallimento da cui abbiamo imparato a non concludere facilmente le indagini prima di approfondirle con cura.
Siamo quindi costretti a ritornare sui nostri passi ed ricominciare le indagini dall’inizio con più zelo, cercando di raccogliere informazioni sempre più precise e concordanti su cosa stava accadendo ai neuroni poco prima di morire.
Direi di iniziare l’interrogatorio su tutti i possibili testimoni oculari o detentori di informazioni cruciali.
Dove trovare i colpevoli?
 Pensare all’ipossia come innesco di un meccanismo che porterà a morte inevitabile per i neuroni non è male come teoria, tuttavia ci sono dei ricercatori che la pensano diversamente. Una volta, in un congresso un mio amico mi fece un’obbiezione inappellabile… per quanto possa essere interessante quel meccanismo che innesca la morte delle cellule, non c’è modo di evitarlo, un paziente arriva al pronto soccorso quando manifesta già i sintomi, ovvero quando c’è già stato “l’innesco letale”. Inoltre non è neanche possibile prevedere quando un individuo avrà un ictus, la nostra unica possibilità di aiutarlo risiede proprio in quella finestra di tempo che intercorre tra la comparsa dei sintomi e l’effettiva morte neuronale.
Pensare all’ipossia come innesco di un meccanismo che porterà a morte inevitabile per i neuroni non è male come teoria, tuttavia ci sono dei ricercatori che la pensano diversamente. Una volta, in un congresso un mio amico mi fece un’obbiezione inappellabile… per quanto possa essere interessante quel meccanismo che innesca la morte delle cellule, non c’è modo di evitarlo, un paziente arriva al pronto soccorso quando manifesta già i sintomi, ovvero quando c’è già stato “l’innesco letale”. Inoltre non è neanche possibile prevedere quando un individuo avrà un ictus, la nostra unica possibilità di aiutarlo risiede proprio in quella finestra di tempo che intercorre tra la comparsa dei sintomi e l’effettiva morte neuronale.
Se ci pensate è assurdo che le cellule siano ancora vive quando arrivano nelle nostre mani, e nonostante i nostri mezzi siamo incapaci evitarne la morte. Se vogliamo veramente fare qualcosa il primo punto dell’ordine del giorno deve essere fermare l’arma che ucciderà i neuroni, e solo dopo capire chi ha innescato il meccanismo ed è colpevole (scoprire il mandante).
Nel nostro caso dovremmo soffermarci sul perché le cellule non riescono più a gestire il calcio e muoiono. La soluzione di questo enigma sarà certamente correlata con la possibilità di salvare le cellule, mentre la cattura del mandante che ha scatenato la serie di eventi non servirà ad evitare nessun decesso cellulare al momento. Solo in un passaggio successivo potremmo chiarire anche chi ha causato tale massacro neuronale e perché.
Seguendo questa linea di pensiero in questo post ci concentreremo sui meccanismi di controllo e mantenimento dell’omeostasi ionica, cercando di fare il punto della situazione per poi trarne degli indizi.
La prima domanda è chi mantiene in ordine le concentrazioni ioniche intra ed extra cellulari?
 Se fate questa domanda ad un qualsiasi esperto nel settore vi dirà che ci sono migliaia di proteine che fanno ‘ordine’ tra i diversi ioni, e sono divise in famiglie, superfamiglie e classi. Questi meccanismi possono dividersi grossolanamente in pompe e trasportatori, in base al fatto che usano direttamente, o no, l’ATP.
Se fate questa domanda ad un qualsiasi esperto nel settore vi dirà che ci sono migliaia di proteine che fanno ‘ordine’ tra i diversi ioni, e sono divise in famiglie, superfamiglie e classi. Questi meccanismi possono dividersi grossolanamente in pompe e trasportatori, in base al fatto che usano direttamente, o no, l’ATP.
Tra le pompe più famose ci sono la Na+/K+ ATPasi che estrude sodio e fa entrare potassio, la pompa del calcio di membrana ed endoplasmatica (PMCA e SERCA), etc. Tra i trasportatori passivi i più noti sono lo scambiatore sodio/calcio (NCX), lo scambiatore sodio/calcio potassio (NCKX), lo scambiatore sodio/idrogeno (NHE), ed altri. Si tratta di un gruppo enorme di proteine che mettono continuamente in ordine i vari ioni, riportando continuamente le condizioni cellulari allo stato di riposo dopo le stimolazioni nervose che sono servite per attivare la cellula e per comunicare con il neurone successivo. E’ un po’ come avere delle cameriere e dei maggiordomi in una grande villa che mettono continuamente in ordine le camere ogni qual volta sono utilizzate.
Oggi ci concentreremo proprio su questi personaggi che stavano lì quando dalla calma apparente si è scatenata la disfatta neuronale.
La domanda ora è ‘Perché non hanno funzionato a dovere nel momento del bisogno?’
Vale la pena rispondere con chiarezza.
Prima domanda: Chi era in servizio durante l’ischemia e poco prima?
 A questa domanda c’è una risposta più o meno ovvia. Poco prima dell’ischemia funzionava tutto come al solito, nulla lasciava presagire il disastro, e tutte le proteine risiedevano al loro nomale posto fino a che è mancata l’energia necessaria per il trasporto attivo degli ioni. Quando è iniziata a mancare l’energia l’efficienza del trasporto ionico si è ridotta mentre il disordine ionico dei neuroni aumentava. Poco dopo questa fase gli unici che potevano fare qualcosa erano gli scambiatori ionici che non necessitano di ATP, ma il destino della cellula era oramai segnato; senza ATP non si può andare avanti per molto. Poi d’improvviso è arrivata nuova energia e tutto è cominciato a rifunzionare alla normalità fino al danno irreparabile.
A questa domanda c’è una risposta più o meno ovvia. Poco prima dell’ischemia funzionava tutto come al solito, nulla lasciava presagire il disastro, e tutte le proteine risiedevano al loro nomale posto fino a che è mancata l’energia necessaria per il trasporto attivo degli ioni. Quando è iniziata a mancare l’energia l’efficienza del trasporto ionico si è ridotta mentre il disordine ionico dei neuroni aumentava. Poco dopo questa fase gli unici che potevano fare qualcosa erano gli scambiatori ionici che non necessitano di ATP, ma il destino della cellula era oramai segnato; senza ATP non si può andare avanti per molto. Poi d’improvviso è arrivata nuova energia e tutto è cominciato a rifunzionare alla normalità fino al danno irreparabile.
In questa indagine tutto è sottoposto alla lente di ingrandimento, e nulla è dato per scontato, quindi le dichiarazioni vanno convalidate e come al solito andiamo in laboratorio con una ricostruzione del delitto per cercare di confutare tali ipotesi. In questo caso potremmo ricorrere ad esperimenti in vitro fatto con delle cellule neuronali sottoposte a dei modelli di deprivazione di ossigeno e glucosio, seguito dalla riossigenazione. Si tratta ovviamente di un modello molto semplice, ma che ci evita di sacrificare animali, e consente un maggiore grado di controllo delle condizioni sperimentali. Effettivamente quando manca ATP funzionano solo i trasportatori passivi, e la loro capacità di controllare l’omeostasi ionica è discreta considerando le condizioni di emergenza. Inoltre nulla sembra cambiare nell’assetto dei vari trasportatori attivi e passivi, dopotutto non c’è abbastanza energia e tempo per cambiare le cose con una sintesi/degradazione proteica. I sistemi sono ri-settati all’essenziale ed a tutto quello che può aiutare a tamponare i danni o trarre energia.
Se tutte queste considerazioni sono vere dobbiamo escludere chi non poteva funzionare al momento dell’ictus e considerare invece solo chi poteva ed ha fatto qualcosa…
La prossima domanda è quindi: Chi funzionava al momento e cosa stava facendo?
NCX: il maggiordomo
 A questo punto del racconto io mi recherei sul luogo del delitto alla ricerca di qualche indizio e soprattutto di qualche risposta.
A questo punto del racconto io mi recherei sul luogo del delitto alla ricerca di qualche indizio e soprattutto di qualche risposta.
Escludendo le pompe che fanno uso di ATP, tra i pochi trasportatori passivi che rimangono e che possono dare un consistente aiuto c’è lo scambiatore sodio/calcio (NCX).
Io immaginerei un ipotetico interrogatorio a questa proteina, magari in una stanza buia e fumosa.
Lei chi è?
NCX è una proteina di membrana fatta da circa 1.000 aminoacidi che è presente in tutte le cellule dei mammiferi e che fisiologicamente espelle il calcio citosolico in cambio dell’ingresso di sodio.
Da quanto tempo è in servizio?
In pratica quasi tutti gli organismi possiedono uno scambiatore del calcio, e sono tutti filogeneticamente collegati da un gene ancestrale che si è mantenuto molto conservato sia nella sua struttura che nella sua funzione. In altre parole è una proteina presente negli archeobatteri, funghi, piante, fino a tutte le cellule eucariotiche di mammifero, quindi una proteina davvero molto conservata…
Davvero notevole, ma mi dica… qual è la Sua funzione nel cervello e con chi collabora solitamente?
Sappiamo bene che, quando i neuroni si trovano a riposo, le concentrazioni ioniche sono mantenute soprattutto da pompe che fanno uso di energia sottoforma di ATP. In queste condizioni un trasportatore passivo come NCX funziona relativamente poco, poiché ha una bassa affinità per il calcio e per il sodio. Tuttavia le condizioni cambiano drasticamente dopo l’eccitazione neuronale, ovvero quando le concentrazioni di calcio citosolico aumentano improvvisamente a dismisura, le pompe si saturano e non riescono a riportare la cellula alle condizioni ioniche di riposo. In queste circostanze entrano in funzione NCX e proteine simili che hanno una bassa affinità per gli ioni, ma possono trasportarne enormi quantità in pochi istanti.
In pratica NCX espelle uno ione calcio mediante scambio con tre ioni sodio che entrano nella cellula, (proprio da questo deriva il suo nome).
Quindi Lei è specializzato nelle condizioni di ‘emergenza’, ovvero quando le pompe non riescono a mettere ordine… cosa mi sa dire riguardo all’ipossia? cosa stava facendo in quei momenti?
La risposta sarebbe ovvia. NCX stava espellendo il calcio dalle cellule sfruttando l’unica fonte di energia disponibile al momento ovvero il gradiente del sodio.
Perché?
Come già abbiamo accennato nei post precedenti il calcio è un ottimo segnale citosolico, ma quando supera certi livelli può causare disastri, quindi l’azione di NCX è in linea con le aspettative.
Ha visto qualcosa di strano in quei ‘momenti’? Può dirmi qualcosa a tal riguardo?
Quello che NCX ha visto è che la pompa del calcio in una prima fase era efficiente e riusciva a mantenere le concentrazioni di calcio citosolico a livelli estremamente bassi, ma riusciva ad espellere solo pochi ioni alla volta. Ad un certo punti si stava accumulando il calcio, la pompa è andata subito in saturazione e non riusciva ad espellere abbastanza ioni… poi è cominciata a mancare l’energia e l’efficienza di estrusione si è ridotta sempre di più. Si stava accumulando calcio citosolico oltre i normali livelli e tempi sopportabili per il neurone, per cui NCX è entrato in funzione ed ha espulso fino ad oltre 10.000 volte più ioni calcio nell’unità di tempo rispetto alla pompa in presenza di ATP, un fenomeno insomma.
…e cosa sa dirmi su cosa sia successo negli ultimi ‘istanti di agonia’? Alla fine è riuscito a tenere sotto controllo il calcio?
Effettivamente ci è riuscito parzialmente, poiché durante l’ipossia le concentrazioni di calcio si sono mantenute più o meno stabili per quanto fosse possibile farlo senza utilizzare ATP, e soprattutto fatto in così poco tempo… successivamente al ritorno dell’ossigeno tutto è tornato ad una apparente normalità; il livello di calcio citosolico è tornato nel suo normale range di concentrazioni citosoliche, quindi tutto ok, passata la tempesta è stato ovvio pensare che il peggio era oramai passato. Tuttavia, dopo un po’ qualcosa è cominciato ad andare sempre peggio, ci sono stati degli sbalzi di calcio improvvisi sempre più gravi, e la cellula si è resa conto ad un certo punto che non era possibile recuperare la situazione e si è arrivati all’inevitabile. Quei momenti sono stati talmente turbolenti che non è stato possibile capire cosa stesse succedendo.
Uhmm.. Per ora l’interrogatorio è finito, e diciamo che siamo soddisfatti delle informazioni raccolte…
Riepilogando, stiamo parlando di una proteina molto conservata, al che se ne potrebbe dedurre che il suo ruolo sia fondamentale per la sopravvivenza; insomma sembra interessante, ma purtroppo non sembra essersi aperta alcuna strada per noi. Praticamente non ci ha detto nulla.
C’è un’altra cosa…
 Ritornando in ufficio c’è una cosa che non quadra… questo trasportatore passivo dove ha trovato tutta questa energia per espellere una quantità di calcio ionico così colossale? Una pompa del calcio consuma circa 1 ATP per 1 ione calcio, possibile che NCX abbia lavorato gratis contro ogni legge della termodinamica? In altre parole quanto è costato alla cellula questo ‘servizio’?
Ritornando in ufficio c’è una cosa che non quadra… questo trasportatore passivo dove ha trovato tutta questa energia per espellere una quantità di calcio ionico così colossale? Una pompa del calcio consuma circa 1 ATP per 1 ione calcio, possibile che NCX abbia lavorato gratis contro ogni legge della termodinamica? In altre parole quanto è costato alla cellula questo ‘servizio’?
Ovviamente NCX ha sfruttato il gradiente di sodio tra l’ambiente extracellulare e quello intracellulare, ed in questo modo ha potuto espellere il pericoloso calcio dalla cellula scambiandolo con l’innocuo sodio…
Ma cosa succede a tutto quel sodio che NCX ha fatto entrare nella cellula e che non può essere espulso dalla pompa sodio/potassio?
Se sono stati necessari 3 ioni sodio per espellere ciascuno ione calcio, facendo dei semplici calcoli, a naso direi che nella cellula si sarà accumulato tanto di quel sodio da innescare altri meccanismi, ad esempio alterare il potenziale di membrana.
Se questo fosse vero la depolarizzazione causerebbe l’attivazione della cellula, con rilascio di neurotrasmettitori e conseguenze da definire. Sicuramente potremmo parzialmente spiegare l’ipereccitabilità, il calcio che rientra nuovamente nelle cellule e le onde di eccitazione neuronale che si espandono dal core ischemico.
La situazione non è molto chiara, e tornando alla centrale io darei un’occhiata allo schedario delle fedine penali, www.pubmed.gov , in cerca di cosa si sappia in giro di questo ‘maggiordomo’.
Da una rapida occhiata possiamo vedere che è correlato con numerosi meccanismi, NCX si lega con pompe e trasportatori ed esalta alcune caratteristiche dei canali ionici. Però qualcosa è più importante di tutto, è stato visto correlato con l’ischemia cardiaca; leggendo bene possiamo vedere che l’uso di farmaci che inibiscono l’attività di NCX diminuisce l’estensione della morte del miocardio in seguito all’infarto.
L’ipotesi è che la cellula si sia talmente indebitata di energia durante l’ipossia che al ripristino delle condizioni ottimali non ce n’è abbastanza per ristabilire il gradiente di sodio e reimpostare le condizioni di riposo. Un giro vizioso che può portare solo al disastro, come aver chiesto dei soldi ad uno strozzino.
Una crepa sul vetro cristallino di NCX: Calunnie?
 Uhmm… Forse calunnie, leggendo bene qua e là i farmaci utilizzati per inibire NCX non sono molto specifici, agiscono anche su altri canali; magari NCX è stato coinvolto in qualcosa di più grande ed è stato usato come capro espiatorio. Improbabile che una proteina così letale possa essere conservata per milioni di anni durante l’evoluzione se non migliori sensibilmente il fitness dell’organismo.
Uhmm… Forse calunnie, leggendo bene qua e là i farmaci utilizzati per inibire NCX non sono molto specifici, agiscono anche su altri canali; magari NCX è stato coinvolto in qualcosa di più grande ed è stato usato come capro espiatorio. Improbabile che una proteina così letale possa essere conservata per milioni di anni durante l’evoluzione se non migliori sensibilmente il fitness dell’organismo.
Per dare una prova decisiva possiamo utilizzare, come tutti voi sapete, la prova del nove… un topo transgenico knock-out per NCX e verificare cosa succede.
In questo modello, infatti, se non ci sono variazioni dell’espressione degli altri canali/trasportatori c’è la massima specificità dell’inibizione di questa proteina… e quindi potremmo ufficialmente capire se si tratta di una proteina così cattiva.
Andiamo in lab e chiediamo di sviluppare il topo knock-out. Passano anni e qui il primo intoppo, il topo muore durante l’embriogenesi per mancato battito cardiaco. Si tratta di una scoperta senz’altro interessante ma sono anche anni di lavoro buttati al vento senza una risposta. Rifare tutto il lavoro daccapo e passare altri anni a sviluppare un altro topo? Uhmm…
Qualcuno ha suggerito una soluzione da fantascienza che potrebbe risolvere la situazione, ovvero utilizzare un virus in grado di infettare i cardiomiociti dell’embrione knock-out ed inserire in queste cellule il cDNA di NCX in maniera transiente… insomma abbastanza per attivare il battito cardiaco, poi successivamente l’espressione calerà di nuovo quando il topo non sarà più infettato.
Lo sviluppo della metodologia ha impiegato un paio di anni con risultati sconfortanti, il risultato è stato che l’espressione transiente di NCX nei cardiomiociti non serve a nulla. La mancanza di NCX è fondamentale per la vita dell’animale, probabilmente è necessaria l’espressione anche in altri tessuti (es le cellule pacemaker del cuore, di tipo nervoso), oppure è necessaria una espressione ancora più precoce della proteina, magari quando non si è ancora formato il primo abbozzo di cuore.
Disperati, si è ricorsi a strategie farmacologiche sempre più complesse, ma i risultati sono stati discordanti e dubbi; mancano sempre di selettività e specificità.
Il volo Pindarico
 Le cose, da allora, non sono andate molto avanti, le pubblicazioni si sono rincorse tra di loro in un misto di ripetizioni e staccate con farmaci sempre più specifici e potenti. A questi articoli facevano seguito altri che descrivevano dell’effetto di queste sostanze sulla circolazione, ipertensione, inibizione di canali del calcio, respirazione mitocondriale, disaccoppiamenti mitocondriali etc etc.
Le cose, da allora, non sono andate molto avanti, le pubblicazioni si sono rincorse tra di loro in un misto di ripetizioni e staccate con farmaci sempre più specifici e potenti. A questi articoli facevano seguito altri che descrivevano dell’effetto di queste sostanze sulla circolazione, ipertensione, inibizione di canali del calcio, respirazione mitocondriale, disaccoppiamenti mitocondriali etc etc.
Tuttavia per fare una buona ricerca c’è bisogno di determinazione, genialità ed anche un po’ di fortuna, tutte caratteristiche ben rappresentate nel padre di NCX, Kenneth Philipson, quando a sorpresa decide di intraprendere un nuovo e più Pindarico volo, investendo diversi anni nella generazione di un nuovo topo knock-out per NCX, ma questa volta condizionato (tecnica Cre/LoxP). Si tratta di una tecnica citata già più volte e che funziona bene, in poche parole il topo nascerà con una normale espressione di NCX in tutto l’organismo, poi ad un certo punto l’enzima Cre, come una bomba ad orologeria, eliminerà il gene di NCX solo nei cardiomiociti e darà un topo adulto privato improvvisamente di NCX.
Per i più curiosi il meccanismo sfrutta il cambio della catena pesante della miosina dei cardiomiociti subito dopo la pubertà. In questi topi transgenici insieme al promotore della catena pesante della miosina c’è una ricombinasi che andrà a distruggere il gene ncx causando un knock-out tessuto e tempo specifico.
Non vi dico del rischio che il topo muoia proprio quando la proteina verrà a mancare e vanificare ancora una volta il lavoro di anni di sacrifici.
Passarono degli anni e finalmente eravamo arrivati vicino al fatidico momento, la nascita del primo topo transgenico. Da quel momento devo dire che c’è stata una lunga agonia misto di silenzio ed impazienza aspettando quel fatidico momento in cui un topolino che ha in sé tutte le promesse di questo mondo deve passare per quell’unico istante in cui diventerà knock-out e dimostrerà al mondo se è possibile vivere senza una specifica proteina cardiaca.
Purtroppo capita anche di affezionarsi ad un animale che vivendo darà inconsapevolmente un enorme contributo alla ricerca. I giorni passavano ed il topo alla sua maturità sessuale era ancora vivo e vitale, le analisi non hanno dimostrato anomalie cardiache e tutto procede come nulla fosse. Così è stato anche per le nidiate successive e la biochimica ha dato l’ok, questi topi adulti hanno un knock-out cardiaco. Si decide di fare l’ischemia cardiaca e il risultato è stato sconcertante. La mancanza di NCX nel cuore provoca un’entità del danno al miocardio pari al 50% circa rispetto ai topi wild-type.
NCX è sicuramente colpevole… un fulmine nel cielo sereno, una pubblicazione che cambierà definitivamente la storia di questo trasportatore.
Su questo modello animale sono stati poi tentati tantissimi esperimenti, soprattutto con quei farmaci così potenti e specifici per NCX; i risultati hanno dimostrato in maniera incontrovertibile che gli effetti ottenuti erano dovuti all’azione su altre proteine, è stato solo un caso che l’uso di queste sostanze dimostrano gli stessi effetti del knock-out per NCX.
Quello che succede al cuore succede anche al cervello?
 Analisi su analisi in diverse salse hanno dimostrato che questa proteina è fondamentale per alcuni meccanismi cardiaci e non solo, ma sicuramente esalta anche il danno ischemico al miocardio. E’ una circostanza difficile da spiegare in termini evoluzionistici e non è possibile capirne a fondo il meccanismo esatto.
Analisi su analisi in diverse salse hanno dimostrato che questa proteina è fondamentale per alcuni meccanismi cardiaci e non solo, ma sicuramente esalta anche il danno ischemico al miocardio. E’ una circostanza difficile da spiegare in termini evoluzionistici e non è possibile capirne a fondo il meccanismo esatto.
Qualcuno fa notare che sia l’eccesso di ioni sodio durante il lavoro di NCX a causare danno per osmosi; tre ioni sodio per miliardi di ioni calcio determinerebbero uno squilibrio osmotico che liserebbe la membrana cellulare formando prima delle bolle sulla superficie e poi la rottura fino alla morte.
Ovviamente la trasposizione al cervello è immediata, se fa male al cuore potrebbe far male anche ai neuroni?
La situazione non è semplice, abbiamo diverse opzioni per verificare questa ipotesi e nessuna di queste è facile.
L’esperimento più determinante potrebbe essere, come al solito, la generazione di un knock-out per NCX nel cervello, però si corre nuovamente il rischio di un nuovo tonfo in acqua, poiché potrebbe mancare l’embriogenesi del SNC e quindi aborto precoce. Se questo dovesse avvenire avremmo speso tempo e denaro inutilmente, per non parlare delle sofferenze indotte sugli animali.
D’altra parte fare dei knock-out tessuto specifico, soprattutto per il cervello, è difficile, lungo e dispendioso; per ora accantoniamo l’idea fino a che non sia strettamente necessario.
Potremmo ricorrere a dei saggi alternativi per chiarire la situazione, e magari li vediamo nella prossima puntata.
Conclusione
Si potrebbe definire serendipità: cercare un ago in un pagliaio e trovarci la figlia del contadino (Julius H. Comroe).
Stavamo brancolando nel buio in cerca di prove e ci siamo scontrati con un pregiudicato per il danno cardiaco ischemico camuffato da semplice faccendiere delle pulizie da calcio.
Nelle prossime puntate analizzeremo meglio il personaggio, il suo ruolo nel cuore e poi nel cervello, cercheremo nuove prove a cui ovviamente farà seguito il ‘processo’ per concorso in neuro-omicidio.
Alla prossima
Tags:
Animali transgenici,
Calcio,
Cre/LoxP,
Ictus,
Ischemia Cerebrale,
NCX,
Neuroni,
Neuroscienze,
PMCA,
pompe,
Potenziali d'azione,
sodio
4 settembre 2009 - 1:00 pm
Preambolo
Finalmente le tanto meritate vacanze sono iniziate anche per me, e colgo l’occasione per finire finalmente questo post in elaborazione oramai da tanto tempo, come al solito cortesemente corretto da Valentina. Qui descriverò un argomento abbastanza lungo, difficile e ‘spigoloso’ per i profani ed esperti, anche se penso che tutti lo conoscono almeno un po’ per sentito dire.
Parleremo dell’olfatto, un argomento non facile da raccontare in un post divulgativo senza ‘smussare’ qua e là il mosaico di teorie e di esperimenti che sono stati fatti fino ad ora.
L’Olfatto: Alcuni dettagli ovvi

Come al solito mi servirò inizialmente di qualche punto di riferimento per metterci d’accordo ed inizierò dagli odori che sono causati, come tutti voi sapete, da molecole sprigionate dalle sostanze e disperse nell’aria che respiriamo, dove raggiungono il nostro naso. L’altro punto di riferimento utile si trova subito dietro il naso e sopra la volta della nostra cavità buccale dove passano tutte le molecole che noi respiriamo. E’ una cavità rivestita da una mucosa di circa 10 cm2 che attraverso la solubilizzazione, la dispersione, l’adsorbimento e quant altro, ferma una porzione delle molecole che si trovano nello stadio aeriforme nella cavità nasale e le disperde nel fluido mucoso. Qui le molecole possono incontrare una o più cellule recettoriali olfattive (ORC), in un uomo adulto se ne contano circa 10-20 milioni, ricche di propagini dette ciglia e di proteine dette recettori olfattivi (da qui chiamate Odorant Receptor OR).
I OR hanno il compito ‘legare’ in maniera più o meno specifica alcuni gruppi funzionali di queste molecole presenti nel fluido mucoso, ed innescare una cascata di eventi che si amplifica fino ad attivare la cellula recettrice e scatenare la propagazione del ‘segnale odoroso’. Il cervello, a sua volta, provvederà ad interpretare il segnale in diversi stadi con una serie di meccanismi molto complessi. Per dettagli ed approfondimenti potete guardare questo link.
Fin qui il tutto è quasi scontato ed ovvio, però dalla teoria alla pratica c’è una notevole differenza, vi dico subito che ancora oggi ci sono vari lati oscuri che cercherò di descrivervi in parole semplici, portandovi ai problemi scientifici in maniera intuitiva per quanto sia nelle mie capacità.
Quanti odori esistono?
 Come penso molti di voi possono intuire, esiste un numero inimmaginabile di odori, e la maggioranza di questi è causato da un mix di ‘odori primari’ in diversi rapporti, ma a complicare la situazione c’è che una molecola odorosa può agire su decine di recettori diversi con diversa specificità. I OR dei composti aminici, ad esempio, riconoscono solamente l’azoto primario, secondario o terziario con diversa efficacia, per cui gli odori di questi composti non possono essere discriminati con facilità e sembrano tutti molto simili. C’è da dire però che nonostante questa piccola sovrapposizione di segnali si possono discriminare con elevata sensibilità circa 10.000 odori diversi.
Come penso molti di voi possono intuire, esiste un numero inimmaginabile di odori, e la maggioranza di questi è causato da un mix di ‘odori primari’ in diversi rapporti, ma a complicare la situazione c’è che una molecola odorosa può agire su decine di recettori diversi con diversa specificità. I OR dei composti aminici, ad esempio, riconoscono solamente l’azoto primario, secondario o terziario con diversa efficacia, per cui gli odori di questi composti non possono essere discriminati con facilità e sembrano tutti molto simili. C’è da dire però che nonostante questa piccola sovrapposizione di segnali si possono discriminare con elevata sensibilità circa 10.000 odori diversi.
Ciò premesso, consentitemi da questo punto in poi di semplificare e di concentrarci esclusivamente sugli ‘odori primari‘ che sono riconosciuti quasi esclusivamente da un solo tipo di OR e che danno una sensazione odorosa molto precisa.
Cosa c’è di difficile?
 Nel mondo animale, il non saper distinguere l’odore di una preda dall’odore del proprio predatore fa la differenza tra fare una buona colazione ed essere la colazione di qualcun altro. Anche riconoscere l’odore delle cose che si possono mangiare da quelle che è meglio evitare è fondamentale per la sopravvivenza, quindi i mammiferi durante l’evoluzione hanno accumulato più di 1.000 geni che sovraintendono il più misterioso dei 5 sensi. In pratica più del 3% del genoma dei mammiferi è deputato alla percezione degli odori, e dato che questi recettori possono riconoscere anche più tipologie di molecole con diversa affinità determinando una combinazione di interazioni intermedie, questo amplifica esponenzialmente il ventaglio di sensazioni che possono dare le molecole presenti nell’aria.
Nel mondo animale, il non saper distinguere l’odore di una preda dall’odore del proprio predatore fa la differenza tra fare una buona colazione ed essere la colazione di qualcun altro. Anche riconoscere l’odore delle cose che si possono mangiare da quelle che è meglio evitare è fondamentale per la sopravvivenza, quindi i mammiferi durante l’evoluzione hanno accumulato più di 1.000 geni che sovraintendono il più misterioso dei 5 sensi. In pratica più del 3% del genoma dei mammiferi è deputato alla percezione degli odori, e dato che questi recettori possono riconoscere anche più tipologie di molecole con diversa affinità determinando una combinazione di interazioni intermedie, questo amplifica esponenzialmente il ventaglio di sensazioni che possono dare le molecole presenti nell’aria.
La chiave di volta per ottenere un buon olfatto è sicuramente il collegamento tra le cellule recettoriali odorose (ORC) ed il cervello, ovvero quel meccanismo che consente di poter capire quale specifico OR è stato attivato. Si tratta di un meccanismo per nulla banale, e come punto di riferimento, possiamo considerare l’esempio del gusto, dove i recettori cellulari sono generati in base alla localizzazione sulla superficie della lingua. Nel cervello si forma una sorta di correlazione tra aree specifiche corticali ed aree della lingua denominata ‘mappa sensoriale‘. A questo consegue che è possibile percepire il salato, l’amaro, il dolce ed l’acido in base a quale zona della lingua è stata stimolata maggiormente.
Possiamo trasportare questa ipotesi nell’olfatto, ed immaginare che l’area in cui si trovano le ORC determina anche il set di recettori da esprimere. Ipotizziamo che ciascuna cellula recettrice dell’olfatto possa esprimere un centinaio o più OR localizzati in diverse aree della mucosa nasale. Ogni area in cui vi sono le ORC potrebbe essere correlata ad una zona del cervello a cui corrisponderebbero determinate sensazioni odorose.
Quanti recettori per cellula?
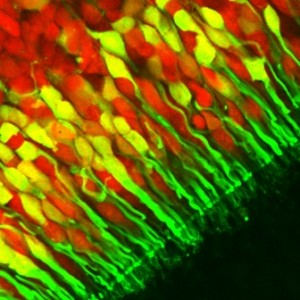 Sapere quanti tipi di recettori sono presenti per cellula è fondamentale per capire quante aree ci dovremmo aspettare di trovare e per verificarlo potremmo ricorrere a tecniche avanzatissime di in situ hybridization, e di retrotrascrizione ed amplificazione per PCR su singola cellula. Ovviamente non sono tecniche facili e nemmeno tanto diffuse, ma gli esperti sono riusciti a dimostrare con questi esperimenti che ogni ORC esprime solamente un singolo OR.
Sapere quanti tipi di recettori sono presenti per cellula è fondamentale per capire quante aree ci dovremmo aspettare di trovare e per verificarlo potremmo ricorrere a tecniche avanzatissime di in situ hybridization, e di retrotrascrizione ed amplificazione per PCR su singola cellula. Ovviamente non sono tecniche facili e nemmeno tanto diffuse, ma gli esperti sono riusciti a dimostrare con questi esperimenti che ogni ORC esprime solamente un singolo OR.
Una cosa simile avviene durante il differenziamento cellulare, dove la combinazione di alcuni fattori trascrizionali decide l’attivazione di meccanismi sempre più specializzati che ‘bloccano’ l’espressione specifica di determinati geni. Questo meccanismo, definito ‘deterministico’, è quello maggiormente utilizzato durante la specializzazione cellulare nel nostro organismo. Potremmo ipotizzare un meccanismo simile per le ORC in cui dalla combinazione di alcuni fattori trascrizionali si determina l’attivazione dell’espressione di un singolo OR.
Verifica della Teoria Deterministica
 Secondo questa teoria la combinazione casuale o pseudocasuale di fattori trascrizionali per esprimere un singolo OR non può essere disturbata dalla coespressione di un OR transgenico scelto da noi. Per verificare questa teoria ‘deterministica‘, quindi, possiamo generare un topo transgenico in cui alcune ORC esprimono in maniera forzata un determinato OR scelto da noi e valutare se c’è coespressione.
Secondo questa teoria la combinazione casuale o pseudocasuale di fattori trascrizionali per esprimere un singolo OR non può essere disturbata dalla coespressione di un OR transgenico scelto da noi. Per verificare questa teoria ‘deterministica‘, quindi, possiamo generare un topo transgenico in cui alcune ORC esprimono in maniera forzata un determinato OR scelto da noi e valutare se c’è coespressione.
Il risultato è interessante, non c’è alcuna sovrapposizione di segnali tra il OR espresso forzatamente da noi ed un qualsiasi altro recettore olfattivo endogeno. In pratica l’espressione forzata del nostro OR transgenico non permette di esprimere un qualsiasi altro OR endogeno, e se si tenta di generare un topo transgenico con una espressione forzata di due OR diversi nella stessa ORC, queste muoiono per apoptosi. Questi dati non sono di certo a supporto per la teoria deterministica, evidentemente la scelta del recettore olfattivo è un meccanismo molto più complesso. Ad aggiungere benzina sul fuoco c’è un’altra prova interessante, ovvero le ORC possono cambiare più volte il recettore odoroso espresso prima di prendere contatto con il cervello (maturazione cellulare). La teoria deterministica è molto fallace con questi risultati, poco probabile che sia quella buona.
La Teoria Stocastica
 Un’altra teoria che si è fatta strada nel tempo è basata sulla casualità della scelta del OR espresso (teoria stocastica). Per capirci immaginiamo un fattore trascrizionale unico che sia in grado di legare il promotore di tutti i geni dei OR e di consentirne l’espressione; tecnicamente può legarsi ad un solo OR e quindi può esprimere solo quello. Se il fattore trascrizionale non è molto efficiente nell’esprimere un OR si potrebbe spiegare come mai una ORC cambia OR nei primi stadi pur seguendo sempre la regola di esprimere un solo OR alla volta. In seguito, quando un OR espresso dà un forte segnale di funzione (feed-back) il fattore trascrizionale si fissa sul gene che sta trascrivendo fino allo stadio di maturazione.
Un’altra teoria che si è fatta strada nel tempo è basata sulla casualità della scelta del OR espresso (teoria stocastica). Per capirci immaginiamo un fattore trascrizionale unico che sia in grado di legare il promotore di tutti i geni dei OR e di consentirne l’espressione; tecnicamente può legarsi ad un solo OR e quindi può esprimere solo quello. Se il fattore trascrizionale non è molto efficiente nell’esprimere un OR si potrebbe spiegare come mai una ORC cambia OR nei primi stadi pur seguendo sempre la regola di esprimere un solo OR alla volta. In seguito, quando un OR espresso dà un forte segnale di funzione (feed-back) il fattore trascrizionale si fissa sul gene che sta trascrivendo fino allo stadio di maturazione.
E’ una teoria che funziona e che spiega anche i risultati dei topi transgenici; il OR transgenico blocca l’espressione di altri recettori attraverso un feed-back abberrante. Però, come al solito la teoria va convalidata, e c’è l’imbarazzo della scelta sul come; una prova schiacciante potrebbe derivare dall’eliminazione del feed-back recettoriale. In particolare potremmo alterare un gene OR in modo tale da codificare un recettore non funzionante pur conservandone la struttura genica.
I risultati dimostrano che il topo transgenico non esprime mai un OR non funzionante, probabilmente proprio per la mancanza del feed-back del recettore maturo necessario per fissare la scelta. Per esserne sicuri, è stata effettuata una controprova per dimostrare che le ORC tentano di esprimere il OR non funzionante, e che solo successivamente cambiano la scelta su un altro gene OR che funzioni. Per dimostrarlo si è generato un topo transgenico in cui l’espressione anche transiente del recettore non funzionante provoca un danno irreversibile al DNA della stessa cellula (tecnica Cre/LoxP), ed i risultati hanno mostrato che le ORC scelgono il OR transgenico e non funzionante con la stessa probabilità di tutti gli altri OR, sebbene questa scelta sia cambiata prima della maturazione cellulare per mancanza di feed-back. Un’altra prova conclusiva e schiacciante è che la generazione di un topo trangenico che esprime un OR esogeno e non funzionante non disturba l’espressione dei OR endogeni. Questo dimostra che è la funzione di un OR a bloccare l’espressione dei OR endogeni, non la struttura e l’espressione dei geni OR endogeni.
La spina nel fianco per la Teoria Stocastica
La teoria stocastica fino ad ora ha sempre soddisfatto tutti i dati sperimentali ottenuti, ma ciononostante ha un punto debolissimo. Questa teoria è retta dalla possibilità di poter innescare la trascrizione di qualsiasi dei 1.000 geni dei OR da uno o pochi fattori trascrizionali, e questo sarebbe possibile solo nel caso in cui i geni OR presentino una sequenza consenso che li identifichi nel genoma. Ebbene, nonostante molti ricercatori si siano impegnati nell’analisi di omologie di sequenze tra i geni degli OR, i risultati ottenuti sono stati alquanto deludenti; con i dati attuali si potrebbero raggruppare non più di una decina di geni degli OR per volta tirando in ballo meccanismi di riconoscimento improbabili.
E se fossero dei Linfociti?
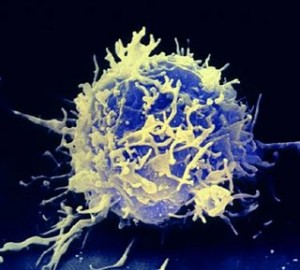 Se ci pensate, esiste un meccanismo di scelta molto simile che avviene nei linfociti. Queste cellule, però, non decidono l’anticorpo da esprimere in base a fattori trascrizionali, ma attraverso una ricombinazione genetica guidata. Si tratta di una piccola deviazione della teoria stocastica ed è anche risolutiva.
Se ci pensate, esiste un meccanismo di scelta molto simile che avviene nei linfociti. Queste cellule, però, non decidono l’anticorpo da esprimere in base a fattori trascrizionali, ma attraverso una ricombinazione genetica guidata. Si tratta di una piccola deviazione della teoria stocastica ed è anche risolutiva.
Come al solito dobbiamo convalidare tale teoria… ed escludiamo subito la proposta di sequenziare l’intero genoma di singole cellule, sarebbe difficilissimo e ci vorrebbero tanti anni! Possiamo ricorrere ad un trucco chiamato FISH (fluorescent in situ hybridization), ovvero rendere fluorescente una sonda ad RNA verso un introne di un OR. In questa tecnica non è possibile valutare una ricombinazione genica in maniera diretta, tuttavia è possibile localizzare dove inizia la trascrizione di un determinato gene all’interno del nucleo e valutare se, in seguito ad una ricombinazione, cambia posizione. I risultati, alquanto discutibili, dimostrano che il sito di inizio della trascrizione avviene sempre nello stesso punto del nucleo e del genoma, quindi niente ricombinazione, ma c’è una novità inaspettata; la trascrizione di un OR proviene solamente da un singolo allele.
Sbrogliare la matassa di informazioni non è mai facile

Spesso nella ricerca è importante definire delle ipotesi e porsi le domande giuste, ovvero cercare di identificare la cosa più importante di un meccanismo e trarne quante più informazioni possibili per verifica e deduzione. Nel nostro caso la codifica di un singolo allele, cioè solo 1 delle due copie genetiche di un OR, è ancora in linea con la teoria della ricombinazione genetica, poiché se è vero che la scelta è casuale, questa non può avvenire in entrambi gli alleli fratelli allo stesso modo. Inoltre se l’inizio della trascrizione avviene sempre nello stesso punto, questo non esclude che tutto il resto del DNA (es il promotore) possa essere stato ricombinato.
L’ipotesi che ne scaturisce è questa: La cellula sceglie un OR da esprimere in modo casuale, in mancanza di un feed-back funzionale cambia scelta, in seguito, alla maturazione cellulare la scelta diventa definitiva mediante ricombinazione di un promotore o di segnali a monte dell’OR scelto. Questa ipotesi potrebbe spiegare come mai l’espressione forzata di un recettore esogeno possa bloccare l’espressione dei recettori endogeni; probabilmente la proteina inserita provoca un feed-back che innesca una ricombinazione abberrante del DNA nei OR endogeni. La teoria per ora tiene ma con le parole non si dimostra mai niente, è fondamentale convalidare la teoria e questa volta non è per nulla facile evidenziare tante piccole ricombinazioni in singole cellule di 20 micron di diametro circa.
Come dimostrare una ricombinazione che si possa trovare in un qualsiasi punto del genoma? In questo caso il test di validazione è non semplicissimo. L’idea è che la ricombinazione del DNA in una ORC provocherebbe il blocco dell’espressione di un determinato OR in tutte le condizioni, come avviene per un linfocita. Se da questo DNA ricombinato si clonasse il topo stesso da cui deriva… l’animale che risulterebbe dovrebbe esprimere solo un OR, poiché il suo DNA è già ricombinato in maniera irreversibile. I risultati sono stati scioccanti, il topo che ne risulta è perfettamente sano e ha tutto l’apparato olfattivo intatto e funzionante come in un qualsiasi wild-type. Nonostante l’analisi di circa 100 kb a monte ed a valle del gene incriminato non c’è stata nessuna modifica genetica o epigenetica.
Basta un soffio ed il castello crolla
 Certamente la ricombinazione è da scartare ma fino ad ora niente ha smentito la casualità della scelta del OR. Tuttavia un gruppo di ricerca ha recentemente messo in discussione anche questa ipotesi granitica.
Certamente la ricombinazione è da scartare ma fino ad ora niente ha smentito la casualità della scelta del OR. Tuttavia un gruppo di ricerca ha recentemente messo in discussione anche questa ipotesi granitica.
L’idea di fondo è la seguente… Se è vero che la cellula sceglie casualmente un gene su circa 1.000, e di questo solo 1 allele, ne consegue che la scelta è di 1 sui 2.000 alleli disponibili. Se riuscissimo ad inattivare solo 1 di questi 2.000 alleli, ad esempio in modo tale che esprima irreversibilmente EGFP (tecnica Cre/loxP), potremmo rendere fluorescenti le cellule che hanno ‘cambiato idea’ per mancanza di feed-back e verificare quale altro gene sceglie dei 1.999 rimanenti.
Il risultato, ancora una volta, è assolutamente strabiliante. Il topo transgenico presenta una coespressione di EGFP solo con il suo allele funzionante corrispondente. In poche parole l’espressione di EGFP, come previsto, non dà feed-back positivo per cui la cellula cambia OR da esprimere; ma la seconda scelta non è per niente casuale, qualcosa guida la scelta sull’allele di ‘backup’ presente sul cromosoma fratello e non sugli altri 1.998 alleli rimanenti. Come potrebbe la cellula riconoscere in modo specifico l’altro allele se la scelta è basata solo sulla casualità? Qualcosa non quadra, ed in questo modo la casualità che ha retto la teoria stocastica fino ad ora è stata, almeno parzialmente, distrutta in un soffio.
L’olfatto che guida l’assone durante il lungo cammino
 L’ultima domanda è ‘Cosa succede con il collegamento al cervello quando forziamo una cellula ORC ad esprimere un recettore specifico scelto da noi?’. Gli esperimenti mostrano che il collegamento cervello-recettore è perfetto, quindi ne consegue che il collegamento è basato solo sull’OR espresso.
L’ultima domanda è ‘Cosa succede con il collegamento al cervello quando forziamo una cellula ORC ad esprimere un recettore specifico scelto da noi?’. Gli esperimenti mostrano che il collegamento cervello-recettore è perfetto, quindi ne consegue che il collegamento è basato solo sull’OR espresso.
Ma quando questa scelta cambia all’improvviso?
Per rispondere a questa domanda un gruppo di ricercatori ha tentato di cambiare il recettore scelto dalla cellula poco prima che questa riesca ad ‘agganciarsi’ al cervello (maturare), attraverso un gene OR esogeno ed inducibile.
In questo topo transgenico le ORC scelgono un recettore endogeno in un modo apparentemente casuale, e cominciano la propagazione dell’assone verso il cervello cercando la zona giusta per formare sinapsi. Durante questa fase si può innescare l’espressione del recettore transgenico con il conseguentemente spegnimento del recettore endogeno…
La cellula ancora immatura, come abbiamo visto, si ‘adatta’ al nuovo recettore, ma si aggancerà anche alla zona cerebrale giusta? La risposta è incredibilmente sì. il collegamento e la funzione del recettore è perfetto nonostante il cambio recettoriale durante la formazione dell’assone. Tuttavia, se si cerca di cambiare la scelta dell’OR espresso dopo la maturazione della ORC, si provoca una abberrazione che innesca apoptosi.
Come è possibile che un OR possa guidare la scelta della regione cerebrale giusta a cui ‘agganciarsi’ senza avere altri 1.000 geni deputati al riconoscimento dei diversi OR da parte del cervello?
Qualcuno ha suggerito un’ipotesi alquanto affascinante, secondo cui un OR si trovi alla testa dell’assone durante la fase di elongazione, guidandolo verso il corretto punto di aggancio al cervello come farebbe un cane da tartufo a portarci verso questo prezioso tubero in un intero bosco.
Teoria affascinante e stravagante, tuttavia ancora insoluta ed in cerca di qualcuno che la convalidi o la controbatta con esperimenti, o con ipotesi più semplici.
Conclusione
In questo lungo post abbiamo messo sul piatto tutto quello che è noto sull’olfatto senza uscirne fuori con una teoria solida in grado di spiegare tutti i dati sperimentali. Per chi fa ricerca questo risultato è il pane quotidiano poiché non si seguono mai strade battute, si cerca sempre di crearne nuove, con nuove ipotesi, nuove verifiche e nuove deduzioni che porteranno ad altre ipotesi che si spera siano migliori delle precedenti e più vicine alla verità.
Tutt’ora ci sono gruppi di ricerca che analizzano le seguenze di DNA dei recettori OR cercando qualcosa in comune; analisti in cerca di modifiche epigenetiche in questi clusters genomici; cacciatori di nuovi meccanismi cellulari; esperti di transgeni che tentano nuove e più affascinanti teorie, a volte anche bizzarre… e poi ci sono ricercatori che provano a dare un senso a questo puzzle di dati disarmonici. Il tutto per svelare un mistero che dura da tanti anni oramai.
Non vi è dubbio che ci sono persone che provano un certo fascino nel partecipare a questa continua caccia alla soluzione del problema strato dopo strato, tirando fuori teorie sempre più complesse ed affascinanti, ed a volte come in questo caso si tirano fuori addirittura nuovi meccanismi che si ignoravano fino a poco tempo fa.
Un in bocca al lupo a chi si addentrerà nel risolvere questo mistero anche solo per 5 minuti ed un grazie a Nico e Patrizio per l’incoraggiamento ed i consigli che mi hanno dato per la stesura di questo post.
Tags:
Animali transgenici,
Apoptosi,
Biologia molecolare,
Cellule Recettoriali,
Cre/LoxP,
fattori trascrizionali,
mappa sensoriale,
Neuroni,
neuroni olfattivi,
Olfatto,
Percezione
9 febbraio 2009 - 9:19 pm
Ciao a tutti! Oggi vi parlerò di un articolo che non tratta strettamente le neuroscienze, ma che propone una tecnica che sicuramente potrà trovare interessanti risvolti in questo campo. Questo post è la traduzione (abbastanza fedele) di quello che ho scritto originariamente (in inglese) sull’ottimo blog ReporterGene.
Il
calcium imaging è una tecnica che è decisamente maturata negli ultimi tempi, e di anno in anno vengono generati indicatori per il
calcio codificati geneticamente sempre più evoluti.
Uno dei vantaggi dell’utilizzo di indicatori codificati geneticamente è quello di poterli utilizzare per l’imaging in vivo e quindi per studiare processi fisiologici (o patologici) in un sistema molto più completo (e complesso) di -per esempio- una coltura cellulare o una fettina di tessuto.
Diversi approcci sono stati utilizzati per ottenere imaging in vivo, alcuni dei quali fanno uso di una fibra ottica, o “fibroscopio”, inserita nella regione da analizzare e collegata ad un microscopio. Questo è ovviamente un metodo invasivo, e limita l’osservazione alla piccola zona d’azione della fibra. Un altro approccio meno invasivo è quello di utilizzare obiettivi a lunga distanza focale per ottenere immagini di una regione del corpo esposta: come già visto, questo metodo è stato usato, ad esempio, per analizzare la plasticità delle spine dendritiche nella corteccia cerebrale. Anche questa tecnica, tuttavia, permette la visione di una limitata area di interesse, oltre a richiedere un intervento chirurgico piuttosto delicato.
L’approccio recentemente descritto da Rogers e colleghi su PlOS One, invece, è completamente non invasivo. Hanno infatti generato una linea di topi transgenici che esprimono in maniera selettiva (tamite un approccio floxed-stop) una proteina sensibile al calcio, detta GFP-aequorina. Il reporter può essere espresso selettivamente nelle cellule di interesse semplicemente incrociando questi topi con topi che esprimono Cre in quelle cellule (molte di queste linee sono disponibili commercialmente). La GFP-aequorina è una proteina che consiste di una parte sensibile al calcio (aequorina) che in presenza di ioni Ca2+  può ossidare un substrato (chiamato coelenterazina), producendo luminescenza, la quale eccita l’altra metà della proteina (GFP, green fluorescent protein) che quindi fluoresce.
può ossidare un substrato (chiamato coelenterazina), producendo luminescenza, la quale eccita l’altra metà della proteina (GFP, green fluorescent protein) che quindi fluoresce.
L’idea è quindi quella di iniettare coelenterazina e misurare la fluorescenza generata da GFP.
Questo metodo permette di osservare variazioni di calcio nell’intero animale, anche se ovviamente ha una risoluzione spazio-temporale più bassa (ma comunque buona) rispetto agli altri metodi sopra menzionati.
E in effetti sembra che funzioni bene! Quando GFP-aequorin è stata espressa nei mitocondri delle cellule muscolari, infatti, ha permesso di misurare l’aumento di calcio durante la contrazione muscolare. Questo è stato testato sia dopo una contrazione introdotta artificialmente, sia in condizioni fisiologiche come l’attività muscolare spontanea di topi neonati (vedi figura), sia in situazioni “patologiche”, come le convulsioni evocate da kainato.
Per meglio vedere questo sistema in azione consiglio fortemente di guardare i video allegati all’articolo (che come tutti gli articoli di PLoS è ad accesso gratuito).
Riassumendo, questo approccio permette di misurare il calcio in modo non invasivo e su tutto l’animale in condizioni fisiologiche e patologiche. Questa tecnica potrebbe trovare interessanti applicazioni in studi che misurano lo stato metabolico di un certo tessuto, o l’apoptosi o uno dei moltissimi processi regolati dal calcio (la memoria ad esempio). Il passo successivo, ovviamente, sarebbe quello di ottenere questo tipo di registrazioni in un sistema in cui l’animale si può muovere liberamente. Se avete visitato il link qui a sinistra avrete capito che non siamo lontani dall’ottenerlo, ed infatti lo stesso gruppo ha già pubblicato un articolo a riguardo (Roncali et al., J. Biomed. Opt. 2008)!
Tags:
Animali transgenici,
Calcio,
Imaging,
In vivo
30 luglio 2008 - 5:54 pm
Molti dei nostri processi biologici sono regolati da ritmi regolari. Il nostro cuore batte circa 70 volte al minuto, molti ormoni vengono prodotti dal cervello ad intervalli regolari di 2-3 ore, e così via. Oltre a questi ritmi, spesso chiamati “ultradiani” (cioè che si ripetono più di una volta al giorno) esistono però dei ritmi “circadiani” cioè che si ripetono con cicli di un giorno, che regolano ad esempio il fatto che – normalmente – siamo attivi di giorno e dormiamo di notte. La luce gioca quindi un ruolo estremamente importante nel controllare queste funzioni.
Una delle aree che si ritengono essere più importanti per il controllo dei ritmi circadiani è il nucleo soprachiasmatico (SCN), una regione cerebrale che riceve afferenze anche dalla retina ed è quindi in grado di processare le informazioni sull’orario attuale (giorno/notte).
Oggi vi parlerò di un interessante studio pubblicato qualche anno fa su
Nature, nel quale si analizzava il ruolo di due geni importanti per il mantenimento di questi ritmi, chiamati cry1 e cry2.
La scoperta dei geni cry è già di per se molto interessante. Sono stati infatti scoperti come omologhi di geni che codificano per i criptocromi, pigmenti sensibili alla luce blu presenti in alcune piante e responsabili di processi quali la fioritura in determinati periodi dell’anno. Ma a cosa servono in un mammifero?
Lo studio di van der Horst e colleghi analizza il comportamento di topi knockout (KO) per questi geni, ossia topi a cui sono stati rimossi questi determinati geni. Quando confrontati con animali normali, infatti, i topi knockout per i geni cry presentano ovvie anomalie.

L’immagine qui sopra mostra l’attività di topi normali e KO per i geni cry. Le barrette nere indicano l’attività motoria dei topi, lo sfondo bianco indica luce e grigio indica buio. I topi normali (pannello a) sono animali notturni e come tali mostrano attività motoria di notte e non di giorno. L’attività motoria ha un periodo di circa 24 ore. Come si può notare dalla parte bassa del pannello a, anche mettendo i topi in condizioni di buio costante, il ritmo circadiano rimane inalterato.
I topi KO per cry1, (pannello b) invece, mostrano un periodo più breve (di 22.5 ore). Questo viene evidenziato solo quando vengono messi in condizioni di buio costante, mentre in presenza di cicli luce/buio normali (12h/12h) si comportano normalmente. Notare come la periodicità rimanga, ne viene solo alterata la lunghezza.
Opposta situazione avviene nei KO per cry2 (pannello c), che invece hanno un periodo più lungo (24.6 ore) e quindi in condizioni di buio completo sono sfasati pian piano “in avanti”. In presenza di singoli KO, tuttavia, una delle due proteine potrebbe compensare, almeno in parte per l’altra.
Quando vennero invece analizzati i doppi KO (che quindi mancano sia di cry1 che di cry2), si notarono due interessanti fenomeni. Innanzitutto i topi avevano ancora una marcata attività circadiana in condizioni di luce/buio (pannello f), indicando che altri sistemi, oltre a cry1/2 possono modulare questi processi. In oltre, in condizioni di buio totale, invece, si ottiene un’immediata perdita di questo ritmo, e l’attività motoria diventa irregolare. I pannelli d ed e, mostrano situazioni intermedie in cui viene mantenuta solo una copia di cry1 o di cry2.
Questi risultati, nel complesso, indicano che il corretto bilanciamento dell’attività di questi due geni è necessario per ottenere un corretto ritmo circadiano.
Infine, a conferma di quanto appena detto, si può osservare che quando si fa passare un topo normale (pannello a) tra due diversi regimi di luce/buio, si nota solo un lento adattamento dell’attività motoria al nuovo “pattern”. I KO per cry1/2, invece, mostrano un immediato cambiamento nell’attività (pannelli c e d).
Molta strada è stata fatta negli ultimi anni per comprendere questi fenomeni, ma c’è ancora molto da studiare e l’argomento è sicuramente affascinante.
Tags:
Animali transgenici,
Neuroscienze,
Ritmi circadiani
2 febbraio 2008 - 11:44 pm
 Negli ultimi 20 anni la biologia molecolare ha fatto passi da gigante. Siamo arrivati ad un punto in cui parlare di DNA è cosa normale, tanto che uno si può far sequenziare il genoma ad un prezzo relativamente abbordabile, ci si può costruire il proprio batterio personale e chiunque ha la propria opinione sugli OGM (anche se magari non sa cosa siano…).
Negli ultimi 20 anni la biologia molecolare ha fatto passi da gigante. Siamo arrivati ad un punto in cui parlare di DNA è cosa normale, tanto che uno si può far sequenziare il genoma ad un prezzo relativamente abbordabile, ci si può costruire il proprio batterio personale e chiunque ha la propria opinione sugli OGM (anche se magari non sa cosa siano…).
Anche le neuroscienze sono state colpite da questa ondata di novità, tanto che oramai è cosa assolutamente normale e quasi necessaria utilizzare animali transgenici per molti tipi di esperimenti.
C’è però un’area delle neuroscienze che forse non ha ricevuto questo grande successo di pubblico ed è l’imaging. L’imaging è un campo molto vasto, che non è solo ristretto alle neuroscienze e che comprende una serie di tecniche atte a visualizzare molti processi cellulari. Pur non essendo necessariamente ristretto alle neuroscienze, credo che negli ultimi anni molti dei maggiori progressi a riguardo siano stati fatti proprio in questo campo.
Penso che uno dei motivi per cui queste tecniche siano un po’ sconosciute a molti (o solo conosciute di nome) sia la difficoltà tecnica dei processi coinvolti. Molte di queste tecniche richiedono l’uso di un microscopio ma, mentre ci sono poche difficoltà a capire come funziona un microscopio tradizionale e magari uno a fluorescenza, quando si comincia a parlare di eccitazione a due fotoni, deflettori opto-acustici e amenità del genere generalmente si perde molto velocemente l’attenzione di chi non è del campo. Se è vero infatti che fare un esperimento di imaging non richiede generalmente particolari conoscenze tecniche, per riuscire ad ottimizzare ed usare al meglio queste tecniche è necessaria una conoscenza piuttosto ampia dei processi fisici sottostanti. Ebbene sì, la fisica quantistica è molto importante in questo caso ed è cosa piuttosto normale oramai trovare articoli di microscopia applicata alle neuroscienze che sembrano trattare di elettronica o fisica più che di biologia! Personalmente sono affascinato da tutte queste tecniche, e credo che nei prossimi anni con nuovi avanzamenti tecnologici si riusciranno a fare cose ancora più incredibili di quanto si riesca a fare ora.
Tanto per farvi un paio di esempi, è oggigiorno facilmente possibile usare l’imaging per misurare il livello di ioni (come calcio, cloro, magnesio e zinco) all’interno di una cellula, all’interno di singoli compartimenti della cellula o addirittura visualizzare l’apertura di un singolo canale ionico. E’ possibile “visualizzare” l’attività elettrica di un neurone senza usare elettrodi, usando particolari coloranti sensibili al voltaggio. E’ possibile visualizzare singole molecole e vedere come si muovono all’interno di una cellula. E’ inoltre possibile visualizzare la crescita e plasticità dei neuroni al passare del tempo, come dicevo in precedenza… e potrei andare avanti per pagine e pagine!
Tutte queste cose sono relativamente facili su sistemi in vitro (es. cellule in coltura), tuttavia è ora possibile applicarne alcune su animali anestetizzati o addirittura svegli, ed è quindi possibile osservare questi processi cellulari in funzione durante determinate attività.
Insomma le possibilità sono tantissime e veramente affascinanti, e credo che nei prossimi anni ci sarà veramente un boom di nuove tecniche in questo campo… dobbiamo solo aspettare e vedere!
Tags:
Animali transgenici,
Biologia molecolare,
Imaging,
Neuroscienze
 Commenti disabilitati
Commenti disabilitati
18 dicembre 2007 - 6:44 pm
Uno dei più grandi segreti nel campo delle neuroscienze è sicuramente il meccanismo della memoria.
Per un molti aspetti scientifici che riguardano la fisiologia o la fisiopatologia di cellule ed organi potremmo dire con orgoglio che negli ultimi anni si sono fatti dei progressi da giganti, anche se è lungo il cammino della strada che ci porterà verso la risoluzione di molte malattie come l’Alzheimer ed il Parkinson. Per intenderci, sono noti tanti possibili target farmacologici di queste neuropatologie, tuttavia la ricerca effettiva della “terapia” è ancora ai primi stadi. Nel campo della memoria invece aleggia un mistero irrisolto, ovvero quello che si sa è che non si è nemmeno prossimi a saperne qualcosa di più.
Le domande sono semplici: “In cosa consiste la memoria dell’uomo? Dove si conserva? È un senso fisico, elettrico oppure è un eco di un meccanismo che è continuamente in funzione?”. Quando si troverà una risposta vera ad una di queste domande potremmo definirci vicini ad una svolta epocale nel campo della psiche e più in generale nel campo delle neuroscienze.
Ovvio che se avessimo a disposizione tutti i farmaci che bloccano o attivano ogni singolo prodotto genico avremmo un tool strabiliante per capire il funzionamento del sistema nervoso centrale (SNC), la psiche e di conseguenza anche la memoria e le patologie ad essa correlate, ma questa è solo utopia. Un approccio più realistico come supporto per lo studio di questo strano meccanismo è la generazione di un topo transgenico per ciascuna proteina del genoma, specie di quelle coinvolte nel SNC, con il fine di studiarne gli effetti direttamente in vivo su tutti i processi fisiologici e patologici. Non si tratta di utopia, questo progetto è già in atto in tanti laboratori specializzati nel mondo; ovvio che ci vorrà del tempo come è stato per il sequenziamento del genoma umano.
E’ da dire che l’intervento dei topi transgenici nel campo delle neuroscienze ha portato ad enormi sviluppi nell’ambito dei meccanismi molecolari e soprattutto di tecniche sempre più complesse e specifiche che consentono persino di eliminare proteine importantissime per l’embriogenesi del topo in modo relativamente semplice ed efficace. Grazie a queste tecniche si è arrivati a capire che l’ippocampo è un’interfaccia per fissare ed interpretare i ricordi, anche se non è la sede dell’immagazzinamento.
A tal proposito ricordo che da bambino fui affascinato non poco da questo “mistero” della memoria, ma di seguito questo ricordo fu seppellito da anni di studi in altre cose fino a tornare di nuovo in auge in una gita a Pompei fuori dall’ordinario. Proprio questo ha risvegliato in me tanti ricordi, dubbi, perplessità e domande, tanto che vorrei dedicare il mio primo blog al racconto di due personaggi scientifici agli antipodi del globo e della personalità che stanno studiando alcuni di questi meccanismi della memoria.
Il primo personaggio vive in Korea, si chiama Hee-Sup Shin ed ultimamente ho avuto l’onore di conoscerlo personalmente in una gita di piacere a Pompei. Shin è professore in Scienze della Vita nell’università della repubblica Koreana, negli anni si è specializzato nella produzione di topi transgenici per il SNC ed in particolare si occupa soprattutto dei canali e trasportatori del calcio. Il nostro incontro è avvenuto in seguito ad un seminario che ha tenuto qui a Napoli e tra una chiacchierata e l’altra mi sono offerto di accompagnarlo in una gita a Pompei per fargli conoscere il nostro territorio e la nostra storia. Non ci è voluto molto per capire che Shin è sicuramente quello che si può definire una persona di poche parole, con aria spesso distratta e seria, vestito sempre elegante con un’economia di movimenti che ricorda gli antichi maestri di arti marziali, il contatto con lui infatti mi ha intimorito non poco. In una giornata ci sono state migliaia di cose raccontante ma un argomento è stato principe, riassumibile due frasi esemplari… “Prof. Shin, sono stato sempre affascinato dai misteri della memoria, ma non ci ho mai capito molto. Lei invece ci lavora da tempo ed ha fatto diverse pubblicazioni su questo argomento, che idea se n’è fatta? Di cosa si tratta e come funziona?”.
La sua risposta intelligente e telegrafica è stata “La memoria è quel meccanismo che ti consente di capire che non ho risposto alla tua domanda”. Ero troppo imbarazzato per insistere ma ho colto subito l’occasione per discutere di una sua scoperta che mi ha fatto pensare molto. L’articolo in questione è stato pubblicato addirittura su Neuron, una tra le più importanti riviste nel campo delle neuroscienze e che fa parte del gruppo di Cell.
Shin ha generato un topo transgenico che manca di una proteina che è espressa solo nel SNC, il fenotipo del topo transgenico è incredibile, il topo ha aumentato significativamente la capacità cognitiva e di memoria in alcuni semplici esperimenti. In effetti l’eliminazione di questo scambiatore sodio calcio 2 (NCX2) consentirebbe al topo una maggiore capacità di ricordare eventi ed esperienze e soprattutto di imparare da questi. Ho potuto vedere questi animali in azione rispetto ai propri fratelli wild-type congenici e l’effetto è praticamente visibile ad occhio nudo senza neanche mettere in mezzo la statistica. Un topo lasciato in acqua (Water maze) deve trovare una piattaforma di vetro a pelo d’acqua, praticamente impossibile da vedere. Con un minimo di accorgimento il topo può ricordare mediante dei simboli e le distanze dai bordi dove ha trovato la piattaforma nei giorni precedenti. Ebbene le performance dei topi normali migliorano di giorno in giorno anche se girano sempre un po’ nella piscina prima di trovare la piattaforma, ma se si guardano i topi KO imparano quasi subito come dirigersi direttamente verso la piattaforma e impiegano sempre meno secondi per trovarla, al confronto i loro fratelli WT sembrano stupidi.
La situazione non finisce qui, poiché dall’altra parte del mondo, in Canada, c’è stato uno studio praticamente identico ma con risultati completamente opposti. Il Prof Jonathan Lytton ha generato un topo transgenico fatto in maniera simile che manca di una proteina che scambia sodio e calcio con l’aggiunta del potassio (NCKX2). Le regioni di espressione di NCKX2 e le funzioni sono sovrapponibili alla proteina precedente NCX2. L’effetto? è drasticamente opposto. Il knock-out della proteina NCKX2 porta ad un peggioramento delle funzioni cognitive del topo rispetto ai suoi fratelli WT, anche se apparentemente sembrano indistinguibili. Come mai due proteine che fanno le stesse cose, con una topologia simile ed una espressione nelle stesse regioni cerebrali possono portare a dei risultati così discordanti?
Un fenomeno davvero paradossale che Shin taglia corto, “Non sappiamo ancora nulla di importante sulla memoria e sulle funzioni cognitive per capire quali siano i veri meccanismi che sottendono a questi processi, di certo non è il semplice accumulo di calcio o sodio nelle cellule che determina la memoria. La memoria è di certo un meccanismo molto più complesso”.
In effetti per la memoria si potrebbe parlare di circuiti elettrici completi di chips, resistenze ed interruttori. Ciascun neurone in sé non fa nulla, ma è l’intera rete che ha l’effetto, la modifica dell’espressione di una proteina potrebbe consentire dei sovraccarichi ionici in alcune cellule ed innescare dei corto circuiti in altre aree, bypass di emergenza per il ripristino ed il risultato può essere migliore o peggiore dello stato precedente. Ora noi guardiamo semplici sovraccarichi ionici a livello locale, ma si dovrebbe pensare sempre alle interconnessioni tra le varie aree del cervello che si stimolano e si disattivano a vicenda. Una semplice proteina può disturbare tale armonia e l’effetto che vediamo non è mai diretto, ma il risultato del ripristino di tale armonia.
“Prof. Shin, mi scusi ma allora che senso ha studiare i topi transgenici se poi l’interpretazione di tutti questi fenomeni è troppo complessa per capirla. Per intenderci, se Lei già sa che eliminando una proteina si causano centinaia di fenomeni per cui l’effetto finale non è determinato da una singola proteina ma dall’alterazione di centinaia di fenomeni a valle che sono difficili da prevedere e da comprendete, perché generare topi transgenici e non limitarsi ad analizzare le vie neuronali che sono alla base di tali fenomeni.”.
Shin mi guarda con un’aria sorridente e poi replica:
“Migliaia di persone hanno studiato per anni queste vie, descrivendole anche in maniera esaustiva, ma funzionalmente si può solo ipotizzare a cosa servano e cosa succederebbe se fossero alterate. Avere dei topi in cui queste vie sono già alterate può dare maggiori informazioni su quello che si è studiato e può dare dei riscontri in vivo importantissimi.”.
“Prof. Shin, secondo Lei quanto manca alla comprensione della memoria?”.
“Il primo mattone è dietro l’angolo, basta svoltare al punto giusto per poter iniziare a capire, poi sarà questione di anni e non più di secoli come ora. Le persone come me stanno cercando quest’angolo.”
Tags:
Animali transgenici,
Memoria,
Neuroscienze,
Water maze
20 novembre 2007 - 9:49 pm
Immaginate di voler capire come funziona un apparecchio elettronico:
lo aprite e ciò che vedete è un ammasso di cavi che vanno da ogni parte… una cosa che potreste fare per cominciare è disegnare una mappa dei fili, segnandovi da dove partono e dove arrivano. Certo, non sarebbe la soluzione finale al vostro problema, ma potrebbe essere un buon punto di partenza.
Studiando il cervello ci si trova spesso di fronte ad un problema simile, ma molto più complesso: un cervello umano contiene approssimativamente 100 miliardi di neuroni di molti diversi tipi e si stima che ciascuno di essi abbia collegamenti (sinapsi) in media con altri 7000 neuroni. Una delle sfide più grandi è quindi capire come questi neuroni siano collegati tra di loro, in modo da poter creare una mappa delle connessioni del cervello.
Un enorme passo avanti in questo senso è stato annunciato in un recente studio apparso sull’ultimo numero di Nature da parte di Jean Livet e colleghi al Dipartimento di Biologia Molecolare e Cellulare dell’Università di Harvard (e con uno studio del genere non c’è da sorprendersi che abbiano avuto l’immagine di copertina…).
 L’articolo riporta la generazione di varie linee di topi transgenici chiamati “Brainbow”, nome derivato dall’unione di brain (=cervello) e rainbow (=arcobaleno). I neuroni dei topi Brainbow, infatti, emettono fluorescenza in 100-150 colori differenti! Ciò è possibile grazie all’espressione nei neuroni di questi topi di diverse proteine fluorescenti: GFP (verde), YFP (gialla), CFP (azzurro), OFP (arancio) e RFP (rossa). Queste proteine vengono fatte esprimere in modo casuale ed a diversi livelli nei diversi neuroni per generare i diversi colori.
L’articolo riporta la generazione di varie linee di topi transgenici chiamati “Brainbow”, nome derivato dall’unione di brain (=cervello) e rainbow (=arcobaleno). I neuroni dei topi Brainbow, infatti, emettono fluorescenza in 100-150 colori differenti! Ciò è possibile grazie all’espressione nei neuroni di questi topi di diverse proteine fluorescenti: GFP (verde), YFP (gialla), CFP (azzurro), OFP (arancio) e RFP (rossa). Queste proteine vengono fatte esprimere in modo casuale ed a diversi livelli nei diversi neuroni per generare i diversi colori.
Topi ed altri animali le cui cellule esprimono proteine fluorescenti non sono certo una novità, negli ultimi 10-15 anni si è visto un aumento esponenziale del loro numero. La novità di questo studio è il fatto di avere un così grande numero di colori diversi che permette di seguire facilmente il percorso di un neurone, capire da dove parte e dove arriva e con quali altri neuroni viene a contatto. Sarà infatti probabile che neuroni vicini tra di loro abbiano diverso colore, rendendo così più “semplice” la mappatura delle varie connessioni.
L’articolo mostra anche esempi pratici d’uso di Brainbow come la ricostruzione in 3D di alcuni network cellulari nel cervelletto ed uno studio dell’interazione neuroni-glia.
Per chi fosse interessato all’aspetto più tecnico: il trucco sta nell’utilizzo di un transgene contenente le diverse XFP messe in sequenza in modo tale che solo la prima proteina possa essere tradotta. Le varie XFP sono messe all’interno di siti lox incompatibili tra loro (loxP, lox2272 e loxN) e mutualmente esclusivi; questo in pratica vuol dire che se Cre excide il DNA all’interno di una coppia di questi siti, gli altri non sono più funzionali. Il taglio può avvenire con la stessa probabilità a ciascun sito, portando così all’espressione di una diversa XFP in neuroni diversi. Aggiungete il fatto che diverse copie del transgene possono essere inserite in tandem (una delle linee riportate nell’articolo ha 8 copie del transgene) ed eccovi tutta la variabilità di espressione necessaria per ottenere 100 o più colori diversi!
Una domanda mi sorge però spontanea: supponendo di arrivare ad avere una mappa completa delle connessioni cerebrali, non credete ci troveremo poi in una situazione di stallo su come analizzare la inimmaginabilmente immensa quantità di dati che deriverebbe da questo studio? E come memorizzare questa enorme quantità di dati in un modo accessibile e funzionale?
Ad ogni modo, per ora la cosa migliore da fare è godersi un paio delle fantastiche immagini dei neuroni Brainbow!
E per chi volesse, ecco il link all’articolo (è necessaria una subscription a Nature per vedere il full-text):
Transgenic strategies for combinatorial expression of fluorescent proteins in the nervous system – Nature, 2007

Tags:
Animali transgenici,
Biologia molecolare,
Imaging,
Neuroscienze

 Prima di trarre conclusioni affrettate andiamo in laboratorio con la nostra ricostruzione della scena del crimine. Induciamo una ischemia cerebrale a dei ratti ed analizziamo nel tempo cosa fa la microglia nel SNC. Anche se non è facile seguire le cellule microgliali che girano nel cervello quando l’animale è vivo, è possibile ricostruire la scena mettendo insieme una serie di animali analizzati a tempi diversi dopo l’evento ischemico.
Prima di trarre conclusioni affrettate andiamo in laboratorio con la nostra ricostruzione della scena del crimine. Induciamo una ischemia cerebrale a dei ratti ed analizziamo nel tempo cosa fa la microglia nel SNC. Anche se non è facile seguire le cellule microgliali che girano nel cervello quando l’animale è vivo, è possibile ricostruire la scena mettendo insieme una serie di animali analizzati a tempi diversi dopo l’evento ischemico. L’accusa inizia l’arringa con delle frasi taglienti e tendenziose. Secondo la sua ricostruzione le cellule microgliali, avvezze all’eutanasia, si sono dirette verso la zona sofferente dall’ipossia. I dati pubblici ci hanno depistato sull’effettivo orario di arrivo sul luogo del delitto, in realtà, recenti scoperte ci indicano che le cellule microgliali si trovavano già in loco prima del tempo dichiarato. Non è stato possibile vederle poiché sono arrivate con un travestimento non noto fino a poco tempo fa. Poi una volta arrivate sul luogo prefissato hanno iniziato a contornare alcuni neuroni in sofferenza. La microglia, adese ai neuroni ha liberato delle sostanze in uno spazio estremamente piccolo, troppo scarse per essere analizzate e troppo rapide per essere viste. In questo istante forse c’é stato un ‘errore’, ed al posto di sostanze neurotrofiche la microglia ha lasciato delle sostanze tossiche. Magari ha valutato che i neuroni non ce l’avrebbero fatta a passare indenni l’ipossia e li ha avvelenati in maniera irreversibile per eutanasia. Poi mentre i neuroni avvelenati stavano resistendo all’ipossia, il colpo di grazia, la microglia si é allontanata aggravando la situazione per il mancato sostentamento trofico. Ciò che ne é conseguito é la morte dei neuroni in circostanze apparentemente solitarie. Poi sono arrivate le cellule microgliali travestite da spazzine ed hanno pulito il luogo del delitto.
L’accusa inizia l’arringa con delle frasi taglienti e tendenziose. Secondo la sua ricostruzione le cellule microgliali, avvezze all’eutanasia, si sono dirette verso la zona sofferente dall’ipossia. I dati pubblici ci hanno depistato sull’effettivo orario di arrivo sul luogo del delitto, in realtà, recenti scoperte ci indicano che le cellule microgliali si trovavano già in loco prima del tempo dichiarato. Non è stato possibile vederle poiché sono arrivate con un travestimento non noto fino a poco tempo fa. Poi una volta arrivate sul luogo prefissato hanno iniziato a contornare alcuni neuroni in sofferenza. La microglia, adese ai neuroni ha liberato delle sostanze in uno spazio estremamente piccolo, troppo scarse per essere analizzate e troppo rapide per essere viste. In questo istante forse c’é stato un ‘errore’, ed al posto di sostanze neurotrofiche la microglia ha lasciato delle sostanze tossiche. Magari ha valutato che i neuroni non ce l’avrebbero fatta a passare indenni l’ipossia e li ha avvelenati in maniera irreversibile per eutanasia. Poi mentre i neuroni avvelenati stavano resistendo all’ipossia, il colpo di grazia, la microglia si é allontanata aggravando la situazione per il mancato sostentamento trofico. Ciò che ne é conseguito é la morte dei neuroni in circostanze apparentemente solitarie. Poi sono arrivate le cellule microgliali travestite da spazzine ed hanno pulito il luogo del delitto. La difesa risponde punto per punto con calma e freddezza.
La difesa risponde punto per punto con calma e freddezza. Se questo fosse un giallo non potrebbe mancare il classico colpo di scena. Questa volta arriva proprio da Mario Capecchi che scopre, in una sua recente pubblicazione su cell, che l’inattivazione della microglia provoca un fenotipo ossessivo-convulsivo. Quello che sorprende é che l’iniezione nel midollo osseo di cellule microgliali marcate e fluorescenti provoca la comparsa di cellule microgliali nel cervello. Ancora una volta la microglia ha mentito, e a quanto pare ha un passaggio segreto per oltrepassare la BEE, anche se oggi non é stato ancora possibile scoprire come. A quanto pare la microglia ha molti aspetti ancora oscuri, forse anche delle identità e dei passaporti che non conosciamo ancora.
Se questo fosse un giallo non potrebbe mancare il classico colpo di scena. Questa volta arriva proprio da Mario Capecchi che scopre, in una sua recente pubblicazione su cell, che l’inattivazione della microglia provoca un fenotipo ossessivo-convulsivo. Quello che sorprende é che l’iniezione nel midollo osseo di cellule microgliali marcate e fluorescenti provoca la comparsa di cellule microgliali nel cervello. Ancora una volta la microglia ha mentito, e a quanto pare ha un passaggio segreto per oltrepassare la BEE, anche se oggi non é stato ancora possibile scoprire come. A quanto pare la microglia ha molti aspetti ancora oscuri, forse anche delle identità e dei passaporti che non conosciamo ancora. Mettere insieme tutti questi dati sparsi non é semplice. Nella ricerca, infatti, é difficile soprattutto distinguere la verità obiettiva dalle interpretazioni, ed in questo lungo processo sono state fatte solo delle allusioni, niente di più. L’articolo di Capecchi parla di una interferenza sui recettori nocicettivi periferici da parte della microglia. Un topo con difficoltà nella percezione del dolore ha dei comportamenti anomali, ma non c’é niente di significativamente neurologico.
Mettere insieme tutti questi dati sparsi non é semplice. Nella ricerca, infatti, é difficile soprattutto distinguere la verità obiettiva dalle interpretazioni, ed in questo lungo processo sono state fatte solo delle allusioni, niente di più. L’articolo di Capecchi parla di una interferenza sui recettori nocicettivi periferici da parte della microglia. Un topo con difficoltà nella percezione del dolore ha dei comportamenti anomali, ma non c’é niente di significativamente neurologico.


 Come abbiamo visto nel precedente post, il nostro ispettore cellulare è stato improvvisamente freddato dallo scagionamento del primo imputato eccellente. La teoria iniziale non faceva una grinza e c’erano anche molti indizi pesanti contro l’accusato. Purtroppo con il tempo e con l’uso di sostanze sempre più specifiche per il blocco del fattore transcrizionale la teoria della difesa ha avuto sempre più supporto. HIF-1 non è sicuramente una proteina da mettere tra i cattivi per l’
Come abbiamo visto nel precedente post, il nostro ispettore cellulare è stato improvvisamente freddato dallo scagionamento del primo imputato eccellente. La teoria iniziale non faceva una grinza e c’erano anche molti indizi pesanti contro l’accusato. Purtroppo con il tempo e con l’uso di sostanze sempre più specifiche per il blocco del fattore transcrizionale la teoria della difesa ha avuto sempre più supporto. HIF-1 non è sicuramente una proteina da mettere tra i cattivi per l’ Pensare all’ipossia come innesco di un meccanismo che porterà a morte inevitabile per i
Pensare all’ipossia come innesco di un meccanismo che porterà a morte inevitabile per i  Se fate questa domanda ad un qualsiasi esperto nel settore vi dirà che ci sono migliaia di proteine che fanno ‘ordine’ tra i diversi ioni, e sono divise in famiglie, superfamiglie e classi. Questi meccanismi possono dividersi grossolanamente in pompe e trasportatori, in base al fatto che usano direttamente, o no, l’ATP.
Se fate questa domanda ad un qualsiasi esperto nel settore vi dirà che ci sono migliaia di proteine che fanno ‘ordine’ tra i diversi ioni, e sono divise in famiglie, superfamiglie e classi. Questi meccanismi possono dividersi grossolanamente in pompe e trasportatori, in base al fatto che usano direttamente, o no, l’ATP. A questa domanda c’è una risposta più o meno ovvia. Poco prima dell’ischemia funzionava tutto come al solito, nulla lasciava presagire il disastro, e tutte le proteine risiedevano al loro nomale posto fino a che è mancata l’energia necessaria per il trasporto attivo degli ioni. Quando è iniziata a mancare l’energia l’efficienza del trasporto ionico si è ridotta mentre il disordine ionico dei
A questa domanda c’è una risposta più o meno ovvia. Poco prima dell’ischemia funzionava tutto come al solito, nulla lasciava presagire il disastro, e tutte le proteine risiedevano al loro nomale posto fino a che è mancata l’energia necessaria per il trasporto attivo degli ioni. Quando è iniziata a mancare l’energia l’efficienza del trasporto ionico si è ridotta mentre il disordine ionico dei  A questo punto del racconto io mi recherei sul luogo del delitto alla ricerca di qualche indizio e soprattutto di qualche risposta.
A questo punto del racconto io mi recherei sul luogo del delitto alla ricerca di qualche indizio e soprattutto di qualche risposta. Ritornando in ufficio c’è una cosa che non quadra… questo trasportatore passivo dove ha trovato tutta questa energia per espellere una quantità di
Ritornando in ufficio c’è una cosa che non quadra… questo trasportatore passivo dove ha trovato tutta questa energia per espellere una quantità di  Uhmm… Forse calunnie, leggendo bene qua e là i farmaci utilizzati per inibire NCX non sono molto specifici, agiscono anche su altri canali; magari NCX è stato coinvolto in qualcosa di più grande ed è stato usato come capro espiatorio. Improbabile che una proteina così letale possa essere conservata per milioni di anni durante l’evoluzione se non migliori sensibilmente il fitness dell’organismo.
Uhmm… Forse calunnie, leggendo bene qua e là i farmaci utilizzati per inibire NCX non sono molto specifici, agiscono anche su altri canali; magari NCX è stato coinvolto in qualcosa di più grande ed è stato usato come capro espiatorio. Improbabile che una proteina così letale possa essere conservata per milioni di anni durante l’evoluzione se non migliori sensibilmente il fitness dell’organismo. Le cose, da allora, non sono andate molto avanti, le pubblicazioni si sono rincorse tra di loro in un misto di ripetizioni e staccate con farmaci sempre più specifici e potenti. A questi articoli facevano seguito altri che descrivevano dell’effetto di queste sostanze sulla circolazione, ipertensione, inibizione di canali del
Le cose, da allora, non sono andate molto avanti, le pubblicazioni si sono rincorse tra di loro in un misto di ripetizioni e staccate con farmaci sempre più specifici e potenti. A questi articoli facevano seguito altri che descrivevano dell’effetto di queste sostanze sulla circolazione, ipertensione, inibizione di canali del  Analisi su analisi in diverse salse hanno dimostrato che questa proteina è fondamentale per alcuni meccanismi cardiaci e non solo, ma sicuramente esalta anche il danno ischemico al miocardio. E’ una circostanza difficile da spiegare in termini evoluzionistici e non è possibile capirne a fondo il meccanismo esatto.
Analisi su analisi in diverse salse hanno dimostrato che questa proteina è fondamentale per alcuni meccanismi cardiaci e non solo, ma sicuramente esalta anche il danno ischemico al miocardio. E’ una circostanza difficile da spiegare in termini evoluzionistici e non è possibile capirne a fondo il meccanismo esatto. 
 Come penso molti di voi possono intuire, esiste un numero inimmaginabile di odori, e la maggioranza di questi è causato da un mix di ‘odori primari’ in diversi rapporti, ma a complicare la situazione c’è che una molecola odorosa può agire su decine di recettori diversi con diversa specificità. I OR dei composti aminici, ad esempio, riconoscono solamente l’azoto primario, secondario o terziario con diversa efficacia, per cui gli odori di questi composti non possono essere discriminati con facilità e sembrano tutti molto simili. C’è da dire però che nonostante questa piccola sovrapposizione di segnali si possono discriminare con elevata sensibilità circa 10.000 odori diversi.
Come penso molti di voi possono intuire, esiste un numero inimmaginabile di odori, e la maggioranza di questi è causato da un mix di ‘odori primari’ in diversi rapporti, ma a complicare la situazione c’è che una molecola odorosa può agire su decine di recettori diversi con diversa specificità. I OR dei composti aminici, ad esempio, riconoscono solamente l’azoto primario, secondario o terziario con diversa efficacia, per cui gli odori di questi composti non possono essere discriminati con facilità e sembrano tutti molto simili. C’è da dire però che nonostante questa piccola sovrapposizione di segnali si possono discriminare con elevata sensibilità circa 10.000 odori diversi. Nel mondo animale, il non saper distinguere l’odore di una preda dall’odore del proprio predatore fa la differenza tra fare una buona colazione ed essere la colazione di qualcun altro. Anche riconoscere l’odore delle cose che si possono mangiare da quelle che è meglio evitare è fondamentale per la sopravvivenza, quindi i mammiferi durante l’evoluzione hanno accumulato più di 1.000 geni che sovraintendono il più misterioso dei 5 sensi. In pratica più del 3% del genoma dei mammiferi è deputato alla
Nel mondo animale, il non saper distinguere l’odore di una preda dall’odore del proprio predatore fa la differenza tra fare una buona colazione ed essere la colazione di qualcun altro. Anche riconoscere l’odore delle cose che si possono mangiare da quelle che è meglio evitare è fondamentale per la sopravvivenza, quindi i mammiferi durante l’evoluzione hanno accumulato più di 1.000 geni che sovraintendono il più misterioso dei 5 sensi. In pratica più del 3% del genoma dei mammiferi è deputato alla  Sapere quanti tipi di recettori sono presenti per cellula è fondamentale per capire quante aree ci dovremmo aspettare di trovare e per verificarlo potremmo ricorrere a tecniche avanzatissime di in situ hybridization, e di retrotrascrizione ed amplificazione per PCR su singola cellula. Ovviamente non sono tecniche facili e nemmeno tanto diffuse, ma gli esperti sono riusciti a dimostrare con questi esperimenti che ogni ORC esprime solamente un singolo OR.
Sapere quanti tipi di recettori sono presenti per cellula è fondamentale per capire quante aree ci dovremmo aspettare di trovare e per verificarlo potremmo ricorrere a tecniche avanzatissime di in situ hybridization, e di retrotrascrizione ed amplificazione per PCR su singola cellula. Ovviamente non sono tecniche facili e nemmeno tanto diffuse, ma gli esperti sono riusciti a dimostrare con questi esperimenti che ogni ORC esprime solamente un singolo OR. Secondo questa teoria la combinazione casuale o pseudocasuale di fattori trascrizionali per esprimere un singolo OR non può essere disturbata dalla coespressione di un OR transgenico scelto da noi. Per verificare questa teoria ‘deterministica‘, quindi, possiamo generare un topo transgenico in cui alcune ORC esprimono in maniera forzata un determinato OR scelto da noi e valutare se c’è coespressione.
Secondo questa teoria la combinazione casuale o pseudocasuale di fattori trascrizionali per esprimere un singolo OR non può essere disturbata dalla coespressione di un OR transgenico scelto da noi. Per verificare questa teoria ‘deterministica‘, quindi, possiamo generare un topo transgenico in cui alcune ORC esprimono in maniera forzata un determinato OR scelto da noi e valutare se c’è coespressione. Un’altra teoria che si è fatta strada nel tempo è basata sulla casualità della scelta del OR espresso (teoria stocastica). Per capirci immaginiamo un fattore trascrizionale unico che sia in grado di legare il promotore di tutti i geni dei OR e di consentirne l’espressione; tecnicamente può legarsi ad un solo OR e quindi può esprimere solo quello. Se il fattore trascrizionale non è molto efficiente nell’esprimere un OR si potrebbe spiegare come mai una ORC cambia OR nei primi stadi pur seguendo sempre la regola di esprimere un solo OR alla volta. In seguito, quando un OR espresso dà un forte segnale di funzione (feed-back) il fattore trascrizionale si fissa sul gene che sta trascrivendo fino allo stadio di maturazione.
Un’altra teoria che si è fatta strada nel tempo è basata sulla casualità della scelta del OR espresso (teoria stocastica). Per capirci immaginiamo un fattore trascrizionale unico che sia in grado di legare il promotore di tutti i geni dei OR e di consentirne l’espressione; tecnicamente può legarsi ad un solo OR e quindi può esprimere solo quello. Se il fattore trascrizionale non è molto efficiente nell’esprimere un OR si potrebbe spiegare come mai una ORC cambia OR nei primi stadi pur seguendo sempre la regola di esprimere un solo OR alla volta. In seguito, quando un OR espresso dà un forte segnale di funzione (feed-back) il fattore trascrizionale si fissa sul gene che sta trascrivendo fino allo stadio di maturazione. Se ci pensate, esiste un meccanismo di scelta molto simile che avviene nei linfociti. Queste cellule, però, non decidono l’anticorpo da esprimere in base a fattori trascrizionali, ma attraverso una ricombinazione genetica guidata. Si tratta di una piccola deviazione della teoria stocastica ed è anche risolutiva.
Se ci pensate, esiste un meccanismo di scelta molto simile che avviene nei linfociti. Queste cellule, però, non decidono l’anticorpo da esprimere in base a fattori trascrizionali, ma attraverso una ricombinazione genetica guidata. Si tratta di una piccola deviazione della teoria stocastica ed è anche risolutiva.
 Certamente la ricombinazione è da scartare ma fino ad ora niente ha smentito la casualità della scelta del OR. Tuttavia un gruppo di ricerca ha recentemente messo in discussione anche questa ipotesi granitica.
Certamente la ricombinazione è da scartare ma fino ad ora niente ha smentito la casualità della scelta del OR. Tuttavia un gruppo di ricerca ha recentemente messo in discussione anche questa ipotesi granitica. L’ultima domanda è ‘Cosa succede con il collegamento al cervello quando forziamo una cellula ORC ad esprimere un recettore specifico scelto da noi?’. Gli esperimenti mostrano che il collegamento cervello-recettore è perfetto, quindi ne consegue che il collegamento è basato solo sull’OR espresso.
L’ultima domanda è ‘Cosa succede con il collegamento al cervello quando forziamo una cellula ORC ad esprimere un recettore specifico scelto da noi?’. Gli esperimenti mostrano che il collegamento cervello-recettore è perfetto, quindi ne consegue che il collegamento è basato solo sull’OR espresso.


 Negli ultimi 20 anni la
Negli ultimi 20 anni la  L’articolo riporta la generazione di varie linee di topi transgenici chiamati “Brainbow”, nome derivato dall’unione di brain (=cervello) e rainbow (=arcobaleno). I
L’articolo riporta la generazione di varie linee di topi transgenici chiamati “Brainbow”, nome derivato dall’unione di brain (=cervello) e rainbow (=arcobaleno). I 