31 maggio 2010 - 10:29 am
Gli 007 del Sistema Nervoso Centrale
Preambolo
Eccoci di nuovo con il seguito del nostro giallo misterioso, ed iniziamo subito con un breve riassunto.
Siamo nei panni di un improbabile investigatore molecolare che deve scoprire chi ha causato la morte dei neuroni in seguito ad ictus. Nelle prime puntate abbiamo appreso la complessità dell’evento ischemico, ciò che ne consegue, e la volontà preprogrammata di qualcuno di assassinare i neuroni. Nella puntata precedente, invece, abbiamo introdotto le cellule microgliali che rappresentano delle guardie giurate dedicate alla protezione del cervello. Oggi vedremo come queste cellule siano più simili a degli agenti segreti.
L’interrogatorio
Per istituire un processo contro qualcuno é necessario avere delle prove convincenti; i sospetti da soli non bastano.
Ecco i fatti:
- Il cervello si trova in una condizione isolata, prima, durante e dopo il neuroomicidio;
- C’è sicuramente un colpevole e deve necessariamente essere contenuto all’interno del cervello;
- In questa ‘stanza’ troviamo permanentemente i neuroni (le principali vittime), la glia (vittime collaterali), e la microglia (guardie giurate);
- La microglia, il terzo incomodo, sopravvive al danno e si allontana dai neuroni poco prima che muoiano;
- La microglia in opportune condizioni riesce ad uccidere le cellule patogene ed anche i neuroni in agonia;
- La microglia non ha ancora un alibi per l’evento ischemico.
Continuiamo quindi l’interrogatorio nei confronti della microglia.

“…in altre parole i neuroni sono morti poco dopo la sua visita?”
“Sì, ma ero già lontano quando questo è successo”
“Può spiegarci perché Lei si è allontanato dal danno neuronale salvandosi la pelle, invece che combattere fino all’ultimo respiro? Dopotutto questo è il Suo ruolo, Lei è una guardia giurata e non può allontanarsi quando le cose vanno male”
“In realtà c’era ben poco da fare quando sono arrivato sul luogo del delitto, i neuroni stavano già morendo, non ho potuto far nulla ed era inutile sacrificarsi. Noi cellule microgliali non abbiamo alcuna possibilità di rinforzo da parte di progenitori esterni alla BEE, quindi sacrificarsi durante l’ischemia avrebbe comportato una perdita di cellule con una conseguente perdita di protezione per gli altri neuroni ancora vivi.”
“…uhmm… se ho capito bene, Lei è arrivato in ritardo, non ha fatto nulla e si è allontanato quando le cose si sono messe male. Perchè?”
“Sono preparato per affrontare cellule patogene, infezioni, infiammazioni ed eventi simili. L’evoluzione non mi ha selezionato per affrontare l’assenza di ossigeno e nutrienti.”
“…e cosa ha fatto in quei brevi momenti in cui Lei era a contatto con tanti neuroni poco prima che morissero?”
“Ho liberato dei fattori trofici per sostenere i neuroni e la glia. Generalmente i neuroni sono meno sensibili alla morte quando ricevono degli ormoni. Il mio ruolo era quello di incoraggiarli a vivere fino a quando fosse possibile”
Sembra non esserci nulla di serio, ma il dubbio rimane; ad esempio come mai una cellula tanto efficiente nel riconoscere i danni neuronali si è accorta del danno in corso così tanto in ritardo e non abbia potuto far nulla? La morte neuronale sembra avvenire poco dopo la scomparsa della microglia, può essere tutto questo un caso?
La ricostruzione del delitto
 Prima di trarre conclusioni affrettate andiamo in laboratorio con la nostra ricostruzione della scena del crimine. Induciamo una ischemia cerebrale a dei ratti ed analizziamo nel tempo cosa fa la microglia nel SNC. Anche se non è facile seguire le cellule microgliali che girano nel cervello quando l’animale è vivo, è possibile ricostruire la scena mettendo insieme una serie di animali analizzati a tempi diversi dopo l’evento ischemico.
Prima di trarre conclusioni affrettate andiamo in laboratorio con la nostra ricostruzione della scena del crimine. Induciamo una ischemia cerebrale a dei ratti ed analizziamo nel tempo cosa fa la microglia nel SNC. Anche se non è facile seguire le cellule microgliali che girano nel cervello quando l’animale è vivo, è possibile ricostruire la scena mettendo insieme una serie di animali analizzati a tempi diversi dopo l’evento ischemico.
Qui la prima sorpresa. Nel SNC tutte le cellule neuronali e astrocitarie sono pressoché fisse, magari con una mobilità molto limitata e lenta, mentre le cellule microgliali si muovono ad una velocità impressionante. Quello che colpisce molto è la capacità di attraversare reti di assoni, di dendrociti, cellule neuronali ed astrocitarie senza causare danno e senza avere punti di appiglio.
La seconda sorpresa è ancora più scioccante, la forma, le dimensioni e le caratteristiche di queste cellule è enormemente vasta, difficile riconoscerle anche per un occhio esperto. Si possono definire almeno 7 fenotipi principali di microglia: ameboide, ramificata, attiva e non fagocitica, attiva e fagocitica, cellule del composto granulare, perivascolare e juxatavascolare.
Neanche uno 007 potrebbe possedere altrettante identità. Per seguirle, quindi, possiamo usare dei markers, generici come Iba-1 o RCA-1 per riconoscere un po’ tutte le identità microgliali, oppure selettivi come ED1 per riconoscere solo le cellule microgliali attivate. Vi renderete subito conto della complessità di tale analisi, poiché nessun marker fino ad ora scoperto è effettivamente in grado di riconoscere tutte le identità microgliali in maniera specifica e selettiva. Insomma queste cellule sono qualcosa di sfuggente come potrebbe essere un agente segreto.
Ad aggiungere ulteriori sospetti c’è il fatto che le cellule microgliali si avvicinano ai neuroni con una certa identità e se ne allontanano con un’altra. Se poi pensiamo di fare una perquisizione e cercare cosa trasportano le cellule microgliali nelle vescicole potremmo ritrovare una serie infinita di endosomi, lisosomi, autosomi, e vescicole che contengono sostanze altamente tossiche, materiali infiammabili insieme a sostanze neurotrofiche etc etc. Di certo non è quello che si ritroverebbe in una borsa di un medico o infermiere.
Il Processo: L’accusa
 L’accusa inizia l’arringa con delle frasi taglienti e tendenziose. Secondo la sua ricostruzione le cellule microgliali, avvezze all’eutanasia, si sono dirette verso la zona sofferente dall’ipossia. I dati pubblici ci hanno depistato sull’effettivo orario di arrivo sul luogo del delitto, in realtà, recenti scoperte ci indicano che le cellule microgliali si trovavano già in loco prima del tempo dichiarato. Non è stato possibile vederle poiché sono arrivate con un travestimento non noto fino a poco tempo fa. Poi una volta arrivate sul luogo prefissato hanno iniziato a contornare alcuni neuroni in sofferenza. La microglia, adese ai neuroni ha liberato delle sostanze in uno spazio estremamente piccolo, troppo scarse per essere analizzate e troppo rapide per essere viste. In questo istante forse c’é stato un ‘errore’, ed al posto di sostanze neurotrofiche la microglia ha lasciato delle sostanze tossiche. Magari ha valutato che i neuroni non ce l’avrebbero fatta a passare indenni l’ipossia e li ha avvelenati in maniera irreversibile per eutanasia. Poi mentre i neuroni avvelenati stavano resistendo all’ipossia, il colpo di grazia, la microglia si é allontanata aggravando la situazione per il mancato sostentamento trofico. Ciò che ne é conseguito é la morte dei neuroni in circostanze apparentemente solitarie. Poi sono arrivate le cellule microgliali travestite da spazzine ed hanno pulito il luogo del delitto.
L’accusa inizia l’arringa con delle frasi taglienti e tendenziose. Secondo la sua ricostruzione le cellule microgliali, avvezze all’eutanasia, si sono dirette verso la zona sofferente dall’ipossia. I dati pubblici ci hanno depistato sull’effettivo orario di arrivo sul luogo del delitto, in realtà, recenti scoperte ci indicano che le cellule microgliali si trovavano già in loco prima del tempo dichiarato. Non è stato possibile vederle poiché sono arrivate con un travestimento non noto fino a poco tempo fa. Poi una volta arrivate sul luogo prefissato hanno iniziato a contornare alcuni neuroni in sofferenza. La microglia, adese ai neuroni ha liberato delle sostanze in uno spazio estremamente piccolo, troppo scarse per essere analizzate e troppo rapide per essere viste. In questo istante forse c’é stato un ‘errore’, ed al posto di sostanze neurotrofiche la microglia ha lasciato delle sostanze tossiche. Magari ha valutato che i neuroni non ce l’avrebbero fatta a passare indenni l’ipossia e li ha avvelenati in maniera irreversibile per eutanasia. Poi mentre i neuroni avvelenati stavano resistendo all’ipossia, il colpo di grazia, la microglia si é allontanata aggravando la situazione per il mancato sostentamento trofico. Ciò che ne é conseguito é la morte dei neuroni in circostanze apparentemente solitarie. Poi sono arrivate le cellule microgliali travestite da spazzine ed hanno pulito il luogo del delitto.
L’accusa continua rimarcando più volte il passato della microglia, come una cellula già avvezza al neuroomicidio (precedenti penali), inoltre ha mentito sull’orario di arrivo (depistaggi), si trovava vicino ai neuroni durante i fatti (opportunità), aveva dentro di sé l’arma del delitto (capacità), poteva girovagare indisturbato per il cervello con una discreta velocità (possibilità), si è allontanata con un travestimento prima che i neuroni si riprendessero causandone la morte (mancato soccorso). Ed in fine, l’arringa termina con una frase lapidaria: come nei più classici e proverbiali gialli, l’assassino è ritornato sul luogo del delitto ed ha rimosso le prove per fagocitosi (occultamento delle prove).
Non si tratta di un evento accidentale, ma di un pluriomicidio aggravato e premeditato di neuroni ed astrociti da parte di ‘servizi segreti deviati’ appartenenti al SNC.
La parola alla difesa
 La difesa risponde punto per punto con calma e freddezza.
La difesa risponde punto per punto con calma e freddezza.
Le multi identità sono parte del lavoro fisiologico della microglia. Queste cellule, infatti, in mancanza di collaboratrici, (es macrofagi, cellule presentanti l’antigene, cellule B etc,) devono necessariamente fare tutto da sole adattandosi di volta in volta alle nuove necessità. Sull’orario non c’é stata alcuna dichiarazione falsa, ogni cellula della microglia esprime o meno degli antigeni in funzione del lavoro che sta facendo, se non esistono ancora metodi per marcarli tutte ciò non indica alcuna colpevolezza.
Sulla questione delle sostanze tossiche e letali, é ovvio che una guardia giurata abbia sempre con sé la pistola ed il caricatore sempre pronti, tuttavia può anche avere con sé i materiali di primo soccorso. Fino ad ora non ci sono prove che la microglia abbia liberato sostanze tossiche verso i neuroni in quei momenti.
Anzi, l’imputato si è dimostrato utile per rimuovere le sostanze potenzialmente tossiche, ovvero quei residui post-ischemici che aumentano l’infiammazione e la sofferenza neuronale. Inoltre la microglia ha creato anche un ambiente idoneo per la formazione di nuove sinapsi per la ripresa post-danno.
La difesa poi ricorda che i topi transgenici che non hanno la microglia non sopravvivono all’embriogenesi, per cui stiamo trattando di cellule essenziali per la vita stessa. Poi cita gli innumerevoli casi in cui la microglia ha svolto ruoli eroici in difesa dei nostri delicati neuroni. Tutto questo non può essere cancellato da qualche sospetto e soprattutto da condizioni alle quali la microglia stessa non era preparata.
Se questo fosse un giallo…
 Se questo fosse un giallo non potrebbe mancare il classico colpo di scena. Questa volta arriva proprio da Mario Capecchi che scopre, in una sua recente pubblicazione su cell, che l’inattivazione della microglia provoca un fenotipo ossessivo-convulsivo. Quello che sorprende é che l’iniezione nel midollo osseo di cellule microgliali marcate e fluorescenti provoca la comparsa di cellule microgliali nel cervello. Ancora una volta la microglia ha mentito, e a quanto pare ha un passaggio segreto per oltrepassare la BEE, anche se oggi non é stato ancora possibile scoprire come. A quanto pare la microglia ha molti aspetti ancora oscuri, forse anche delle identità e dei passaporti che non conosciamo ancora.
Se questo fosse un giallo non potrebbe mancare il classico colpo di scena. Questa volta arriva proprio da Mario Capecchi che scopre, in una sua recente pubblicazione su cell, che l’inattivazione della microglia provoca un fenotipo ossessivo-convulsivo. Quello che sorprende é che l’iniezione nel midollo osseo di cellule microgliali marcate e fluorescenti provoca la comparsa di cellule microgliali nel cervello. Ancora una volta la microglia ha mentito, e a quanto pare ha un passaggio segreto per oltrepassare la BEE, anche se oggi non é stato ancora possibile scoprire come. A quanto pare la microglia ha molti aspetti ancora oscuri, forse anche delle identità e dei passaporti che non conosciamo ancora.
Inoltre come può l’iniezione midollare di una microglia inattiva causare un fenotipo psichiatrico? Siamo di fronte ad un personaggio davvero interessante.
Il giudizio
 Mettere insieme tutti questi dati sparsi non é semplice. Nella ricerca, infatti, é difficile soprattutto distinguere la verità obiettiva dalle interpretazioni, ed in questo lungo processo sono state fatte solo delle allusioni, niente di più. L’articolo di Capecchi parla di una interferenza sui recettori nocicettivi periferici da parte della microglia. Un topo con difficoltà nella percezione del dolore ha dei comportamenti anomali, ma non c’é niente di significativamente neurologico.
Mettere insieme tutti questi dati sparsi non é semplice. Nella ricerca, infatti, é difficile soprattutto distinguere la verità obiettiva dalle interpretazioni, ed in questo lungo processo sono state fatte solo delle allusioni, niente di più. L’articolo di Capecchi parla di una interferenza sui recettori nocicettivi periferici da parte della microglia. Un topo con difficoltà nella percezione del dolore ha dei comportamenti anomali, ma non c’é niente di significativamente neurologico.
La corte, quindi propone una nuova perizia. Verifichiamo cosa avviene in un topo transgenico capace di inattivare la funzione microgliale in maniera condizionata.
Il risultato é sconcertante, l’inattivazione condizionale della microglia, poco prima e durante l’ictus, provoca un notevole peggioramento del danno ischemico ed una sopravvivenza neuronale ridotta. Ovviamente ci sono state anche le critiche su quale gene é stato scelto per disattivare la microglia. Forse é stato scelto quel gene che sovraintende le funzioni microgliali ‘buone’. Si vedrà.
Tratta la somma, l’imputato é assolto per insufficienza di prove.
Conclusioni
Purtroppo, siamo ancora lontani dalla verità. Le indagini sulla microglia sono tutt’altro che concluse, si tratta di un campo in rapida espansione ed é sotto indagine per tantissime patologie come l’HIV, la sclerosi multipla, l’Alzheimer e tante altre patologie neurodegenerative.
Per ora il processo sull’ischemia é fermo per insufficienza di prove, ma qualcuno nel mondo sta ancora tentando di incastrare la microglia, chissà se ci sarà nuovamente qualche altro colpo di scena che la riporterà nuovamente sotto processo.
La ricerca, come al solito, non ha mai fine.
Alla prossima
Tags:
Animali transgenici,
Glia,
Ictus,
Ischemia Cerebrale,
microglia,
Neuroni
28 aprile 2010 - 2:08 pm
Dieci piccoli indiani
Preambolo
Nella puntata precedente abbiamo visto un esempio di un delitto mirato ad uno dei punti cardini delle difese cellulari. I fatti ci dimostrano sempre più che la morte neuronale in seguito ad ischemia non sia un evento incidentale, ma voluto da qualcuno con le idee ben chiare su quali difese eliminare e chi distruggere secondo uno schema prestabilito.
Dieci piccoli indiani
 Per chi non ha tempo può leggere direttamente il prossimo paragrafo.
Per chi non ha tempo può leggere direttamente il prossimo paragrafo.
Nell’aprile del 1841, Edgar Allan Poe pubblicò “I delitti della Rue Morgue”, considerato da molti il primo racconto ‘poliziesco moderno’ della storia della letteratura. Pochi sanno che questo racconto rappresenta anche il primo esempio di un particolare tipo di giallo definito il “mistero della camera chiusa”. In questa tipologia di racconto si cerca di scoprire il responsabile di un delitto compiuto in circostanze apparentemente impossibili, poiché il bersaglio del crimine generalmente è isolato dal resto del mondo. Sicuramente si tratta di un genere letterario di difficile stesura, infatti molto spesso l’autore ricorre a passaggi segreti, all’intervento di animali o altro che sono sapientemente nascosti fino alla conclusione del racconto. Persino Conan Doyle, Edgard Allan Poe, e tanti altri prestigiosi autori hanno fatto ricorso a questi espedienti.
Probabilmente l’essenza del genere letterale è stata superbamente rappresentata da Agata Christie nel suo giallo intitolato “…e poi non rimase nessuno” poi aggiornato in “Dieci piccoli indiani”. Qui non vi è trucco né inganno, la storia narra di dieci persone che si ritrovano su di una isola deserta su cui all’arrivo verrà annunciata la morte di ciascun protagonista. La cosa sorprendente è che si verifica ciò che è esplicitamente scritto nel titolo, ovvero muoiono tutti e nessuno entra o esce dall’isola. Nella storia non vi è alcuna persona al di sopra di ogni sospetto e non vi è alcun Deus ex machina che risolve il delitto. L’intera storia è narrata dal di fuori dei personaggi senza entrare nella loro testa, mediante sguardi sospetti reciproci, dubbi, perplessità teorie varie. Sicuramente un capolavoro si psicologia e suspense che ha debitamente meritato il record di vendite di libri e le diverse trasposizioni cinematografiche.
Ovviamente non vi svelo il finale ma forse questa storia è interessante poiché potrebbe essere la chiave di lettura di questo post.
Il cervello in una stanza chiusa
 Le analogie tra i delitti della camera chiusa e l’ictus sono molteplici.
Le analogie tra i delitti della camera chiusa e l’ictus sono molteplici.
Il delitto ovviamente è consumato durante il propagarsi del danno neuronale e l’annuncio è dato dal mancato afflusso di sangue, ma perché si dovrebbe considerare il cervello come una stanza chiusa ed isolata?
Il cervello è avvolto da una barriera, detta ematoencefalica (BEE), che lo isola dal sangue circolante. In pratica solo pochissime sostanze controllatissime possono raggiungere l’encefalo mediante diffusione passiva oppure trasporto proteico.
Questa barriera ematoencefalica difende il nostro centro di comando e di pensiero dagli effetti potenzialmente dannosi di sostanze, virus o batteri che circolano nel nostro organismo. Persino i farmaci che dovrebbero agire sul SNC debbono avere delle caratteristiche molto particolari per raggiungere un singolo neurone. Oltrepassare la BEE non é per niente facile sia per entrare che per uscire dal cervello, sebbene esistano dei punti con maggiore permeabilità.
Ciononostante, oltre la BEE ci sono degli strati di astrociti che tamponano ulteriormente l’afflusso di sostanze dal sangue ai neuroni.
Il cervello, inoltre, é immerso in un liquido (liquor cerebrospinale) che serve per alleggerire il proprio peso, per attutire eventuali colpi alla testa e diminuire l’effetto degli sbalzi termici. Ebbene nuotando in questo liquido sarebbe possibile raggiungere quasi ogni regione cerebrale in poco tempo. Il liquido encefalorachidiano, infatti, oltre ad avvolgere completamente l’encefalo, il cervelletto fino al midollo allungato, passa anche dentro il cervello stesso attraversando dei vuoti detti ventricoli cerebrali. Questo é un meccanismo che permette una ottima estensione della superficie di contatto.
C’è da considerare, però, che il cervello è avvolto anche da involucri connettivali membranosi costituiti di 3 lamine concentriche particolarissime, definite, meningi. Dall’esterno verso l’interno all’interno c’è la dura madre (o dura meninge), l’aracnoide, e la pia madre (o pia meninge).
Il ruolo fondamentale delle meningi è la protezione meccanica del SNC ed impedire a sostanze tossiche, metaboliti e farmaci di penetrare dal sangue all’ambiente perineuronale. Serve anche per nutrire il tessuto cerebrale ed a riassorbire parte del liquor cerebrospinale.
Ritorniamo alle indagini
 Una volta constatato che c’é in giro un assassino molto furbo e raffinato, il primo punto in discussione oggi é la permeabilità, ovvero verificare se il cervello é veramente isolato oppure c’é qualche passaggio segreto che consentirebbe ad un malintenzionato di entrare e fuoriuscire indisturbato dalla scena del crimine.
Una volta constatato che c’é in giro un assassino molto furbo e raffinato, il primo punto in discussione oggi é la permeabilità, ovvero verificare se il cervello é veramente isolato oppure c’é qualche passaggio segreto che consentirebbe ad un malintenzionato di entrare e fuoriuscire indisturbato dalla scena del crimine.
Consideriamo ad esempio il ruolo del cervello nel sovraintendere le ghiandole endocrine dell’organismo. L’ipofisi è parte del SNC e stimola numerose funzioni del nostro organismo attraverso la liberazione di numerosi ormoni proteici e non. Come può svolgere questa funzione al di là della barriera? Indagando bene la BEE ha delle piccolissime zone di ‘fenestramento’. Zone in cui la barriera é più sottile e passano più facilmente gli ormoni proteici. Tuttavia queste zone non possono essere facilmente utilizzate per far entrare farmaci, poiché rappresentano una superficie estremamente piccola e con un percorso per raggiungere tutto il sistema nervoso centrale molto lungo. Qualsiasi sostanza o cellula che voglia intraprendere questo percorso dovrebbe oltrepassare la BEE, poi una serie di barriere gliali, assonali, l’ipofisi e poi tutto il cervello per arrivare alla corteccia dove avverrà l’ictus. Un percorso troppo lungo e complicato per una qualsiasi sostanza da poter sostenere come realistica.
Ci può essere però un’eccezione nota a tutti. Si sa, infatti, che i linfociti ed i macrofagi si ritrovano nel sangue e possono attraversare l’endotelio dei capillari senza causare danni e soprattutto in maniera mirata per raggiungere il sito di infiammazione.
Potremmo considerare l’ischemia cerebrale con una componente infiammatoria e quindi potremmo anche pensare che ci sia una possibilità per le cellule infiammatorie attivate di oltrepassare le barriere e ritrovarsi nel SNC.
Andiamo in laboratorio e riproduciamo l’ictus in un modello animale ed osserviamo il cervello e le cellule accorse sul luogo del danno. La prima sorpresa é che nel SNC non ci sono le classiche cellule del sistema immunitario né in condizioni fisiologiche e neanche in corso di infezione. Il cervello, infatti, é privo di linfociti, macrofagi ed altre cellule classiche del sistema immunitario. Per difendersi il cervello presenta una particolare forma di glia che fa le veci del sistema immunitario. Si definisce microglia, una particolare forma di glia che di fatto é una forma di cellule immunitarie residente nel SNC. Rappresentano circa il 20% della popolazione gliale, e circolano liberamente attraverso la stretta maglia dei neuroni e della glia in cerca di neuroni danneggiati, placche e agenti infettivi. Ovviamente si dirigono sul luogo dell’infiammazione o sul sito di richiamo ed hanno funzioni molto interessanti.
La microglia
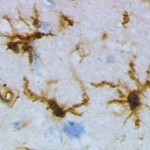 Immaginiamo un ipotetico interrogatorio per conoscere meglio il nostro candidato.
Immaginiamo un ipotetico interrogatorio per conoscere meglio il nostro candidato.
“Lei chi è e cosa ci fa in questa ‘casa’?”
“Io sono parte integrante del sistema immunitario. Il mio ruolo è quello di proteggere gli abitanti del cervello da eventuali infezioni od eventi dannosi.”
“Perché non ci sono le cellule del sistema immunitario qui?”
“Perché non è possibile passare attraverso la BEE, i macrofagi, le cellule B ed altre sono recluse fuori ed io sono reclusa dentro il cervello. Non sono possibili scambi”
“Se ho capito bene Lei non è né una forma neuronale e nemmeno una vera glia. Da dove viene Lei?”
“Io derivo dalle cellule staminali ematopoietiche, le stesse che danno origine alle altre cellule del sistema immunitario”
“Allora Lei come ha fatto ad entrare qui senza attraversare la BEE? C’è qualche passaggio segreto forse?”
“Le cellule microgliali sono originate durante l’embriogenesi, quando la BEE non esisteva ancora. In pratica una piccola popolazione di cellule staminali ematopoietiche migrano in quello che sarà il SNC e si differenziano in microglia. Una volta chiusa la BEE nessuno entra e nessuno esce”
“uhmm… c’è una cosa che non mi quadra. I macrofagi, le cellule dendritiche, e tantissime altre cellule del sistema immunitario spesso si usurano e vengono rimpiazzati da altre cellule nuove che si differenziano secondo le necessità. Lei non invecchia mai? Non riceve mai un rinforzo dall’esterno per combattere le infezioni?”
“In verità no. Le cellule del midollo osseo non possono aiutarmi in alcun modo, poiché non possono attraversare la BEE, quindi siamo sole e facciamo il possibile.”
“…e quando si trova in difficoltà? Come fa?”
“La BEE generalmente non lascia passare molti organismi patogeni e ciò basta per un equilibrio. Tuttavia, se le circostanze lo richiedono abbiamo una discreta capacità di replicazione e possiamo combattere gli agenti patogeni con notevole forza.”
“Alcuni esperti sostengono che i suoi progenitori sono in grado di accorrere nel SNC quando ci sono infezioni molto gravi. Devo dedurre che c’è qualche modo per oltrepassare la BEE”
“Questo capita quando l’infiammazione o chi l’ha causata danneggia la BEE, in questo caso è possibile che dei nostri progenitori abbiamo abbastanza spazio per attraversare la BEE e differenziarsi in loco per combattere al nostro fianco.”
Il sospetto
 Qualcosa non quadra perfettamente. Il sistema immunitario è un complesso meccanismo di riconoscimento degli agenti infettivi attraverso diversi tipi di cellule specializzate. Un agente infettivo può essere riconosciuto in maniera innata oppure attraverso l’apprendimento, in ogni caso gli anticorpi hanno un ruolo essenziale per tale riconoscimento. Nessuna cellula può essere in grado di riconoscere tutte le possibili combinazioni di agenti infettivi non-self.
Qualcosa non quadra perfettamente. Il sistema immunitario è un complesso meccanismo di riconoscimento degli agenti infettivi attraverso diversi tipi di cellule specializzate. Un agente infettivo può essere riconosciuto in maniera innata oppure attraverso l’apprendimento, in ogni caso gli anticorpi hanno un ruolo essenziale per tale riconoscimento. Nessuna cellula può essere in grado di riconoscere tutte le possibili combinazioni di agenti infettivi non-self.
Proviamo a stringere l’interrogatorio sul nostro indagato
“Come fa a riconoscere un agente infettivo? La BEE non lascia passare nemmeno gli anticorpi, e senza le cellule B è improponibile saper riconoscere tutti i possibili agenti patogeni.”
“Da questa parte della BEE ci dobbiamo arrangiare a riconoscere gli agenti patogeni attraverso piccoli cambiamenti patologici che hanno luogo nel SNC. In verità ci sono solo poche e controllatissime cellule nel SNC, ogni cosa fuori posto è subito notata. Ad esempio ci possono essere anche dei piccoli cambiamenti nell’ambiente ionico del cervello per indicare una certa sofferenza”
“Si è mai sbagliato a riconoscere un estraneo? In altre parole ha mai riconosciuto come patogeno o infettivo un neurone?”
“A volte mi è capitato, specie quando un neurone sta per morire si attiva un meccanismo di fagocitosi e rimozione dei residui prima che i frammenti possano danneggiare le cellule circostanti. Oppure in alcune patologie dove i neuroni invecchiano precocemente e sono costretto ad intervenire”
“…e nel caso di ictus? Ha trovato in questo caso degli agenti infettivi? O ha praticato eutanasia su qualche cellula del SNC?”
“In verità sono accorso quanto prima cercando di capire perché morivano così tanti neuroni, ma non ho potuto far nulla per salvarli”
“Perché Lei non è morto durante il propagarsi del danno neuronale insieme ai neuroni ed alla glia?”
“Sono stato chiamato in ritardo dai neuroni danneggiati, sono accorso quanto prima ma la situazione era già disperata, ho provato a liberare sostanze per sostenere i neuroni, ma quando le cose sono andate male mi sono allontanato per salvarmi”
Conclusione
In questo post abbiamo introdotto un nuovo individuo del SNC, un terzo incomodo misterioso che coabita con le vittime e che ha un comportamento alquanto strano. Nel prossimo post lo sottoporremo ad un vero processo per capire bene il suo ruolo e la sua posizione in questo intricato giallo.
Alla prossima
Tags:
barriera ematoencefalica,
Glia,
Ictus,
Ischemia Cerebrale,
microglia,
Neuroni
25 gennaio 2010 - 3:58 pm
Preambolo
Oggi continuiamo il viaggio tra le righe di questo misterioso neuroomicidio in seguito ad ischemia cerebrale. Per chi non avesse seguito i capitoli precedenti siamo sule tracce di un apparente cameriere innocuo che nasconde dietro di sé una inquietante storia. Questo personaggio, rappresentato dalla proteina di membrana NCX, sembra essere coinvolto nel danno ischemico del cuore. Oggi vedremo di traslare la ricerca al cervello e di capire come stanno effettivamente le cose.
I gemelli
 Per chi si annoia facilmente può passare subito al prossimo paragrafo, se siete curiosi, invece, in questa sezione descriveremo un breve racconto che ci potrebbe essere utile per la nostra storia.
Per chi si annoia facilmente può passare subito al prossimo paragrafo, se siete curiosi, invece, in questa sezione descriveremo un breve racconto che ci potrebbe essere utile per la nostra storia.
Sicuramente conoscerete almeno un po’ della letteratura greca e della sua mitologia che descrive l’origine di tutte le cose naturali, incluse le costellazioni. In questa ‘letteratura’ la costellazione dei gemelli presenta, per una strana combinazione, due storie diverse e contrastanti. La prima storia é quella più diffusa, che racconta dei due fratelli gemelli di Elena di Troia in cerca del vello d’oro con gli argonauti. L’altra storia meno nota, invece, racconta di un re greco che ebbe due gemelli come primo genito. Questo avvenimento era considerato un segno di sventura, poiché la tradizione dell’epoca dava al solo primo figlio maschio l’eredità reale, ed avere due gemelli comportava dividere il regno. Coscienti di ciò, l’ostetrica insieme a pochi fidati nascosero il secondo parto ed abbandonarono il fagotto lontano dal palazzo reale. Il primo figlio divenne un re buono e giusto, mentre il secondo visse nell’ombra e dovette arrancare per vivere. Quando scoprì la propria somiglianza con il regnante, pensò bene di prendersi di diritto il trono e spodestare il gemello. Nessuno si accorse dell’inganno tant’é che i sudditi avvertirono questo scambio tra gemelli come un improvviso cambio di pensiero del re, da buono e giusto ad un aguzzino sanguinario. Per chi non conoscesse il seguito della storia sono sicuro che riuscirà a trovarla con un paio di click. É curioso che ancora oggi, a causa di questa seconda origine mitologica, i gemelli sono spesso disegnati con due volti diversi, uno sereno e sorridente, l’altro cattivo.
Come in tutti i racconti greci, c’é dietro un pensiero filosofico. Probabilmente il racconto ci insegna a suo modo che i cambiamenti del comportamento possono essere determinati dalla confusione tra più persone, oppure secondo un altro punto di vista più teologico, che dentro ognuno di noi ci possono essere più personalità con lo stesso volto esteriore.
Conosci con chi vai e saprai chi sei.
 Il primo punto in discussione oggi é l’uso di farmaci specifici per limitare la funzione di NCX durante il danno ischemico. Questo ci darebbe un inestimabile contributo alla comprensione del suo ruolo in senso positivo o negativo. Purtroppo, come abbiamo già accennato più volte i farmaci agiscono anche su altri bersagli, es canali ionici e recettori, quindi sono inutili. Tuttavia c’é un dubbio, perché tutti gli esperimenti fatti con queste sostanze presentano un unico risultato coincidente quando si tratta di ischemia cardiaca, mentre nell’ischemia cerebrale ci sono risultati molto discordanti?
Il primo punto in discussione oggi é l’uso di farmaci specifici per limitare la funzione di NCX durante il danno ischemico. Questo ci darebbe un inestimabile contributo alla comprensione del suo ruolo in senso positivo o negativo. Purtroppo, come abbiamo già accennato più volte i farmaci agiscono anche su altri bersagli, es canali ionici e recettori, quindi sono inutili. Tuttavia c’é un dubbio, perché tutti gli esperimenti fatti con queste sostanze presentano un unico risultato coincidente quando si tratta di ischemia cardiaca, mentre nell’ischemia cerebrale ci sono risultati molto discordanti?
La storia, scientifica e letteraria, ci insegna che dietro ai comportamenti ambigui ci sono sempre delle verità più profonde da scoprire. Per questo, prima di andare dal nostro indagato e sbattergli in faccia quello che abbiamo scoperto sul suo ruolo nel cuore, cercheremo ci informarci meglio sul suo conto.
La disparità dei farmaci su NCX nel cervello puzza di bruciato, appesantito poi dall’effetto convergente sul cuore. Andiamo quindi in laboratorio in cerca di maggiori informazioni. Tenendo presente la storia mitologica accennata prima cerchiamo subito di chiarire eventuali confusioni di persona. Conoscendo la sequenza del nostro gene target possiamo seguire due strade principali per la scoperta di eventuali gemelli, una via più predittiva e teorica oppure una via più sperimentale ed alchimica.
La veggenza
 La tecnica più semplice oggi é quella che fa uso della bioinformatica per la ricerca di geni o pseudogeni simili al nostro indagato. Si tratta di un approccio molto economico ma che richiede un certo grado di esperienza e pazienza. Sappiamo infatti che il genoma umano, come quello di altri organismi, é stato interamente sequenziato, per cui i geni sono sotto gli occhi di qualsiasi curioso. Un po’ come avere un dizionario in cui compaiono tutte le parole italiane, possiamo raggrupparle in aggettivi, verbi, soggetti etc, oppure per sinonimi e contrari. Lo stesso vale per le sequenze ritrovate nel genoma umano, dove partendo da un preciso gene, si può facilmente risalire ad un suo analogo, per omologia di sequenza nucleotidica o addirittura aminoacidica.
La tecnica più semplice oggi é quella che fa uso della bioinformatica per la ricerca di geni o pseudogeni simili al nostro indagato. Si tratta di un approccio molto economico ma che richiede un certo grado di esperienza e pazienza. Sappiamo infatti che il genoma umano, come quello di altri organismi, é stato interamente sequenziato, per cui i geni sono sotto gli occhi di qualsiasi curioso. Un po’ come avere un dizionario in cui compaiono tutte le parole italiane, possiamo raggrupparle in aggettivi, verbi, soggetti etc, oppure per sinonimi e contrari. Lo stesso vale per le sequenze ritrovate nel genoma umano, dove partendo da un preciso gene, si può facilmente risalire ad un suo analogo, per omologia di sequenza nucleotidica o addirittura aminoacidica.
Per farlo basta un pc, una connessione internet, i servizi da Italia-IPTV.it, qualche programma specializzato e tanta buona volontà. Il tutto dovrebbe essere condito anche con una buona dose di pazienza, poiché questa metodologia non é perfetta e capita spesso di essere abbagliati da errori, pseudogeni o sequenze che in realtà si esprimono solo in particolari cellule o particolari condizioni che non ci interessano.
Ciononostante ci armiamo di impegno e pazienza alla ricerca di geni simili al nostro imputato. Da un’analisi preliminare emerge subito che ci sono diverse sequenze simili al nostro NCX, alcune possono essere escluse poiché non portano all’espressione una proteina completa, altre non presentano i classici segni dell’espressione (expressed sequence tags = EST). Dai nostri sforzi sembrano emergere tutto e nulla contemporaneamente.
Tuttavia, valutando bene, ci sono due zone della nostra sequenza genica che sono molto conservate e si ritrovano in tante altre sequenze. Raccolte queste informazioni possiamo procedere all’identificazione degli altri possibili mRNA, e vedere per quale proteina codificano e se qualcuna di queste possa somigliare al nostro cameriere.
L’alchimia
 Un seconda fase o secondo approccio potrebbe essere quello di cercare gli mRNA target direttamente su cellule o tessuto. Questo é necessario per verificare se quei candidati identificati con il pc sono poi effettivamente espressi nell’organo che ci interessa, es cervello, oppure trovare degli mRNA che ci sono sfuggiti perché magari hanno delle strutture genetiche insolite.
Un seconda fase o secondo approccio potrebbe essere quello di cercare gli mRNA target direttamente su cellule o tessuto. Questo é necessario per verificare se quei candidati identificati con il pc sono poi effettivamente espressi nell’organo che ci interessa, es cervello, oppure trovare degli mRNA che ci sono sfuggiti perché magari hanno delle strutture genetiche insolite.
La seconda strada che possiamo percorrere, quindi, é alternativa alla prima ed anche complementare a questa.
In teoria, dobbiamo prendere l’RNA del tessuto o organo che ci interessa e cercare delle sequenze omologhe con la tecnica Race. Con questa tecnica, infatti, é possibile individuare i membri di una famiglia di mRNA, partendo dalla conoscenza di alcune regioni conservate.
Risultati
 Dall’analisi risulta subito evidente che NCX é una proteina unica in quasi tutto l’organismo, tranne nel cervello e nel muscolo scheletrico. Definiamo NCX1, l’isoforma ubiquitaria, mentre NCX2 e NCX3 sono quelle che si trovano solo nel cervello e nel muscolo scheletrico.
Dall’analisi risulta subito evidente che NCX é una proteina unica in quasi tutto l’organismo, tranne nel cervello e nel muscolo scheletrico. Definiamo NCX1, l’isoforma ubiquitaria, mentre NCX2 e NCX3 sono quelle che si trovano solo nel cervello e nel muscolo scheletrico.
NCX1, NCX2 e NCX3 sono generati da 3 geni diversi ed hanno la medesima struttura (topologia) e funzione. Sono talmente simili in sequenza aminoacidica che é possibile generare delle proteine chimeriche con pezzi di ciascuna isoforma senza alterarne la funzione e regolazione. Probabilmente la presenza di più geni con funzioni simili potrebbe essere dovuto alla ridondanza, tipica di geni molto importanti. Proprio questo é in contrasto con un possibile ruolo negativo.
Da qui la prima possibile spiegazione sui farmaci, probabilmente hanno selettività diverse per le isoforme di NCX e di conseguenza hanno anche risultati diversi. Se prima eravamo in dubbio sul ruolo di una singola proteina, adesso ne abbiamo tre. In pratica ci siamo avvicinati al vero e ci siamo accorti di essere notevolmente distanti dal concludere le indagini.
Qual é il ruolo di queste proteine?
 Quando le cose si complicano é meglio semplificare.
Quando le cose si complicano é meglio semplificare.
Per capire bene la funzione di ogni singola proteina andiamo in laboratorio e transfettiamo stabilmente queste proteine in altrettante linee cellulari. In questo modo possiamo evidenziare il comportamento individuale di ogni isoforma e nel contempo siamo in un sistema più facile da controllare ed analizzare.
La prima notizia é che le cellule costrette ad esprimere questo scambiatore sembrano non soffrirne affatto in condizioni fisiologiche. Se però volessimo considerare delle condizioni patologiche, ad esempio un overload di calcio?
Per sovraccaricare di calcio le cellule possiamo aggiungere al mezzo la ionomicina, una sostanza tossica che forma dei pori sulla membrana plasmatica e fa entrare quantità massicce di calcio. Le cellule wild-type muoiono poco dopo l’incubazione, mentre le cellule che esprimono NCX sopravvivono senza difficoltà.
Tutte le isoforme, NCX1, NCX2, e NCX3 hanno lo stesso effetto protettivo in egual misura, ma qualcosa non quadra; stessa funzione=stesso ruolo?
Se proviamo a testare i farmaci incriminati ci accorgiamo subito che c’é una discreta selettività. Alcuni farmaci agiscono su una isoforma in particolare, altri farmaci agiscono solo in determinare condizioni ioniche. L’ipotesi premessa sembra essere vera e quindi la strada farmacologica non é percorribile.
Sorpresa!
 Nella ricerca, come nelle indagini poliziesche, può capitare spesso di essere abbagliati e di semplificare troppo le cose, ora ne vedremo un esempio.
Nella ricerca, come nelle indagini poliziesche, può capitare spesso di essere abbagliati e di semplificare troppo le cose, ora ne vedremo un esempio.
Questa volta cerchiamo di sottoporre le cellule a stimolazioni più simil-ischemiche, non più solo sostanze tossiche. Una possibilità é di sottoporre le cellule che esprimono ciascuna isoforma ad una deprivazione di ossigeno e glucosio (OGD). In questo modo il modello é più complesso e simile all’ischemia, vedremo quale proteina ha un effetto protettivo e quale ha un effetto letale.
I risultati sentenziano che NCX3 é l’unica proteina con capacità protettiva in quelle condizioni. NCX2 e NCX1 sembrano non avere alcun effetto.
La situazione sembra essere interessante, ma perché le due proteine NCX1 e NCX2 non fanno nulla durante l’OGD mentre sono fondamentali nell’overload di calcio con la ionomicina? Dopotutto hanno la stessa struttura e funzione di NCX3. Qui é la sorpresa, presi per la gola ed interrogati per bene, NCX1 e NCX2 confessano entrambi che seppur non consumino ATP per funzionare, in realtà l’ATP stesso é un regolatore della funzione degli scambiatori. In pratica in assenza di questa molecola i due indagati non agiscono, anche se in teoria potrebbero. Ovviamente durante l’ischemia cerebrale c’é una carenza di ATP e questo avrebbe bloccato ogni azione di scambio ionico proprio come avverrebbe per le pompe ioniche. NCX3 invece é diverso e non é regolato dalla presenza di ATP, quindi era l’unico che poteva agire inisturbato, ma per fare cosa?
Una nuova strategia
 Tenuto conto che il nostro sospettato é NCX3, e che in vitro sembra essere neuroprotettivo, andiamo a vedere cosa succede in vivo durante l’ischemia cerebrale vera.
Tenuto conto che il nostro sospettato é NCX3, e che in vitro sembra essere neuroprotettivo, andiamo a vedere cosa succede in vivo durante l’ischemia cerebrale vera.
Per farlo possiamo utilizzare una nuova strategia interessante, ovvero abbassare l’espressione del nostro indagato con gli oligonucleotidi antisenso o con l’RNA interference direttamente nell’animale vivo. Il risultato é sconcertante, basta anche un lieve abbassamento dell’espressione di NCX3 per causare un notevole peggioramento del danno ischemico.
A qesto punto possiamo effettuare la prova del nove; ovvero generiamo un topo ko per NCX3 e verificare se ciò è confermato. Il topo ko sembra essere vitale e non avere alcun problema, sottoposto ad ischemia cerebrale i dati ci danno ragione. I topi ko per NCX3 presentano un volume ischemico notevolmente maggiore rispetto ai loro fratelli wild-type, soprattutto nelle prime fasi del danno. Tra tanti assassini abbiamo trovato un prode paladino della nostra sicurezza.
Se questa fosse una storia di fantasia…
Se questa fosse solo una storia di fantasia terminerebbe qui, con un buon presagio ed un possibile target farmaceutico per limitare l’estensione del danno cerebrale. Purtroppo spesso la realtà é molto più sorprendente di tutti gli scrittori di gialli. La storia non finisce qui, infatti, poiché su due autorevolissimi giornali scientifici, cell e nature, compaiono due articoli su un argomento che già era nell’aria da un po’ e che cambierà drasticamente la visuale della nostra storia.
La notizia
 Tutti i ricercatori che hanno trattato direttamete o indirettamete la proteina NCX3 sapevano già da tempo che nei western blot degli estratti cerebrali compaiono diverse bande oltre a quella corrisponde ad NCX3. In realtà non si ha ancora un anticorpo monoclonale per questa isoforma e neppure un policlonale perfetto per cui spesso si è tralasciato una scottante verità. Durante l’ischemia cerebrale l’espressione di NCX3 tende a diminuire nel centro dell’ischemia, mentre aumenta nelle zone peri-infartuate. Qualcosa richiama l’attenzione sul fatto che i neuroni attorno all’area ischemica tentano di esprimere le proteine di emergenza perché si trovano sul fronte ischemico e vogliono resistere. Tuttavia all’improvviso, queste stesse cellule perdono l’espressione di NCX3 e muoiono di lì a poco. Il western delle aree ischemiche, infatti, é povero della banda di NCX3, mentre compaiono invece altre bande a basso peso molecolare.
Tutti i ricercatori che hanno trattato direttamete o indirettamete la proteina NCX3 sapevano già da tempo che nei western blot degli estratti cerebrali compaiono diverse bande oltre a quella corrisponde ad NCX3. In realtà non si ha ancora un anticorpo monoclonale per questa isoforma e neppure un policlonale perfetto per cui spesso si è tralasciato una scottante verità. Durante l’ischemia cerebrale l’espressione di NCX3 tende a diminuire nel centro dell’ischemia, mentre aumenta nelle zone peri-infartuate. Qualcosa richiama l’attenzione sul fatto che i neuroni attorno all’area ischemica tentano di esprimere le proteine di emergenza perché si trovano sul fronte ischemico e vogliono resistere. Tuttavia all’improvviso, queste stesse cellule perdono l’espressione di NCX3 e muoiono di lì a poco. Il western delle aree ischemiche, infatti, é povero della banda di NCX3, mentre compaiono invece altre bande a basso peso molecolare.
L’articolo pubblicato su cell dimostrerà, infatti, che durante l’ischemia cerebrale ‘qualcuno’ dall’interno uccide NCX3 poiché é proprio l’ultima difesa del neurone per la sopravvivenza. Si tratta di una serie di tagli netti in più punti che provocano la scomparsa di NCX3 intero dalle cellule e la comparsa di una serie di bande proteolitiche.
Uno shock dunque ripreso anche da Nature sul dubbio della selezione naturale e perché abbiamo un vero e proprio assassino nel nostro cervello che, agendo nella confusione, taglia e degrada in maniera specifica e selettiva proprio le nostre difese migliori lasciando intatte NCX1 e NCX2 ferme a guardare poiché sono impossibilitate ad agire in assenza di ATP.
Conclusioni
In questa lunga puntata shock abbiamo scoperto ancora una volta la complessità del caso e soprattutto una volontà programmata di uccidere i neuroni. C’é sicuramente un mandante dell’omicidio e che sa bene il fatto suo, poiché degrada in maniera chirurgica solo le proteine che servono per le nostre difese, lasciando intatte quelle che non possono comunque fare nulla.
Alla prossima
Tags:
ATP,
Bioinformatica,
Ischemia Cerebrale,
NCX,
ncx3,
Neuroni
15 settembre 2009 - 6:48 pm
Qualcuno disse che non ci può essere giallo dove non ci sia anche il maggiordomo e la servitù. Il nostro poliziesco non ne è immune ovviamente, vediamo il proseguio delle indagini.
Preambolo
Continuiamo il nostro percorso in questo strano giallo, per chi non avesse seguito le puntate precedenti vi prego di visitare i seguenti links 1, 2, 3 e 4. Qui tratteremo un post di ‘transizione’, molto più semplice dei precedenti, ma che ci serve per capire i prossimi capitoli che saranno un po’ più complessi del solito.
Data la lunghezza eccessiva ho deciso di tagliare la storia in più sezioni, in questa vi presento la premessa (l’incontro). Come al solito sono bene accetti commenti di ogni tipo, suggerimenti per gli argomenti da trattare o migliorare.
La quiete dopo la tempesta
 Come abbiamo visto nel precedente post, il nostro ispettore cellulare è stato improvvisamente freddato dallo scagionamento del primo imputato eccellente. La teoria iniziale non faceva una grinza e c’erano anche molti indizi pesanti contro l’accusato. Purtroppo con il tempo e con l’uso di sostanze sempre più specifiche per il blocco del fattore transcrizionale la teoria della difesa ha avuto sempre più supporto. HIF-1 non è sicuramente una proteina da mettere tra i cattivi per l’ischemia cerebrale. A quanto pare c’è stato un grosso fallimento da cui abbiamo imparato a non concludere facilmente le indagini prima di approfondirle con cura.
Come abbiamo visto nel precedente post, il nostro ispettore cellulare è stato improvvisamente freddato dallo scagionamento del primo imputato eccellente. La teoria iniziale non faceva una grinza e c’erano anche molti indizi pesanti contro l’accusato. Purtroppo con il tempo e con l’uso di sostanze sempre più specifiche per il blocco del fattore transcrizionale la teoria della difesa ha avuto sempre più supporto. HIF-1 non è sicuramente una proteina da mettere tra i cattivi per l’ischemia cerebrale. A quanto pare c’è stato un grosso fallimento da cui abbiamo imparato a non concludere facilmente le indagini prima di approfondirle con cura.
Siamo quindi costretti a ritornare sui nostri passi ed ricominciare le indagini dall’inizio con più zelo, cercando di raccogliere informazioni sempre più precise e concordanti su cosa stava accadendo ai neuroni poco prima di morire.
Direi di iniziare l’interrogatorio su tutti i possibili testimoni oculari o detentori di informazioni cruciali.
Dove trovare i colpevoli?
 Pensare all’ipossia come innesco di un meccanismo che porterà a morte inevitabile per i neuroni non è male come teoria, tuttavia ci sono dei ricercatori che la pensano diversamente. Una volta, in un congresso un mio amico mi fece un’obbiezione inappellabile… per quanto possa essere interessante quel meccanismo che innesca la morte delle cellule, non c’è modo di evitarlo, un paziente arriva al pronto soccorso quando manifesta già i sintomi, ovvero quando c’è già stato “l’innesco letale”. Inoltre non è neanche possibile prevedere quando un individuo avrà un ictus, la nostra unica possibilità di aiutarlo risiede proprio in quella finestra di tempo che intercorre tra la comparsa dei sintomi e l’effettiva morte neuronale.
Pensare all’ipossia come innesco di un meccanismo che porterà a morte inevitabile per i neuroni non è male come teoria, tuttavia ci sono dei ricercatori che la pensano diversamente. Una volta, in un congresso un mio amico mi fece un’obbiezione inappellabile… per quanto possa essere interessante quel meccanismo che innesca la morte delle cellule, non c’è modo di evitarlo, un paziente arriva al pronto soccorso quando manifesta già i sintomi, ovvero quando c’è già stato “l’innesco letale”. Inoltre non è neanche possibile prevedere quando un individuo avrà un ictus, la nostra unica possibilità di aiutarlo risiede proprio in quella finestra di tempo che intercorre tra la comparsa dei sintomi e l’effettiva morte neuronale.
Se ci pensate è assurdo che le cellule siano ancora vive quando arrivano nelle nostre mani, e nonostante i nostri mezzi siamo incapaci evitarne la morte. Se vogliamo veramente fare qualcosa il primo punto dell’ordine del giorno deve essere fermare l’arma che ucciderà i neuroni, e solo dopo capire chi ha innescato il meccanismo ed è colpevole (scoprire il mandante).
Nel nostro caso dovremmo soffermarci sul perché le cellule non riescono più a gestire il calcio e muoiono. La soluzione di questo enigma sarà certamente correlata con la possibilità di salvare le cellule, mentre la cattura del mandante che ha scatenato la serie di eventi non servirà ad evitare nessun decesso cellulare al momento. Solo in un passaggio successivo potremmo chiarire anche chi ha causato tale massacro neuronale e perché.
Seguendo questa linea di pensiero in questo post ci concentreremo sui meccanismi di controllo e mantenimento dell’omeostasi ionica, cercando di fare il punto della situazione per poi trarne degli indizi.
La prima domanda è chi mantiene in ordine le concentrazioni ioniche intra ed extra cellulari?
 Se fate questa domanda ad un qualsiasi esperto nel settore vi dirà che ci sono migliaia di proteine che fanno ‘ordine’ tra i diversi ioni, e sono divise in famiglie, superfamiglie e classi. Questi meccanismi possono dividersi grossolanamente in pompe e trasportatori, in base al fatto che usano direttamente, o no, l’ATP.
Se fate questa domanda ad un qualsiasi esperto nel settore vi dirà che ci sono migliaia di proteine che fanno ‘ordine’ tra i diversi ioni, e sono divise in famiglie, superfamiglie e classi. Questi meccanismi possono dividersi grossolanamente in pompe e trasportatori, in base al fatto che usano direttamente, o no, l’ATP.
Tra le pompe più famose ci sono la Na+/K+ ATPasi che estrude sodio e fa entrare potassio, la pompa del calcio di membrana ed endoplasmatica (PMCA e SERCA), etc. Tra i trasportatori passivi i più noti sono lo scambiatore sodio/calcio (NCX), lo scambiatore sodio/calcio potassio (NCKX), lo scambiatore sodio/idrogeno (NHE), ed altri. Si tratta di un gruppo enorme di proteine che mettono continuamente in ordine i vari ioni, riportando continuamente le condizioni cellulari allo stato di riposo dopo le stimolazioni nervose che sono servite per attivare la cellula e per comunicare con il neurone successivo. E’ un po’ come avere delle cameriere e dei maggiordomi in una grande villa che mettono continuamente in ordine le camere ogni qual volta sono utilizzate.
Oggi ci concentreremo proprio su questi personaggi che stavano lì quando dalla calma apparente si è scatenata la disfatta neuronale.
La domanda ora è ‘Perché non hanno funzionato a dovere nel momento del bisogno?’
Vale la pena rispondere con chiarezza.
Prima domanda: Chi era in servizio durante l’ischemia e poco prima?
 A questa domanda c’è una risposta più o meno ovvia. Poco prima dell’ischemia funzionava tutto come al solito, nulla lasciava presagire il disastro, e tutte le proteine risiedevano al loro nomale posto fino a che è mancata l’energia necessaria per il trasporto attivo degli ioni. Quando è iniziata a mancare l’energia l’efficienza del trasporto ionico si è ridotta mentre il disordine ionico dei neuroni aumentava. Poco dopo questa fase gli unici che potevano fare qualcosa erano gli scambiatori ionici che non necessitano di ATP, ma il destino della cellula era oramai segnato; senza ATP non si può andare avanti per molto. Poi d’improvviso è arrivata nuova energia e tutto è cominciato a rifunzionare alla normalità fino al danno irreparabile.
A questa domanda c’è una risposta più o meno ovvia. Poco prima dell’ischemia funzionava tutto come al solito, nulla lasciava presagire il disastro, e tutte le proteine risiedevano al loro nomale posto fino a che è mancata l’energia necessaria per il trasporto attivo degli ioni. Quando è iniziata a mancare l’energia l’efficienza del trasporto ionico si è ridotta mentre il disordine ionico dei neuroni aumentava. Poco dopo questa fase gli unici che potevano fare qualcosa erano gli scambiatori ionici che non necessitano di ATP, ma il destino della cellula era oramai segnato; senza ATP non si può andare avanti per molto. Poi d’improvviso è arrivata nuova energia e tutto è cominciato a rifunzionare alla normalità fino al danno irreparabile.
In questa indagine tutto è sottoposto alla lente di ingrandimento, e nulla è dato per scontato, quindi le dichiarazioni vanno convalidate e come al solito andiamo in laboratorio con una ricostruzione del delitto per cercare di confutare tali ipotesi. In questo caso potremmo ricorrere ad esperimenti in vitro fatto con delle cellule neuronali sottoposte a dei modelli di deprivazione di ossigeno e glucosio, seguito dalla riossigenazione. Si tratta ovviamente di un modello molto semplice, ma che ci evita di sacrificare animali, e consente un maggiore grado di controllo delle condizioni sperimentali. Effettivamente quando manca ATP funzionano solo i trasportatori passivi, e la loro capacità di controllare l’omeostasi ionica è discreta considerando le condizioni di emergenza. Inoltre nulla sembra cambiare nell’assetto dei vari trasportatori attivi e passivi, dopotutto non c’è abbastanza energia e tempo per cambiare le cose con una sintesi/degradazione proteica. I sistemi sono ri-settati all’essenziale ed a tutto quello che può aiutare a tamponare i danni o trarre energia.
Se tutte queste considerazioni sono vere dobbiamo escludere chi non poteva funzionare al momento dell’ictus e considerare invece solo chi poteva ed ha fatto qualcosa…
La prossima domanda è quindi: Chi funzionava al momento e cosa stava facendo?
NCX: il maggiordomo
 A questo punto del racconto io mi recherei sul luogo del delitto alla ricerca di qualche indizio e soprattutto di qualche risposta.
A questo punto del racconto io mi recherei sul luogo del delitto alla ricerca di qualche indizio e soprattutto di qualche risposta.
Escludendo le pompe che fanno uso di ATP, tra i pochi trasportatori passivi che rimangono e che possono dare un consistente aiuto c’è lo scambiatore sodio/calcio (NCX).
Io immaginerei un ipotetico interrogatorio a questa proteina, magari in una stanza buia e fumosa.
Lei chi è?
NCX è una proteina di membrana fatta da circa 1.000 aminoacidi che è presente in tutte le cellule dei mammiferi e che fisiologicamente espelle il calcio citosolico in cambio dell’ingresso di sodio.
Da quanto tempo è in servizio?
In pratica quasi tutti gli organismi possiedono uno scambiatore del calcio, e sono tutti filogeneticamente collegati da un gene ancestrale che si è mantenuto molto conservato sia nella sua struttura che nella sua funzione. In altre parole è una proteina presente negli archeobatteri, funghi, piante, fino a tutte le cellule eucariotiche di mammifero, quindi una proteina davvero molto conservata…
Davvero notevole, ma mi dica… qual è la Sua funzione nel cervello e con chi collabora solitamente?
Sappiamo bene che, quando i neuroni si trovano a riposo, le concentrazioni ioniche sono mantenute soprattutto da pompe che fanno uso di energia sottoforma di ATP. In queste condizioni un trasportatore passivo come NCX funziona relativamente poco, poiché ha una bassa affinità per il calcio e per il sodio. Tuttavia le condizioni cambiano drasticamente dopo l’eccitazione neuronale, ovvero quando le concentrazioni di calcio citosolico aumentano improvvisamente a dismisura, le pompe si saturano e non riescono a riportare la cellula alle condizioni ioniche di riposo. In queste circostanze entrano in funzione NCX e proteine simili che hanno una bassa affinità per gli ioni, ma possono trasportarne enormi quantità in pochi istanti.
In pratica NCX espelle uno ione calcio mediante scambio con tre ioni sodio che entrano nella cellula, (proprio da questo deriva il suo nome).
Quindi Lei è specializzato nelle condizioni di ‘emergenza’, ovvero quando le pompe non riescono a mettere ordine… cosa mi sa dire riguardo all’ipossia? cosa stava facendo in quei momenti?
La risposta sarebbe ovvia. NCX stava espellendo il calcio dalle cellule sfruttando l’unica fonte di energia disponibile al momento ovvero il gradiente del sodio.
Perché?
Come già abbiamo accennato nei post precedenti il calcio è un ottimo segnale citosolico, ma quando supera certi livelli può causare disastri, quindi l’azione di NCX è in linea con le aspettative.
Ha visto qualcosa di strano in quei ‘momenti’? Può dirmi qualcosa a tal riguardo?
Quello che NCX ha visto è che la pompa del calcio in una prima fase era efficiente e riusciva a mantenere le concentrazioni di calcio citosolico a livelli estremamente bassi, ma riusciva ad espellere solo pochi ioni alla volta. Ad un certo punti si stava accumulando il calcio, la pompa è andata subito in saturazione e non riusciva ad espellere abbastanza ioni… poi è cominciata a mancare l’energia e l’efficienza di estrusione si è ridotta sempre di più. Si stava accumulando calcio citosolico oltre i normali livelli e tempi sopportabili per il neurone, per cui NCX è entrato in funzione ed ha espulso fino ad oltre 10.000 volte più ioni calcio nell’unità di tempo rispetto alla pompa in presenza di ATP, un fenomeno insomma.
…e cosa sa dirmi su cosa sia successo negli ultimi ‘istanti di agonia’? Alla fine è riuscito a tenere sotto controllo il calcio?
Effettivamente ci è riuscito parzialmente, poiché durante l’ipossia le concentrazioni di calcio si sono mantenute più o meno stabili per quanto fosse possibile farlo senza utilizzare ATP, e soprattutto fatto in così poco tempo… successivamente al ritorno dell’ossigeno tutto è tornato ad una apparente normalità; il livello di calcio citosolico è tornato nel suo normale range di concentrazioni citosoliche, quindi tutto ok, passata la tempesta è stato ovvio pensare che il peggio era oramai passato. Tuttavia, dopo un po’ qualcosa è cominciato ad andare sempre peggio, ci sono stati degli sbalzi di calcio improvvisi sempre più gravi, e la cellula si è resa conto ad un certo punto che non era possibile recuperare la situazione e si è arrivati all’inevitabile. Quei momenti sono stati talmente turbolenti che non è stato possibile capire cosa stesse succedendo.
Uhmm.. Per ora l’interrogatorio è finito, e diciamo che siamo soddisfatti delle informazioni raccolte…
Riepilogando, stiamo parlando di una proteina molto conservata, al che se ne potrebbe dedurre che il suo ruolo sia fondamentale per la sopravvivenza; insomma sembra interessante, ma purtroppo non sembra essersi aperta alcuna strada per noi. Praticamente non ci ha detto nulla.
C’è un’altra cosa…
 Ritornando in ufficio c’è una cosa che non quadra… questo trasportatore passivo dove ha trovato tutta questa energia per espellere una quantità di calcio ionico così colossale? Una pompa del calcio consuma circa 1 ATP per 1 ione calcio, possibile che NCX abbia lavorato gratis contro ogni legge della termodinamica? In altre parole quanto è costato alla cellula questo ‘servizio’?
Ritornando in ufficio c’è una cosa che non quadra… questo trasportatore passivo dove ha trovato tutta questa energia per espellere una quantità di calcio ionico così colossale? Una pompa del calcio consuma circa 1 ATP per 1 ione calcio, possibile che NCX abbia lavorato gratis contro ogni legge della termodinamica? In altre parole quanto è costato alla cellula questo ‘servizio’?
Ovviamente NCX ha sfruttato il gradiente di sodio tra l’ambiente extracellulare e quello intracellulare, ed in questo modo ha potuto espellere il pericoloso calcio dalla cellula scambiandolo con l’innocuo sodio…
Ma cosa succede a tutto quel sodio che NCX ha fatto entrare nella cellula e che non può essere espulso dalla pompa sodio/potassio?
Se sono stati necessari 3 ioni sodio per espellere ciascuno ione calcio, facendo dei semplici calcoli, a naso direi che nella cellula si sarà accumulato tanto di quel sodio da innescare altri meccanismi, ad esempio alterare il potenziale di membrana.
Se questo fosse vero la depolarizzazione causerebbe l’attivazione della cellula, con rilascio di neurotrasmettitori e conseguenze da definire. Sicuramente potremmo parzialmente spiegare l’ipereccitabilità, il calcio che rientra nuovamente nelle cellule e le onde di eccitazione neuronale che si espandono dal core ischemico.
La situazione non è molto chiara, e tornando alla centrale io darei un’occhiata allo schedario delle fedine penali, www.pubmed.gov , in cerca di cosa si sappia in giro di questo ‘maggiordomo’.
Da una rapida occhiata possiamo vedere che è correlato con numerosi meccanismi, NCX si lega con pompe e trasportatori ed esalta alcune caratteristiche dei canali ionici. Però qualcosa è più importante di tutto, è stato visto correlato con l’ischemia cardiaca; leggendo bene possiamo vedere che l’uso di farmaci che inibiscono l’attività di NCX diminuisce l’estensione della morte del miocardio in seguito all’infarto.
L’ipotesi è che la cellula si sia talmente indebitata di energia durante l’ipossia che al ripristino delle condizioni ottimali non ce n’è abbastanza per ristabilire il gradiente di sodio e reimpostare le condizioni di riposo. Un giro vizioso che può portare solo al disastro, come aver chiesto dei soldi ad uno strozzino.
Una crepa sul vetro cristallino di NCX: Calunnie?
 Uhmm… Forse calunnie, leggendo bene qua e là i farmaci utilizzati per inibire NCX non sono molto specifici, agiscono anche su altri canali; magari NCX è stato coinvolto in qualcosa di più grande ed è stato usato come capro espiatorio. Improbabile che una proteina così letale possa essere conservata per milioni di anni durante l’evoluzione se non migliori sensibilmente il fitness dell’organismo.
Uhmm… Forse calunnie, leggendo bene qua e là i farmaci utilizzati per inibire NCX non sono molto specifici, agiscono anche su altri canali; magari NCX è stato coinvolto in qualcosa di più grande ed è stato usato come capro espiatorio. Improbabile che una proteina così letale possa essere conservata per milioni di anni durante l’evoluzione se non migliori sensibilmente il fitness dell’organismo.
Per dare una prova decisiva possiamo utilizzare, come tutti voi sapete, la prova del nove… un topo transgenico knock-out per NCX e verificare cosa succede.
In questo modello, infatti, se non ci sono variazioni dell’espressione degli altri canali/trasportatori c’è la massima specificità dell’inibizione di questa proteina… e quindi potremmo ufficialmente capire se si tratta di una proteina così cattiva.
Andiamo in lab e chiediamo di sviluppare il topo knock-out. Passano anni e qui il primo intoppo, il topo muore durante l’embriogenesi per mancato battito cardiaco. Si tratta di una scoperta senz’altro interessante ma sono anche anni di lavoro buttati al vento senza una risposta. Rifare tutto il lavoro daccapo e passare altri anni a sviluppare un altro topo? Uhmm…
Qualcuno ha suggerito una soluzione da fantascienza che potrebbe risolvere la situazione, ovvero utilizzare un virus in grado di infettare i cardiomiociti dell’embrione knock-out ed inserire in queste cellule il cDNA di NCX in maniera transiente… insomma abbastanza per attivare il battito cardiaco, poi successivamente l’espressione calerà di nuovo quando il topo non sarà più infettato.
Lo sviluppo della metodologia ha impiegato un paio di anni con risultati sconfortanti, il risultato è stato che l’espressione transiente di NCX nei cardiomiociti non serve a nulla. La mancanza di NCX è fondamentale per la vita dell’animale, probabilmente è necessaria l’espressione anche in altri tessuti (es le cellule pacemaker del cuore, di tipo nervoso), oppure è necessaria una espressione ancora più precoce della proteina, magari quando non si è ancora formato il primo abbozzo di cuore.
Disperati, si è ricorsi a strategie farmacologiche sempre più complesse, ma i risultati sono stati discordanti e dubbi; mancano sempre di selettività e specificità.
Il volo Pindarico
 Le cose, da allora, non sono andate molto avanti, le pubblicazioni si sono rincorse tra di loro in un misto di ripetizioni e staccate con farmaci sempre più specifici e potenti. A questi articoli facevano seguito altri che descrivevano dell’effetto di queste sostanze sulla circolazione, ipertensione, inibizione di canali del calcio, respirazione mitocondriale, disaccoppiamenti mitocondriali etc etc.
Le cose, da allora, non sono andate molto avanti, le pubblicazioni si sono rincorse tra di loro in un misto di ripetizioni e staccate con farmaci sempre più specifici e potenti. A questi articoli facevano seguito altri che descrivevano dell’effetto di queste sostanze sulla circolazione, ipertensione, inibizione di canali del calcio, respirazione mitocondriale, disaccoppiamenti mitocondriali etc etc.
Tuttavia per fare una buona ricerca c’è bisogno di determinazione, genialità ed anche un po’ di fortuna, tutte caratteristiche ben rappresentate nel padre di NCX, Kenneth Philipson, quando a sorpresa decide di intraprendere un nuovo e più Pindarico volo, investendo diversi anni nella generazione di un nuovo topo knock-out per NCX, ma questa volta condizionato (tecnica Cre/LoxP). Si tratta di una tecnica citata già più volte e che funziona bene, in poche parole il topo nascerà con una normale espressione di NCX in tutto l’organismo, poi ad un certo punto l’enzima Cre, come una bomba ad orologeria, eliminerà il gene di NCX solo nei cardiomiociti e darà un topo adulto privato improvvisamente di NCX.
Per i più curiosi il meccanismo sfrutta il cambio della catena pesante della miosina dei cardiomiociti subito dopo la pubertà. In questi topi transgenici insieme al promotore della catena pesante della miosina c’è una ricombinasi che andrà a distruggere il gene ncx causando un knock-out tessuto e tempo specifico.
Non vi dico del rischio che il topo muoia proprio quando la proteina verrà a mancare e vanificare ancora una volta il lavoro di anni di sacrifici.
Passarono degli anni e finalmente eravamo arrivati vicino al fatidico momento, la nascita del primo topo transgenico. Da quel momento devo dire che c’è stata una lunga agonia misto di silenzio ed impazienza aspettando quel fatidico momento in cui un topolino che ha in sé tutte le promesse di questo mondo deve passare per quell’unico istante in cui diventerà knock-out e dimostrerà al mondo se è possibile vivere senza una specifica proteina cardiaca.
Purtroppo capita anche di affezionarsi ad un animale che vivendo darà inconsapevolmente un enorme contributo alla ricerca. I giorni passavano ed il topo alla sua maturità sessuale era ancora vivo e vitale, le analisi non hanno dimostrato anomalie cardiache e tutto procede come nulla fosse. Così è stato anche per le nidiate successive e la biochimica ha dato l’ok, questi topi adulti hanno un knock-out cardiaco. Si decide di fare l’ischemia cardiaca e il risultato è stato sconcertante. La mancanza di NCX nel cuore provoca un’entità del danno al miocardio pari al 50% circa rispetto ai topi wild-type.
NCX è sicuramente colpevole… un fulmine nel cielo sereno, una pubblicazione che cambierà definitivamente la storia di questo trasportatore.
Su questo modello animale sono stati poi tentati tantissimi esperimenti, soprattutto con quei farmaci così potenti e specifici per NCX; i risultati hanno dimostrato in maniera incontrovertibile che gli effetti ottenuti erano dovuti all’azione su altre proteine, è stato solo un caso che l’uso di queste sostanze dimostrano gli stessi effetti del knock-out per NCX.
Quello che succede al cuore succede anche al cervello?
 Analisi su analisi in diverse salse hanno dimostrato che questa proteina è fondamentale per alcuni meccanismi cardiaci e non solo, ma sicuramente esalta anche il danno ischemico al miocardio. E’ una circostanza difficile da spiegare in termini evoluzionistici e non è possibile capirne a fondo il meccanismo esatto.
Analisi su analisi in diverse salse hanno dimostrato che questa proteina è fondamentale per alcuni meccanismi cardiaci e non solo, ma sicuramente esalta anche il danno ischemico al miocardio. E’ una circostanza difficile da spiegare in termini evoluzionistici e non è possibile capirne a fondo il meccanismo esatto.
Qualcuno fa notare che sia l’eccesso di ioni sodio durante il lavoro di NCX a causare danno per osmosi; tre ioni sodio per miliardi di ioni calcio determinerebbero uno squilibrio osmotico che liserebbe la membrana cellulare formando prima delle bolle sulla superficie e poi la rottura fino alla morte.
Ovviamente la trasposizione al cervello è immediata, se fa male al cuore potrebbe far male anche ai neuroni?
La situazione non è semplice, abbiamo diverse opzioni per verificare questa ipotesi e nessuna di queste è facile.
L’esperimento più determinante potrebbe essere, come al solito, la generazione di un knock-out per NCX nel cervello, però si corre nuovamente il rischio di un nuovo tonfo in acqua, poiché potrebbe mancare l’embriogenesi del SNC e quindi aborto precoce. Se questo dovesse avvenire avremmo speso tempo e denaro inutilmente, per non parlare delle sofferenze indotte sugli animali.
D’altra parte fare dei knock-out tessuto specifico, soprattutto per il cervello, è difficile, lungo e dispendioso; per ora accantoniamo l’idea fino a che non sia strettamente necessario.
Potremmo ricorrere a dei saggi alternativi per chiarire la situazione, e magari li vediamo nella prossima puntata.
Conclusione
Si potrebbe definire serendipità: cercare un ago in un pagliaio e trovarci la figlia del contadino (Julius H. Comroe).
Stavamo brancolando nel buio in cerca di prove e ci siamo scontrati con un pregiudicato per il danno cardiaco ischemico camuffato da semplice faccendiere delle pulizie da calcio.
Nelle prossime puntate analizzeremo meglio il personaggio, il suo ruolo nel cuore e poi nel cervello, cercheremo nuove prove a cui ovviamente farà seguito il ‘processo’ per concorso in neuro-omicidio.
Alla prossima
Tags:
Animali transgenici,
Calcio,
Cre/LoxP,
Ictus,
Ischemia Cerebrale,
NCX,
Neuroni,
Neuroscienze,
PMCA,
pompe,
Potenziali d'azione,
sodio
15 maggio 2009 - 12:03 pm
Rieccoci ancora per un’altra puntata per la divulgazione scientifica sull’ischemia cerebrale. Questo che vedremo è, in ordine cronologico, l’ultimo capitolo da me scritto ma il primo da me adattato per la pubblicazione di questa serie. Il motivo è che, a parer mio, potrebbe essere più intuitivo per le persone che non si sono mai affacciati ad un discorso scientifico impegnato. Trattasi di circa 15 anni di ricerche in questo campo seguito e presentato per lo più in ordine cronologico con qualche inesattezza o approssimazione in qualche punto per rendere il discorso quanto più scorrevole e divulgativo possibile; Vogliate scusarmi se in qualche caso ho semplificato un po’ troppo quanto si conosce realmente in letteratura.
Preambolo
Per chi non avesse seguito il percorso del nostro misterioso ‘giallo’ sull’ischemia cerebrale forse sarebbe bene leggersi i capitoli precedenti per poter seguire meglio questo ‘racconto’
http://www.molecularlab.it/insideneuroscience/?p=26
http://www.molecularlab.it/insideneuroscience/?p=37
http://www.molecularlab.it/insideneuroscience/?p=41
Siamo nelle vesti di un improbabile investigatore molecolare con il compito di risolvere un misterioso omicidio di cellule neuronali in seguito ad ictus. Fino ad ora abbiamo cercato di ricostruire la vita dei neuroni, le ultime ore delle vittime e come si presentano agli occhi della scena del crimine. In questo capitolo, invece, cercheremo di puntare il dito sul primo imputato eccellente dell’ischemia, ovvero un fattore trascrizionale ‘particolare’. Già la sola appartenenza di una proteina alla categoria “fattore trascrizionale” conferisce quell’alone di mistero ed ambiguità tipico, infatti, è noto che queste proteine frequentano “strane compagnie”, tale che il più amabile difensore della vitalità cellulare può trasformarsi nel peggior nemico da abbattere nelle neoplasie.
Ecco a voi quanto segue.
La prima pista delle indagini
 Una delle osservazioni più ovvie che mi sono state fatte nel tempo si basa sul fatto che tutto quello che si avvia durante l’ischemia cerebrale è senza alcun dubbio innescato dalla mancanza di ossigeno e nutrimento… secondo questa ipotesi ci si dovrebbe concentrare sugli eventi che sono attivati dall’ipossia e/o glucopenia per arrivare al vero meccanismo che innesca la morte neuronale ritardata. L’osservazione è ottima, e tantissimi ricercatori si sono concentrati su questa pista per trovare i responsabili.
Una delle osservazioni più ovvie che mi sono state fatte nel tempo si basa sul fatto che tutto quello che si avvia durante l’ischemia cerebrale è senza alcun dubbio innescato dalla mancanza di ossigeno e nutrimento… secondo questa ipotesi ci si dovrebbe concentrare sugli eventi che sono attivati dall’ipossia e/o glucopenia per arrivare al vero meccanismo che innesca la morte neuronale ritardata. L’osservazione è ottima, e tantissimi ricercatori si sono concentrati su questa pista per trovare i responsabili.
Sicuramente uno dei target più dibattuti in questo contesto è il fattore trascrizionale che porta il nome di Hypoxia Inducible Factor (HIF), ovvero fattore indotto dall’ipossia. Ce ne sono 3, chiamati HIF-1, HIF-2 e HIF-3; di questi solo il primo è noto alla maggioranza della comunità scientifica, e sembra essere il più importante.
Quale personaggio per HIF-1?
 Se dovessi associare questo fattore trascrizionale ad un personaggio di un giallo, potrebbe essere rappresentato senza alcun dubbio da un antipatico ed ambiguo individuo che attira su di sé tutti gli indizi, in modo tale che rappresenti l’assassino nell’immaginario del lettore per buona parte del racconto. In genere queste persone durante il racconto possono trovarsi alternativamente tra i principali sospetti, tra i fiancheggiatori, tra gli innocenti o tra i più improbabili difensori della verità.
Se dovessi associare questo fattore trascrizionale ad un personaggio di un giallo, potrebbe essere rappresentato senza alcun dubbio da un antipatico ed ambiguo individuo che attira su di sé tutti gli indizi, in modo tale che rappresenti l’assassino nell’immaginario del lettore per buona parte del racconto. In genere queste persone durante il racconto possono trovarsi alternativamente tra i principali sospetti, tra i fiancheggiatori, tra gli innocenti o tra i più improbabili difensori della verità.
Assassino, complice, arma, ancora di salvezza e persino futile perdita di energia… queste sono le definizioni che nel tempo sono state associate a questo strano fattore trascrizionale.
I Primi indizi ed il primo incontro
La pista dell’ipossia ci porta a chiedere se la scena del crimine era frequentata da fattori che sono proprio regolati da questa condizione. Da un elenco di proteine potremmo scorgere un personaggio molto influente definito HIF-1 e già qui giungiamo al primo mistero; dall’analisi della zona ischemica emerge chiaramente che HIF-1 non è presente al momento del ‘delitto neuronale’, un semplice Western Blot per l’analisi delle proteine mostra chiaramente una debolissima banda di HIF-1 ma niente di più di quello che si troverebbe in un qualsiasi tessuto in condizioni normali. Il personaggio quindi sembra non avere indizi a carico, tuttavia ci sono delle stranezze da puntualizzare.
Tiriamo fuori il nostro asso nella manica, ovvero la ricostruzione dell’avvenimento in un modello di ischemia su animale ed analizziamo la quantità di HIF-1 in diverse aree cerebrali a diversi tempi dopo l’occlusione dell’arteria cerebrale media. Dai risultati ci renderemo conto che HIF-1 non era presente prima dell’occlusione e neanche all’inizio dell’occlusione stessa, mentre è presente per pochissimo tempo durante l’ipossia neuronale per poi sparire di nuovo improvvisamente subito dopo il ripristino del circolo sanguigno.
HIF-1 dovrebbe spiegarci molte cose al riguardo sul perché c’era, cosa ha fatto e come ha fatto ad apparire e scomparire velocemente in circostanze quantomeno sospette.
Il mago Houdinì – Apparizioni e Sparizioni
HIF-1 è un fattore trascrizionale composto da due sub-unità definite HIF-1alfa e HIF-1beta, prodotti da due geni diversi molto conservati nell’evoluzione dei mammiferi. La trascrizione e la formazione di queste due proteine sono costanti ed ubiquitari in tutto l’organismo, tuttavia con un banale western blot non è possibile vedere una buona dose di proteina nei tessuti.
Il perché è subito chiarito dal suo scopritore Gregg Semenza, che ha dimostrato come in condizioni di ossigenazione ‘normale’ HIF-1alfa è idrossilato attraverso un enzima e poi processato per la degradazione… in poche parole HIF-1alfa è continuamente prodotto ma è anche degradato subito dopo in presenza di ossigeno molecolare. Infatti, quando l’ossigeno comincia a mancare HIF-1alfa non si può più degradare e si accumula legandosi al suo cofattore HIF-1beta formando il fattore trascrizionale completo HIF-1 che va ad attivare una serie di geni target. In seguito alla riossigenazione HIF-1alfa è nuovamente degradato ed il complesso HIF-1 non si forma più.
Ecco così spiegato il mistero della sparizione ed apparizione di HIF-1 durante l’ischemia cerebrale.
Conosci gli amici che frequenti e saprai chi sei
La domanda più interessante a questo punto è “quali geni target attiva HIF-1?”. Bhé ce ne sono centinaia, e sono divisi in classi secondo il meccanismo globale a cui afferiscono.
Troviamo geni del metabolismo anaerobico del glucosio, ovvero quegli enzimi che servono per ottenere energia dal glucosio senza la necessità di ossigeno, troviamo anche geni che servono per aumentare l’ossigenazione in una certa regione del tessuto come ad esempio VEGF il fattore che induce la vascolarizzazione in loco per apportare più ossigeno e nutrienti. Tra i target c’è anche l’eritropoietina che aumenta la produzione di globuli rossi che portano l’ossigeno in tutto l’organismo.
Poi ci sono geni un po’ più strani che mirano comunque alla sopravvivenza della cellula in condizioni anaerobiche e geni di cui non si sa bene la funzione nell’ipossia.
Tutto sommato è un ‘buono’ e serve alle cellule per ‘adattarsi’ alle scarse riserve di ossigeno e soprattutto promuovere il rimodellamento dell’organismo per avere più ossigeno.
Buono?
C’è anche l’altra faccia della medaglia, come per ogni fattore trascrizionale. L’altra faccia della ‘Janus Face’ HIF-1 è che se passa ‘dall’altra parte’ favorisce la vascolarizzazione di neoplasie (tumori) rendendolo più maligno e più resistente alle terapie antineoplastiche. Non a caso le mutazioni dei geni che servono per degradare HIF-1 in presenza di ossigeno siano dei noti oncogeni, ovvero geni cruciali che favoriscono la formazione e l’accrescimento dei tumori quando non funzionano a dovere.
Cosa ci faceva HIF-1 durante l’ischemia?
 Bene dopo questa velocissima presentazione di questo angelo o diavolo è ora di chiedersi cosa stava facendo subito dopo l’occlusione dell’arteria cerebrale e proprio in quei neuroni che moriranno diverse ore dopo… Stava avvelenando il loro futuro o stava costituendo un disperato tentativo di salvataggio?
Bene dopo questa velocissima presentazione di questo angelo o diavolo è ora di chiedersi cosa stava facendo subito dopo l’occlusione dell’arteria cerebrale e proprio in quei neuroni che moriranno diverse ore dopo… Stava avvelenando il loro futuro o stava costituendo un disperato tentativo di salvataggio?
Se provate a chiedere a HIF-1 cosa stesse facendo la risposta è ovvia, stava promovendo la sintesi di geni del metabolismo anaerobico per consentire ai neuroni di far fronte all’immediata assenza di ossigeno.
Facendo una Cromatin Immunoprecipitation (ChIP), ovvero una tecnica che ci permette di determinare se un fattore trascrizionale è legato o no ad una determinata regione genomica, c’è un primo riscontro positivo, effettivamente HIF-1 si trovava nelle posizioni di attivazione dei geni che servono per il metabolismo anaerobico.
Però c’è un’incongruenza, il tempo necessario ad HIF-1 per attivare i geni del metabolismo è costituito almeno da diverse ore; ovvero il tempo necessario per aumentare la sintesi di mRNA e di proteine. HIF-1, invece, rimane legato ai geni descritti per pochissimo tempo, al massimo un’ora o anche molto meno, un tempo che non basterebbe neanche a reclutare tutti i cofattori necessari per l’attivazione della trascrizione genica… come mai?
HIF-1 si difende esponendo i propri fatti… ovvero si trovava lì al momento dell’ipossia, aveva visto che ‘la nave stava affondando nell’ipossia’ e quindi si è attivato quanto prima come da suo dovere, poi è subentrata la riossigenazione dell’area cerebrale che lui non poteva prevedere ed è stato degradato dall’ossigeno prima che potesse fare effettivamente qualcosa. Per cui in realtà si tratterebbe di un tentativo andato a vuoto.
Dall’analisi per RT-PCR, tecnica che permette di determinare l’aumento o la diminuzione dell’espressione di determinati geni, c’è una prima conferma dell’alibi di HIF-1. Effettivamente stavano aumentando, seppur di poco, la sintesi dei geni implicati nel metabolismo anaerobico, del tutto sovrapponibile con quello che ci si aspetterebbe dall’azione esplicata da HIF-1.

Innocente allora?
Prima di prosciogliere l’imputato io suggerirei di analizzare anche chi ha frequentato HIF-1 in quella notte misteriosa dove è avvenuta l’ipossia. C’erano altri geni che ha indotto HIF-1?
Un gene molto importante è VEGF come già accennato, implicato nell’induzione della vascolarizzazione a lungo termine, ma che ha anche un’azione neuroprotettiva acuta nei confronti dell’ischemia cerebrale. Poi ci sono l’eritropoietina, che serve per aumentare i globuli rossi nel sangue, anch’esso neuroprotettivo in fase acuta, e tanti altri geni più o meno noti per avere un’azione neuroprotettiva. Un eroe dunque.

Il lato oscuro di HIF-1
C’è però anche chi fa notare che i fattori trascrizionali in condizioni non fisiologiche come l’ischemia cerebrale possono frequentare anche ‘compagnie diverse’ ed insolite da quelle catalogate. Infatti, da alcuni esperimenti di Microarray, tecnica che permette di vedere l’aumento o la diminuzione dell’espressione di un ampio numero di geni in condizioni fisiologiche rispetto a quelle patologiche, è emerso che HIF-1 ha scarsamente indotto geni neuroprotettivi, come già descritto, però durante la sua attivazione sono aumentati enormemente anche tanti geni di ‘malaffare’.
Insomma tanto basta per iniziare il processo contro questo ‘strano individuo’
Che il processo abbia inizio… entri il primo imputato HIF-1
 La parola all’accusa
La parola all’accusa
Quei pochi minuti che bastano
Sebbene siano necessarie diverse ore per attivare i geni del metabolismo anaerobico, per HIF-1 sono stati necessari pochi minuti per attivare alcuni dei geni più distruttivi dell’ischemia. E non si tratta di una piccolo aumento di espressione. Il gene in questione è la nitrossido sintetasi inducibile che produce radicali liberi sottoforma di gas nitrossido con un’azione neurotossica letale per i neuroni. Da un’analisi con Decoy, ovvero la somministrazione di piccoli tratti di DNA a doppio filamento che simulano il sito di legame di HIF-1 e lo sequestrano lontano dai geni bersaglio, è stato possibile determinare con certezza che HIF-1 è il principale responsabile dell’aumento della trascrizione della iNOS. Quando ad una cellula ipossica si dà il Decoy, HIF-1 lo lega e non riesce a raggiungere il gene bersaglio, un effetto simile ad un knock-out genico. La iNOS è nota per causare la morte cellulare dei neuroni, una questione indubbia.
Ma come è possibile che ad HIF-1 bastino pochi minuti per l’attivazione di iNOS mentre sono necessarie ore per i geni neuroprotettivi? Greeg Semenza è riuscito a chiarire anche questo altro aspetto. HIF-1, infatti, è prodotto continuamente dalla cellula, ed è anche degradato continuamente, ma una piccola quota di HIF-1 è presente nelle cellule, visibile per western blot, e basta per legare ed indurre determinati geni insoliti. Talvolta li lega anche quando non c’è ipossia ed attende la mancanza di ossigeno così per trovarsi già in loco quando serve.
Insomma HIF-1 è stato visto aumentare e fomentare geni per la degenerazione neuronale, mentre i geni neuroprotettivi non erano stati trattati allo stesso modo, dando solo un’apparenza di eroe salvatore.
A carico di HIF-1 c’è anche la precisione di espressione proprio nei neuroni e nei luoghi dove ci sarà, diverse ore la sua scomparsa, la maggior percentuale di neuroni morti. Una coincidenza forse?
Insomma, la situazione si è messa male per HIF-1, le prove vanno decisamente contro; il legame degli enzimi metabolici e neuroprotettivi potrebbe essere solo una copertura per il vero scopo, ovvero la degenerazione dei neuroni?
La parola alla difesa
 La difesa tira fuori il dogma scientifico
La difesa tira fuori il dogma scientifico
Il Dogma scientifico
Per chi non lo sapesse, esiste un dogma per ogni disciplina culturale umana e la biologia non ne è immune. Il Dogma dei biologi è che niente succede a caso, poiché per ogni gene o proteina ci sono milioni di anni di evoluzione che raffina tutti i meccanismi a quelli fondamentali per la sopravvivenza e per l’evoluzione. Se ci fosse qualcosa di inutile o peggiorativo sarebbe eliminato automaticamente dall’evoluzione stessa. Per cui la selezione e la conservazione di un fattore indotto dall’ipossia che causi morte nei neuroni non è credibile poiché non darebbe un vantaggio per la sopravvivenza.
Dopotutto quello che si vede è una sommatoria di tantissimi meccanismi che interagiscono tra di loro e quello che si osserva è solo la summa del tutto da cui è difficile estrapolare un singolo messaggio. Meglio ricorrere all’incidente probatorio…
Ovvero spegniamo HIF-1 con un knock-out genico ed induciamo l’ischemia, verifichiamo in questo caso se l’animale che manca di questo fattore è più o meno esposto al danno neuronale rispetto agli animali wild-type.
L’incidente probatorio o la prova del nove
La prova più importante seguita da quella definitiva molto spesso è la generazione di un topo knock-out per il gene di interesse. Ci sono stati tantissimi esempi di questo tipo, vale sia come inizio di una ricerca per capire grossolanamente un gene di cosa sia responsabile e vale anche come prova raffinata per avere la prova definitiva che un determinato gene sia coinvolto in un certo meccanismo.
Purtroppo nonostante intensi sforzi per ottenere topi knock-out per HIF-1alfa, è emerso che un animale privato di questo gene non riesce a svilupparsi ed a sopravvivere ai primi stadi embrionali, anche se è esposto ad un normale livello di ossigenazione. Ovviamente questo è stato il motivo dei ritardi nel fare un topo transgenico e quindi definire una prova evidente del suo ruolo in tanti processi fisiologici e patologici.
Tuttavia, recentemente è stato possibile generare un topo con un knock-out tessuto specifico di HIF-1alfa per i neuroni, il risultato è stato quantomeno sorprendente… l’assenza di HIF-1alfa durante l’ischemia cerebrale ha enormemente potenziato i danni neuronali.
Un fulmine a ciel sereno per tutti… L’imputato è senza dubbio da scagionare e da mettere tra i difensori cellulari.
Conclusioni
In questo capitolo abbiamo visto un esempio di imputato eccellente dell’ischemia cerebrale che ancora oggi per alcuni gruppi di ricerca rappresenta ancora il centro dell’attenzione. Gli studi andranno sicuramente avanti, anche se non ci si aspetterebbe ancora molto da quanto descritto, HIF-1alfa nel processo dell’ischemia cerebrale si potrebbe definire almeno non pericoloso tanto quanto altri imputati eccellenti che vedremo nelle prossime puntate. Per questi motivi l’attenzione su questo fattore trascrizionale si è concentrato soprattutto sulle neoplasie, ed ha tralasciato progressivamente l’ischemia cerebrale, renale e cardiaca. Vedremo se qualcuno in futuro troverà qualche prova rilevante per riaprire nuovamente il processo. In attesa di tale data ci rivedremo nella prossima puntata dove vedremo un altro imputato importante.
Tags: fattori trascrizionali, HIF-1, HIF-1alfa, Ictus, Ischemia Cerebrale, Mente, Neuroscienze
17 dicembre 2008 - 9:55 pm
La ricostruzione della scena del crimine
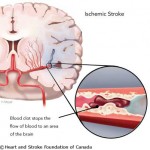 Allora, per chi non avesse seguito le puntate precedenti, abbiamo introdotto un giallo misterioso dove delle cellule del cervello umano muoiono improvvisamente in seguito ad ischemia cerebrale (icutus), mentre noi siamo la polizia scientifica molecolare nominati per cercare di spiegare cosa sia accaduto in quegli istanti e determinare chi ha causato la morte neuronale.
Allora, per chi non avesse seguito le puntate precedenti, abbiamo introdotto un giallo misterioso dove delle cellule del cervello umano muoiono improvvisamente in seguito ad ischemia cerebrale (icutus), mentre noi siamo la polizia scientifica molecolare nominati per cercare di spiegare cosa sia accaduto in quegli istanti e determinare chi ha causato la morte neuronale.
Per chi non avesse seguito le parti precedenti dia uno sguardo ad i seguenti links Ischemia Cerebrale (Parte I) Ischemia Cerebrale (Parte II)
Fino ad ora il nostro taccuino è quasi vuoto, sappiamo ancora poco e ci sono ancora tante cose da analizzare. Se fossimo degli zelanti ispettori, una delle prime cose da fare potrebbe essere ricostruire le ultime ore delle vittime per capire chi poteva trovarsi là al momento del delitto. In questo caso potremmo usare dei modelli cellulari (in vitro) o animali (in vivo) per riprodurre quello che succede nell’ictus umano. La scelta del modello non è banale, anzi è fondamentale per poter chiarire qualcosa. In genere si hanno due strade davanti ed in base a questa scelta dipenderà il livello di difficoltà che si dovrà affrontare.
La prima strada è la scelta di modelli cellulari (in vitro) che danno dei dati semplicemente misurabili ed abbastanza riproducibili; tutto sommato è un sistema semplicissimo da affrontare, ma d’altra parte ci accorgeremo presto che questi modelli sono un’eccessiva semplificazione di quello che avviene nell’uomo e che quindi ci sono anche delle notevoli limitazioni.
La seconda strada, invece, è la scelta di un modello animale (in vivo) che riproduce con molta fedeltà quello che avviene sull’uomo, ma è difficile da capire ed analizzare in tutti i suoi dettagli, proprio perché più simili al danno umano.
Ci sarebbe anche una terza strada definita ex vivo oppure colture organo tipiche, in cui si coltivano interi tessuti o parti di organi prelevati dall’animale vivo per avere una maggiore complessità rispetto alle semplici cellule, ma un vantaggio di semplificazione rispetto all’animale intero.
Le ultime ore delle vittime
Quello che si fa è prendere un certo numero di animali, ad esempio topi o ratti, ed indurre in questi l’ictus attraverso l’occlusione di una arteria cerebrale importante. Ogni animale potrebbe essere analizzato in tempi diversi così da ricostruire gli eventi che seguono l’occlusione sanguigna e precedono il danno finale.
I risultati sono interessanti, poiché è subito evidente che non tutte le cellule neuronali muoiono contemporaneamente; il volume ischemico si espande da una zona più vicina all’occlusione sanguigna fino ad arrivare ad un massimo di espansione a circa 24 ore dal danno. In ogni momento potremmo riconoscere una zona prevalentemente necrotica con poche cellule vive (core ischemico) ed una zona circostante in sofferenza che diverrà ben presto anch’essa morta (penombra ischemica).
L’onda killer
 Se dovessimo ricostruire cosa accade negli ultimi istanti di queste cellule, ci potremmo accorgere che le cellule della penombra moriranno entro qualche ora non riescono a gestire i flussi di calcio citosolico (vedi primo post). Il calcio si accumula nelle cellule poiché queste non hanno energia a sufficienza per pomparlo fuori; di conseguenza le cellule sono più facilmente eccitabili e possono attivarsi anche in momenti non opportuni, liberando neurotrasmettitori che eccitano altre cellule come un’onda di scariche elettriche longitudinali che si propagano dal centro dell’ischemia fino alla periferia del cervello. Proprio in questi momenti, ovvero poco prima della morte cellulare, si possono avere dei corto circuiti neuronali e l’avvio di sistemi di ripristino di emergenza nella metà cerebrale colpita. Questi corto circuiti generano i classici segni premonitori che si possono riassumere nell’acronimo inglese FAST
Se dovessimo ricostruire cosa accade negli ultimi istanti di queste cellule, ci potremmo accorgere che le cellule della penombra moriranno entro qualche ora non riescono a gestire i flussi di calcio citosolico (vedi primo post). Il calcio si accumula nelle cellule poiché queste non hanno energia a sufficienza per pomparlo fuori; di conseguenza le cellule sono più facilmente eccitabili e possono attivarsi anche in momenti non opportuni, liberando neurotrasmettitori che eccitano altre cellule come un’onda di scariche elettriche longitudinali che si propagano dal centro dell’ischemia fino alla periferia del cervello. Proprio in questi momenti, ovvero poco prima della morte cellulare, si possono avere dei corto circuiti neuronali e l’avvio di sistemi di ripristino di emergenza nella metà cerebrale colpita. Questi corto circuiti generano i classici segni premonitori che si possono riassumere nell’acronimo inglese FAST
- Faccia asimmetrica (ad es. una palpebra più bassa, o una bocca storta): ciascuna metà del nostro organismo è gestita da una metà cerebrale, se in una di queste ultime avvengono corto circuiti oppure entrano in funzione sistemi di emergenza, la faccia o il corpo può avere un’asimmetria.
- Arti asimmetrici: si sollevano entrambe le braccia con i palmi rivolti verso l’alto, poi si chiudono gli occhi e si mantiene questa posizione per qualche secondo, nell’ictus un braccio tende a scendere per lo stesso motivo precedente
- Suoni confusi o distorti: Se le scariche elettriche colpiscono il centro del linguaggio, il paziente potrebbe essere colto da afasia con emissione di parole confuse, suoni distorti o potrebbe pensare di parlare correttamente mentre farfuglia parole a caso.
- Tempo: se si notano anche uno solo dei sintomi precedenti non bisogna esitare, una cura tempestiva è fondamentale per una buona riuscita della terapia.
Questi sintomi, infatti, compaiono ben prima che avvenga la morte dei neuroni, quindi sono ancora del tutto reversibili se si riesce a ripristinare la circolazione cerebrale.
Il paziente potrebbe anche avere all’improvviso
- debolezza o insensibilità o comparsa di formicolii a una metà del volto, a un braccio o a una gamba oppure a tutta la metà del corpo
- oscuramento o perdita della visione da un solo occhio
- incapacità di esprimersi o di comprendere qualcuno che parla
- inspiegabile sensazione di vertigine, capogiro, sbandamento o cadute improvvise
- grave e inspiegabile mal di testa.
Se questi sintomi scompaiono entro 24 ore, al paziente verrà detto che ha avuto un Transient Ischemic Attack (TIA), cioè un attacco ischemico transitorio, in pratica un ictus minore, dovuto a una occlusione solo transitoria di un vaso arterioso.
Primo intervento
Se il paziente colpito da icuts ha la fortuna avere vicino qualcuno che sa riconoscere i sintomi e riesce a portarlo in pronto soccorso entro le 3 ore dall’occlusione dell’arteria cerebrale, allora i medici potrebbero somministrare al paziente del tPA, ovvero l’attivatore tissutale del plasminogeno, in grado di degradare il trombo che ha occluso un’arteria e ridare ossigeno alle cellule neuronali prima che sia troppo tardi. Altra alternativa altrettanto valida è inserire un palloncino nell’arteria occlusa per gonfiarlo nell’ostruzione e liberare il circolo sanguigno.
Quando invece è già troppo tardi succede un qualcosa di irreversibile o quasi. Questo impercettibile punto di non ritorno che avviene dopo le prime 3 ore nell’uomo e ben prima che incominci la morte neuronale è l’oggetto della nostra contesa.
Fino ad oggi, infatti, non esistono metodologie che riescano in qualche modo ad identificare il perché le cellule neuronali muoiano anche se ricevono ossigeno, metaboliti e sostanze trofiche, e non si riesce a capire neanche quanto sarà esteso il danno, quali cellule moriranno e soprattutto quale zone saranno interessate. Ai familiari del paziente, infatti, verrà detto che bisognerà aspettare 1-2 giorni per capire quanto esteso è il danno e quali zone del cervello interesserà.
Questo aspetto è il punto cruciale, in queste ore che precedono il danno le cellule sono vive e ci servirebbe capire perché muoiono per poi cercare disperatamente un metodo per bloccare tale procedura apparentemente irreversibile.
Analisi della scena del crimine
 Un ispettore che si trova in una scena del crimine molto complessa come quella descritta e che ha sentito la ricostruzione del danno analizzerebbe sicuramente tutta una batteria di proteine e di mRNA per capire costa stavano facendo i neuroni in quei momenti. Questa analisi ovviamente può essere fatta da una ipotetica polizia scientifica utilizzando, ad esempio, la metodica dei microarray.
Un ispettore che si trova in una scena del crimine molto complessa come quella descritta e che ha sentito la ricostruzione del danno analizzerebbe sicuramente tutta una batteria di proteine e di mRNA per capire costa stavano facendo i neuroni in quei momenti. Questa analisi ovviamente può essere fatta da una ipotetica polizia scientifica utilizzando, ad esempio, la metodica dei microarray.
I microarray sono dei piccoli chips della grandezza della punta del nostro indice con cui è possibile valutare l’aumento o la diminuzione dell’espressione dell’mRNA di tantissimi geni contemporaneamente attraverso l’uso di un estratto di RNA da un controllo ed un estratto di RNA da un trattato.
Per chi non conosce i chips può leggere qui Microarray – Wikipedia
Tecnicamente questa metodica ci consente di guardare sommariamente tra i nostri 30.000 geni, quali sono aumentati o diminuiti in seguito ad un determinato stimolo, farmaco, malattia etc etc.
Questa metodica, infatti, si addice benissimo ad avere una visione globale del problema per incominciare un percorso di indagine sui responsabili della patologia.
Noi potremmo utilizzare questa metodica per analizzare zone analoghe del cervello in un animale ischemico e confrontarlo con un animale shame-operated, ovvero un animale che ha ricevuto una procedura chirurgica simile ma che non ha avuto l’occlusione di un arteria. Questo è importante poiché dobbiamo evitare alcune interferenze dovute allo stress operatorio, ad eventuali infiammazioni o infezioni. Dall’analisi emerge che sono variati almeno 7.000 geni.
Abbiamo quindi 7.000 testimoni o potenziali imputati da valutare con attenzione singolarmente o in gruppo nel processo che si sta aprendo, a cui si dovrebbero aggiungere anche altri imputati eccellenti che non possono essere valutati con i microarray, ad esempio neurotrasmettitori, sostanze endogene, ioni, meccanismi post-traduzionali (su proteine) che possono alterare l’espressione di una proteina, e la sua funzione senza interferire in alcun modo sulla sua espressione.
Conclusione
In questo ultimo post introduttivo abbiamo presentato un piccolo bagliore della difficoltà di questo lungo ed inesauribile processo verso ignoti che causano ogni anno una invalidità più o meno grave fino alla morte di tantissime persone nei paesi industrializzati. Per utilizzare un termine moderno si potrebbe parlare di un maxi-processo in cui gli imputati sono tra loro correlate con gerarchie complesse. Come già accennato, gli imputati sono in realtà numericamente molti di più di 7.000, ma fortunatamente non li prenderemo in considerazione tutti nel nostro blog; vedremo solo alcuni personaggi perché interessanti, ambigui, fortemente sospettati, antipatici, schivi o semplicemente perché si trovava lì al momento del delitto.
Alla prossima puntata.
Tags:
Ictus,
Ischemia Cerebrale,
Microarray,
mRNA,
Neuroni
14 settembre 2008 - 3:50 pm
Preambolo
Allora, rieccoci qui dopo le tanto meritate vacanze. Ringrazio tutti quelli che hanno contribuito con commenti, domande e quant’altro al primo capitolo di questa serie, spero che ce ne siano sempre di più, comprese critiche e puntualizzazioni; accetto persino complimenti.
Nel capitolo precedente abbiamo visto un po’ in generale alcune caratteristiche dell’ictus ed abbiamo introdotto il concetto del calcio come strumento di informazione e distruzione cellulare. Ora, in questo capitolo ci concentreremo maggiormente sulla morte neuronale, trattando il tutto come il più classico dei gialli dove le vittime sono i neuroni, la scena del crimine è il cervello dopo l’ictus e dovremo cercare l’assassino capitolo dopo capitolo, strato dopo strato, mettendo sul banco degli imputati diversi “personaggi ambigui” in cerca del vero colpevole. Di volta in volta saranno presentati nuovi personaggi con nuove “verità” e quindi nuove “teorie”. Ovviamente non mancheranno i colpi di scena come nel più classico dei thriller da leggere la sera a letto prima di dormire.
Data l’importanza dei rudimenti medici che stiamo trattando e dell’interesse mostrato in alcuni commenti ho deciso di aggiungere un piccolo paragrafo di chiarimenti e risposte ai commenti nel post precedente. Per chi si annoia a leggere le osservazioni fatte o per chi sa già questi concetti consiglio di saltare il prossimo paragrafo e passare direttamente al paragrafo sulla morte cellulare che spero sia per loro più interessante.
Il Calcio presente nel nostro organismo

Il calcio (simbolo: Ca2+) in una persona di sesso maschile magro rappresenta circa l’1,5% del peso corporeo, per una persona di 70 kg ce n’è circa 1 kg. Sicuramente è lo ione più abbondante del nostro organismo, seguito dal potassio (simbolo: K+) con soli 240 grammi e poi dal sodio (simbolo: Na+) con 100 grammi. Il 99% del calcio del nostro organismo è presente nelle ossa e nei denti, lo 0,5% è conservato avidamente in particolari compartimenti subcellulari come il reticolo endoplasmatico, insieme a proteine chelanti e mitocondri, come già descritto da Massi-Demish. Solo lo 0,3-0,4% del peso corporeo, circa 0,21 grammi, corrisponde al calcio che è libero di circolare nel nostro organismo e che partecipa a quei meccanismi di cui abbiamo parlato nel post precedente. Per dare un’idea, basti pensare che una mozzarella da 100 grammi contiene 0,4 grammi di calcio, ovvero una quantità doppia rispetto a tutto il calcio libero che è presente nel nostro organismo. Cosa succede se si assume una quantità di calcio superiore alle necessità dell’organismo? quasi sempre alcune cellule specializzate lo depositato nelle ossa oppure lo elimina attraverso le urine. Nei rari casi in cui c’è una carenza di calcio dalla dieta, invece, altre cellule specializzate corrodono meno di un millimetro cubo di ossa (quasi niente) per avere mesi di autonomia da calcio allo stato libero utile per i neuroni e tutte le altre funzioni cellulari descritte. Le nostre ossa sono infatti continuamente corrose e rimodellate in funzione del nostro lavoro fisico, delle trazioni, dai livelli ormonali e tante altre cose, di conseguenza l’organismo può sempre bilanciare l’eccesso o la carenza di calcio libero nei nostri fluidi corporei depositandolo o prelevandolo dalle ossa. Da questo si deduce che la quantità di calcio assunto per via orale di per sé non ha alcuna interferenza sulla quantità di calcio libero nel nostro organismo e di conseguenza non ha alcun effetto neanche sul danno ischemico.
Anche se si considerano i rari casi in cui delle persone, per qualche motivo, hanno una dieta cronica quasi del tutto priva di calcio e che quindi necessitano una integrazione, i livello di calcio libero sono più o meno simili alla media standard. A questi pazienti, però, può essere consigliato l’assunzione di pillole contenenti calcio oppure assumere qualche bicchiere di latte, pezzi di formaggio, carne, acqua del rubinetto per poter ripristinare le riserve di calcio nelle ossa ed evitare spiacevoli facili fratture.
C’è da dire anche che esistono, con una maggiore frequenza, delle persone che hanno carenze di calcio perché non lo riescono ad assumere dal cibo o lo elimina troppo velocemente, come nel caso dell’osteoporosi da menopausa. In questi casi si prescrivono farmaci composti da ormoni che predispongono l’organismo ad accumulare calcio nelle ossa anziché eliminarlo, senza la necessità di variare in alcun modo la dieta. Proprio questi ormoni influiscono sull’ischemia cerebrale, ma per meccanismi che non hanno nulla a che fare con la quantità di calcio ingerito, se volete posso aggiungere un capitolo apposito per questo curioso argomento.
Come può morire una cellula?

Allora, ora prendiamoci una pausa ed immaginiamo per un attimo di trovarci in un insolito thriller e di essere chiamati nel cuore della notte per investigare su un misterioso assassinio di massa. Una volta arrivati sulla scena del delitto, ovvero il cervello ischemico, ci ritroveremmo sicuramente ad analizzare come si presentano le vittime neuronali. Però c’è un problema, anche se fino ad ora abbiamo parlato intuitivamente di morte cellulare, non sappiamo ancora come può morire una cellula e di conseguenza come può presentarsi agli occhi di una insolita polizia scientifica molecolare. Questo è un punto fondamentale poiché ci aiuta a capire meglio la filosofia e la strada che stiamo percorrendo.
Attualmente si classifica la morte cellulare in due tipologie principali:
- Necrosi: generalmente è il risultato di un acuto stress o trauma che porta alla rottura della membrana cellulare con perdita del materiale biologico in esso contenuto. In questo caso la cellula si presenta in maniera inconsistente e quasi irriconoscibile poiché tutti gli organelli di cui è composta si disperdono nella soluzione in cui è immersa la cellula morta, rendendo spesso i resti irriconoscibili.
- Apoptosi: si tratta di un processo di morte molto ordinato in cui è la stessa cellula a decidere come e quando morire, e lo fa in modo tale da non dare alcuna tossicità alle cellule circostanti. La cellula si presenta come piccole vescicole ricoperte di membrana e con dei segnali sulla membrana cellulare (epitopi) che indicano “qui c’è materiale riciclabile”.
La necrosi, quindi, è insieme di morti cellulari “accidentali” senza avere un comune denominatore se non la rottura irreversibile della membrana che avvolge le cellule e di conseguenza la dispersione del materiale in esso contenuto. Proprio la perdita di materiale ed il disordine caratteristico di questo tipo di morte può causare infiammazione o tossicità alle cellule circostanti. Sicuramente la necrosi non è un fenomeno che l’organismo e le cellule stesse apprezzano o considerano come destino. L’apoptosi invece è una forma di morte cellulare molto precisa, portata avanti in modo ordinato e regolato, che dà un vantaggio alla popolazione cellulare circostante durante il ciclo vitale dell’organismo. Si tratta in realtà di un vero e proprio “suicidio cellulare” che necessita di tante proteine dedicate che svolgono un complesso e delicato meccanismo a tappe con un preciso schema prestabilito e con consumo di energia. In condizioni normali, l’apoptosi avviene continuamente perché contribuisce al mantenimento del numero di cellule di un sistema; avviene ad esempio in un seno che si ritira dopo la fase di allattamento dove ci sono migliaia di cellule che si “sacrificano” perché sono di troppo o non più necessarie, lo stesso vale per l’utero dopo una gravidanza etc. Ovviamente la mancata regolazione dell’apoptosi può causare disordini da perdita di cellule, caratteristica di molte patologie neurodegenerative, oppure una crescita cellulare incontrollata che è alla base delle neoplasie (tumori).
L’apoptosi, a differenza della necrosi, non causa infiammazione e la morte delle cellule mediante questo processo provoca la formazione di vescicole con un contenuto prestabilito di sostanze che possono essere riciclate da cellule specializzate. Dato che non c’è la rottura della membrana cellulare e che tutte le cellule del nostro organismo conoscono questo processo, l’apoptosi è un processo silenzioso che non fa danno.
L’infarto cerebrale: La scena del crimine
 Seguendo la storia sulla falsa riga del “giallo”, la prima domanda è come sono morte le cellule? Hanno eseguito un suicidio di massa (apoptosi) oppure sono morte per trauma (necrosi)?
Seguendo la storia sulla falsa riga del “giallo”, la prima domanda è come sono morte le cellule? Hanno eseguito un suicidio di massa (apoptosi) oppure sono morte per trauma (necrosi)?
I ricercatori con un po’ di esperienza sanno bene che un fenomeno di morte in massa è attribuibile solamente alla necrosi, l’apoptosi, infatti, è un fenomeno prevalentemente sporadico, ciò vuol dire che l’apoptosi in natura colpisce poche cellule alla volta e la loro scomparsa è quasi sempre impercettibile, mentre la necrosi è una morte cellulare a cascata, ogni cellula muore poiché si trova vicino una cellula in decomposizione ed è tipico della gangrena, dove si deve amputare un arto per frenare la morte a cascata che potrebbe propagarsi sul corpo del paziente e causarne la morte.
Possiamo essere sicuri che si tratti di necrosi?
Non esistono saggi specifici per la necrosi, ma per esserne sicuri potremmo usare sul cervello ischemico un anticorpo che riconosca selettivamente dei cartelli che indicano “qui c’è materiale apoptotico riciclabile” (epitopo). Se lo facessimo il risultato sarebbe deludente, il segnale apoptotico è molto scarso, l’apoptosi è avvenuta solamente su una piccola percentuale di cellule. E poi basta guardare come si presenta il materiale ischemico; si tratta di una zona amorfa in cui non è possibile riconoscere strutture macroscopiche e microscopiche, tranne alcune cellule resistenti che sopravvivono, e questo ci indica inevitabilmente che si tratta di una massa in necrosi… omicidio quindi.
Se si fosse trattato di una apoptosi di massa?
Se si fosse trattato di apoptosi (suicidio) ci saremmo aspettati qualche cellula qua e là morta con le classiche vescicolette, epitopo dell’apoptosi, assenza di infiammazione e sarebbe stato difficile identificarlo poiché silente.
Le cellule del nostro cervello
 L’investigazione quindi è tutta in salita, non possiamo trarre molte informazioni dal ritrovamento delle vittime se non che siano state uccise da un evento molto traumatico avvenuto diverse ore dopo il ristabilirsi delle condizioni ottimali di circolazione sanguigna (vedi post precedente).
L’investigazione quindi è tutta in salita, non possiamo trarre molte informazioni dal ritrovamento delle vittime se non che siano state uccise da un evento molto traumatico avvenuto diverse ore dopo il ristabilirsi delle condizioni ottimali di circolazione sanguigna (vedi post precedente).
Passiamo quindi alla raccolta delle informazioni sulle vittime nella loro vita quotidiana per poi passare alle indagini vere e proprie sull’assassino. Le vittime di questa storia sono ovviamente le cellule che partecipano alla struttura e funzione del cervello e non stiamo parlando solamente di neuroni. Il cervello, infatti, è costituito da centinaia di tipologie cellulari con ruoli distinti e diversamente collegati a tutte le altre cellule circostanti. Nel cervello abbiamo i neuroni che generano i nostri pensieri, che stimolano i muscoli a contrarsi e che generano anche ormoni che modificano il nostro stato fisico e psitico; poi abbiamo le cellule gliali, una famiglia di cellule nutrici per i neuroni che coccolano, proteggono, danno da mangiare e sostengono le cellule neuronali nel loro faticoso ruolo.
Le cellule gliali: Profilo di una serie di badanti ideali
Le cellule gliali sono suddivise in centinaia di ruoli distinti, dai più elementari ai più complessi, e sono anche le uniche cellule del cervello in grado di riprodursi, contrariamente ai neuroni. Proprio questa caratteristica è la prima distinzione tra le due popolazioni, mentre le cellule gliali possono moltiplicarsi e quindi invadere le zone morte in seguito ad un trauma, i neuroni possono solo diminuire il loro numero durante la nostra vita e mai aumentare. Pensate che il numero di cellule della glia in un cervello umano normale supera di nove volte quello dei neuroni, e proprio da questo è nato il falso mito che noi utilizziamo solamente il 10% del nostro cervello per pensare.
Alcune cellule della glia agiscono principalmente da supporto ai neuroni, altre regolano l’ambiente interno del cervello in particolare i fluidi che circondano i neuroni e le loro sinapsi provvedendo quindi al nutrimento delle cellule nervose. Alcuni tipi di cellule della glia producono molecole in grado di influenzare la crescita degli assoni. Altre funzioni sono state scoperte solo recentemente come la possibilità di comunicare con altre cellule.
La principale suddivisione della glia del cervello prevede due categorie principali:
Microglia: cellule specializzate nel mangiare e riciclare i rifiuti, come le cellule apoptotiche e gli agenti che disturbano la quiete del cervello. In genere si spostano all’interno del nostro cervello per rimuovere i corpi apoptotici e per controllare che tutto funzioni bene. In condizioni fisiologiche la microglia è presente solo in piccolo numero ma si moltiplicano in caso di danni neuronali.
Macroglia: una serie di cellule diverse, tra cui astrociti, oligodendrociti, cellule ependimali, glia radiale. I ruoli sono i più diversi tra loro e tutti hanno il comune denominatore di aiutare i neuroni a vivere in un ambiente ideale.
Bhé sicuramente se stiamo cercando un assassino non si troverà tra le vittime, tantomeno nella glia deputata a coccolare e proteggere i neuroni.
Neuroni: profilo di una vittima ideale

Anche i neuroni sono suddivisi in centinaia di sottotipi cellulari, ognuna con funzioni diverse e specifiche, ma tutti i neuroni hanno caratteristiche molto simili tra loro, tanto che possiamo accomunarli tutti in una sola descrizione generale.
I neuroni sono delle vittime ideali, poiché a differenza di tutte le cellule delle nostro organismo non si replicano mai, necessitano di molte cure e basta poco per ucciderle. Tutte le cellule del nostro organismo, infatti, possiedono delle riserve energetiche che sono utili in caso di prolungata assenza di nutrimenti, alcune cellule possono anche adattarsi a metabolizzare sostanze di diversa natura per sopravvivere ed altre ancora si adattano anche alla scarsa presenza di ossigeno. Purtroppo i neuroni fanno eccezione, non hanno riserve energetiche e si nutrono solamente di zucchero raffinato. Quel che è peggio è che non sanno adattarsi diversamente e che basta anche una carenza di ossigeno, sangue o alcune stimolazioni per innescarne la morte.
La vita di un neurone, inoltre, non è per niente facile, la sua membrana plasmatica è simile ad una batteria con una differenza di potenziale, espressa in milliVolt, che cambia in funzione dello stato cellulare, canali che fanno entrare ed uscire ioni modificando continuamente lo stato d’ordine cellulare mentre una serie di pompe ioniche cercano continuamente di ripristinare l’ordine con una certa fatica.
Tutti i neuroni sono poi interconnessi tra loro con una fitta rete di cavi elettrici (assoni e dendriti) che propagano o captano variazioni delle differenze di potenziale di membrana che viaggiano lungo un neurone, tra un neurone e l’altro e da un lato del cervello ad un altro.
Questi processi sono continui anche durante il sonno, durante la vita intrauterina e nel coma.
Se ne deduce che ognuno dei circa 100 miliardi di neuroni che abbiamo alla nascita è continuamente sull’orlo di un baratro con attività che lo spingono a fare cose eccezionali in frazioni di secondo, e tantissime proteine che devono continuamente ripristinare lo stato d’ordine in altrettanti frazioni di secondo con un poderoso dispendio di energia. Pensate che circa il 20% dell’energia che mangiamo, e che serve per farci stare in uno stato “normale”, serve semplicemente per far funzionare il cervello che rappresenta solo il 2% del peso corporeo; un’altra buona quota serve per mantenere ordine nel resto dell’organismo 98% del peso corporeo e solo una frazione piccola è necessaria per l’attività fisica che facciamo.
Conclusioni
In questo lunghissimo post abbiamo introdotto meglio alcuni concetti fondamentali che ci serviranno nei prossimi capitoli dove, se vorrete, cercheremo di prendere in considerazione alcune teorie su cosa sia avvenuto negli ultimi istanti di vita delle vittime, chi era presente al momento della morte, al momento del ritrovamento e soprattutto chi sia stato l’esecutore materiale di questo misterioso delitto, da dove proviene e come potremmo impedire che questo accada.
Tags:
Apoptosi,
Calcio,
Glia,
Ictus,
Ischemia Cerebrale,
Necrosi,
Neuroni
10 agosto 2008 - 8:15 pm
Rieccoci qua dopo un po’ di tempo di “meditazione lavorativa”, spero di recuperare i post di Nico, poiché sto un po’ indietro.
Allora, per ricominciare vorrei trattare un argomento che ha anche un importante risvolto filosofico che spero possa interessare anche ai “non addetti ai lavori”. Dovete sapere che quando ho iniziato a scrivere l’argomento qui di seguito ho scritto talmente tanto che mi sono subito reso conto che potrebbe essere un po’ troppo lungo e barboso per essere digerito in una sola volta. Di conseguenza ho deciso di farne un argomento a brevi “puntate”, spero che questo sistema vi sarà gradito maggiormente.
Se vi sono commenti vi prego di farmene partecipe.
Buona lettura
Pasquale

Per introdurre questo lungo argomento definirò prima il termine “ischemia“. La parola deriva dal Greco ισχαιμία, ovvero isch (riduzione) ed haima (sangue) e sottintende un apporto di sangue insufficiente per soddisfare le richieste energetiche di un determinato distretto dell’organismo. Ovviamente, la mancanza di nutrienti e di ossigeno porta prima alla sofferenza cellulare e poi, se è prolungata, determina la morte dei tessuti circostanti. L’estensione, inteso come volume, e l’entità del danno, inteso come percentuale di cellule morte, dipendono dal tipo cellulare coinvolto e dalla differenza tra la richiesta energetica e l’energia effettivamente fornita.
Il termine ischemia è riferibile a qualsiasi zona dell’organismo; per cui si può parlare di ischemia cardiaca, renale, muscolare, cerebrale etc. Ognuno di questi organi ha caratteristiche diverse, e di conseguenza sono più o meno sensibili al danno ischemico.
Con il termine ictus (dal latino “colpo”) si intende specificamente l’ischemia che riguarda il cervello. Questa patologia è la prima causa di invalidità permanente e la terza causa di morte nei Paesi industrializzati. I recenti progressi medico-scientifici hanno portato a dei miglioramenti nella gestione dei pazienti ischemici come la diagnosi precoce, la trombolisi, la creazione di centri per lo stroke e la riabilitazione. Tuttavia, l’ictus oggi rappresenta ancora un problema medico senza un’efficace terapia. Stranamente, nonostante i numerosi studi sull’argomento in questione l’ischemia cerebrale è ancora una patologia con molti lati oscuri da chiarire.
L’ictus, infatti, presenta diverse caratteristiche anomale che lo contraddistinguano dagli altri tipi di ischemia. La caratteristica più evidente è che la morte dei neuroni non avviene quando c’è la carenza di carburante ed ossigeno, ma diverse ore fino a giorni dopo il ristabilirsi del normale flusso sanguigno. Si può affermare quindi che la morte neuronale non è causata direttamente della semplice mancanza di cibo ed ossigeno, ma per complessi meccanismi che sono scaturiti da questa mancanza. Questa caratteristica rende l’ischemia cerebrale una sezione medica di notevole interesse scientifico poiché è una patologia molto grave e diffusa, con un periodo di possibile intervento (finestra terapeutica) abbastanza ampia. Il tempo che intercorre tra l’ictus ed il raggiungimento del massimo danno cerebrale è abbastanza lungo per un tempestivo intervento farmacologico sul paziente. Purtroppo le attuali terapie mirano a fenomeni macroscopici come ripristinare il flusso sanguigno mediante agenti anticoagulanti che rompono il coagulo che ha occluso un’arteria. Queste terapie sono utili solo se sono effettuate entro 2-3 ore dall’inizio dei sintomi ed hanno scarsa efficacia. Secondo molti la “vera terapia” dovrebbe mirare a bloccare quei sistemi cellulari che portano una determinata cellula, apparentemente non sofferente, a morire dopo giorni dall’evento ischemico. Per questo motivo è in corso da tempo la caratterizzazione di questi complicati meccanismi cellulari per la ricerca di efficaci bersagli farmacologici che siano in grado fermare questo percorso neurodegenerativo ritardato. Sin dai primi risultati delle ricerche svolte è emerso che uno dei punti chiave della neurodegenearazione è lo ione calcio e la fine regolazione delle sue concentrazioni intracellulari ed extracellulari.
Il Calcio: la “Spada di Damocle” dell’ischemia

Il Calcio (Ca2+) è un componente essenziale per la vita; questo ione infatti oltre ad essere un componente fondamentale per le ossa, è usato anche come un importante segnale cellulare per innescare migliaia di processi fisiologici che vanno dalla contrazione cellulare, come nel caso delle cellule cardiache e muscolari, fino all’impulso nervoso di ogni singolo neurone del cervello.
Pensate che la concentrazione di calcio presente all’interno di una qualsiasi cellula del nostro organismo a riposo è estremamente bassa (50-100 nanoMolare), praticamente meno della concentrazione di calcio che si ha nella semplice acqua distillata! All’esterno delle cellule, invece, c’è una concentrazione di calcio di circa 10.000 volte superiore che è separata dall’interno delle cellule da un doppio strato lipidico sottilissimo. Questa differenza di concentrazione è fondamentale, poiché basta anche un lieve incremento dei livelli di calcio intracellulari per innescare in base al tipo di cellule interessate: l’apertura di canali, fusioni di vescicole, contrazioni cellulari, depolarizzazioni nervose, rilascio di neurotrasmettitori e/o ormoni. Una cellula neuronale, durante la sia attività, può passare per brevi istanti da concentrazioni di calcio di 50-100 nanoMolare fino a 1 milliMolare (1.000 volte di più) per poi ritornare ai livelli basali e prepararsi per essere stimolata nuovamente.
Potete immaginare che mantenere bassa la concentrazione di calcio all’interno delle cellule richiede molti sforzi energetici che consumano ATP, la molecola che conserva l’energia cellulare. Immaginate ora cosa può accadere quando manca il sangue in un determinato distretto del cervello; la mancanza di ossigeno e nutrimenti non consentirebbero alle cellule di produrre energia sottoforma di ATP e di conseguenza comincerebbero ad essere meno efficienti tutti i meccanismi che servono a mantenere basse le concentrazioni cellulari di Calcio. In definitiva, durante l’ischemia, i neuroni non riescono più a cacciare fuori il calcio che entra durante la propria attività, di conseguenza anche le funzioni fondamentali sono compromesse ed inizia la lunga agonia che porterà alla morte cellulare.
Il Calcio, quindi, è una spada di Damocle che pende su tutte le cellule che ne fanno uso; l’ingresso di calcio è fondamentale per attivare la maggior parte dei meccanismi cellulari, ma quando un neurone non c’è l’energia necessaria per estruderlo per ritornare nuovamente alle condizioni basali, le concentrazioni citoplasmatiche di questo ione aumentano e di conseguenza si innescano, in maniera incontrollabile, una serie di meccanismi non desiderati con un ulteriore dispendio energetico.
A complicare le cose c’è la fitta rete di contatti che i neuroni hanno tra di essi e con l’organismo. L’accumulo di calcio in un neurone provoca un’attivazione incontrollabile con il rilascio di neurotrasmettitori eccitatori verso altri neuroni, che a loro volta si attiveranno facendo entrare ioni calcio che non riusciranno ad estrudere. La reazione a catena potrebbe continuare all’infinito in tutto il cervello causando la generazione di scariche elettriche senza controllo che si propagano longitudinalmente rispetto il centro dell’infarto cerebrale (core ischemico) con liberazione di neurotrasmettitori e conseguenze che vedremo nelle prossime puntate.
Il calcio quindi è uno ione fondamentale per la vita perché è il centro di regolazione di funzioni cellulari importanti. Tuttavia proprio per questo motivo è anche uno ione molto pericoloso perché in condizioni patologiche, come l’ictus per l’appunto, può innescare l’autodistruzione cellulare. Un articolo pubblicato su Journal of Neuroscience descrive l’importanza di alcuni meccanismi; per chi è interessato
Durukan and Tatlisumak Pharmacology, Biochemistry and Behavior 87 (2007) 179-197.
Tags:
Biologia molecolare,
Ictus,
Ischemia Cerebrale,
Mente,
Neuroscienze,
Neurotrasmettitori

 Prima di trarre conclusioni affrettate andiamo in laboratorio con la nostra ricostruzione della scena del crimine. Induciamo una ischemia cerebrale a dei ratti ed analizziamo nel tempo cosa fa la microglia nel SNC. Anche se non è facile seguire le cellule microgliali che girano nel cervello quando l’animale è vivo, è possibile ricostruire la scena mettendo insieme una serie di animali analizzati a tempi diversi dopo l’evento ischemico.
Prima di trarre conclusioni affrettate andiamo in laboratorio con la nostra ricostruzione della scena del crimine. Induciamo una ischemia cerebrale a dei ratti ed analizziamo nel tempo cosa fa la microglia nel SNC. Anche se non è facile seguire le cellule microgliali che girano nel cervello quando l’animale è vivo, è possibile ricostruire la scena mettendo insieme una serie di animali analizzati a tempi diversi dopo l’evento ischemico. L’accusa inizia l’arringa con delle frasi taglienti e tendenziose. Secondo la sua ricostruzione le cellule microgliali, avvezze all’eutanasia, si sono dirette verso la zona sofferente dall’ipossia. I dati pubblici ci hanno depistato sull’effettivo orario di arrivo sul luogo del delitto, in realtà, recenti scoperte ci indicano che le cellule microgliali si trovavano già in loco prima del tempo dichiarato. Non è stato possibile vederle poiché sono arrivate con un travestimento non noto fino a poco tempo fa. Poi una volta arrivate sul luogo prefissato hanno iniziato a contornare alcuni neuroni in sofferenza. La microglia, adese ai neuroni ha liberato delle sostanze in uno spazio estremamente piccolo, troppo scarse per essere analizzate e troppo rapide per essere viste. In questo istante forse c’é stato un ‘errore’, ed al posto di sostanze neurotrofiche la microglia ha lasciato delle sostanze tossiche. Magari ha valutato che i neuroni non ce l’avrebbero fatta a passare indenni l’ipossia e li ha avvelenati in maniera irreversibile per eutanasia. Poi mentre i neuroni avvelenati stavano resistendo all’ipossia, il colpo di grazia, la microglia si é allontanata aggravando la situazione per il mancato sostentamento trofico. Ciò che ne é conseguito é la morte dei neuroni in circostanze apparentemente solitarie. Poi sono arrivate le cellule microgliali travestite da spazzine ed hanno pulito il luogo del delitto.
L’accusa inizia l’arringa con delle frasi taglienti e tendenziose. Secondo la sua ricostruzione le cellule microgliali, avvezze all’eutanasia, si sono dirette verso la zona sofferente dall’ipossia. I dati pubblici ci hanno depistato sull’effettivo orario di arrivo sul luogo del delitto, in realtà, recenti scoperte ci indicano che le cellule microgliali si trovavano già in loco prima del tempo dichiarato. Non è stato possibile vederle poiché sono arrivate con un travestimento non noto fino a poco tempo fa. Poi una volta arrivate sul luogo prefissato hanno iniziato a contornare alcuni neuroni in sofferenza. La microglia, adese ai neuroni ha liberato delle sostanze in uno spazio estremamente piccolo, troppo scarse per essere analizzate e troppo rapide per essere viste. In questo istante forse c’é stato un ‘errore’, ed al posto di sostanze neurotrofiche la microglia ha lasciato delle sostanze tossiche. Magari ha valutato che i neuroni non ce l’avrebbero fatta a passare indenni l’ipossia e li ha avvelenati in maniera irreversibile per eutanasia. Poi mentre i neuroni avvelenati stavano resistendo all’ipossia, il colpo di grazia, la microglia si é allontanata aggravando la situazione per il mancato sostentamento trofico. Ciò che ne é conseguito é la morte dei neuroni in circostanze apparentemente solitarie. Poi sono arrivate le cellule microgliali travestite da spazzine ed hanno pulito il luogo del delitto. La difesa risponde punto per punto con calma e freddezza.
La difesa risponde punto per punto con calma e freddezza. Se questo fosse un giallo non potrebbe mancare il classico colpo di scena. Questa volta arriva proprio da Mario Capecchi che scopre, in una sua recente pubblicazione su cell, che l’inattivazione della microglia provoca un fenotipo ossessivo-convulsivo. Quello che sorprende é che l’iniezione nel midollo osseo di cellule microgliali marcate e fluorescenti provoca la comparsa di cellule microgliali nel cervello. Ancora una volta la microglia ha mentito, e a quanto pare ha un passaggio segreto per oltrepassare la BEE, anche se oggi non é stato ancora possibile scoprire come. A quanto pare la microglia ha molti aspetti ancora oscuri, forse anche delle identità e dei passaporti che non conosciamo ancora.
Se questo fosse un giallo non potrebbe mancare il classico colpo di scena. Questa volta arriva proprio da Mario Capecchi che scopre, in una sua recente pubblicazione su cell, che l’inattivazione della microglia provoca un fenotipo ossessivo-convulsivo. Quello che sorprende é che l’iniezione nel midollo osseo di cellule microgliali marcate e fluorescenti provoca la comparsa di cellule microgliali nel cervello. Ancora una volta la microglia ha mentito, e a quanto pare ha un passaggio segreto per oltrepassare la BEE, anche se oggi non é stato ancora possibile scoprire come. A quanto pare la microglia ha molti aspetti ancora oscuri, forse anche delle identità e dei passaporti che non conosciamo ancora. Mettere insieme tutti questi dati sparsi non é semplice. Nella ricerca, infatti, é difficile soprattutto distinguere la verità obiettiva dalle interpretazioni, ed in questo lungo processo sono state fatte solo delle allusioni, niente di più. L’articolo di Capecchi parla di una interferenza sui recettori nocicettivi periferici da parte della microglia. Un topo con difficoltà nella percezione del dolore ha dei comportamenti anomali, ma non c’é niente di significativamente neurologico.
Mettere insieme tutti questi dati sparsi non é semplice. Nella ricerca, infatti, é difficile soprattutto distinguere la verità obiettiva dalle interpretazioni, ed in questo lungo processo sono state fatte solo delle allusioni, niente di più. L’articolo di Capecchi parla di una interferenza sui recettori nocicettivi periferici da parte della microglia. Un topo con difficoltà nella percezione del dolore ha dei comportamenti anomali, ma non c’é niente di significativamente neurologico.
















 Come abbiamo visto nel precedente post, il nostro ispettore cellulare è stato improvvisamente freddato dallo scagionamento del primo imputato eccellente. La teoria iniziale non faceva una grinza e c’erano anche molti indizi pesanti contro l’accusato. Purtroppo con il tempo e con l’uso di sostanze sempre più specifiche per il blocco del fattore transcrizionale la teoria della difesa ha avuto sempre più supporto. HIF-1 non è sicuramente una proteina da mettere tra i cattivi per l’
Come abbiamo visto nel precedente post, il nostro ispettore cellulare è stato improvvisamente freddato dallo scagionamento del primo imputato eccellente. La teoria iniziale non faceva una grinza e c’erano anche molti indizi pesanti contro l’accusato. Purtroppo con il tempo e con l’uso di sostanze sempre più specifiche per il blocco del fattore transcrizionale la teoria della difesa ha avuto sempre più supporto. HIF-1 non è sicuramente una proteina da mettere tra i cattivi per l’ Pensare all’ipossia come innesco di un meccanismo che porterà a morte inevitabile per i
Pensare all’ipossia come innesco di un meccanismo che porterà a morte inevitabile per i  Se fate questa domanda ad un qualsiasi esperto nel settore vi dirà che ci sono migliaia di proteine che fanno ‘ordine’ tra i diversi ioni, e sono divise in famiglie, superfamiglie e classi. Questi meccanismi possono dividersi grossolanamente in pompe e trasportatori, in base al fatto che usano direttamente, o no, l’ATP.
Se fate questa domanda ad un qualsiasi esperto nel settore vi dirà che ci sono migliaia di proteine che fanno ‘ordine’ tra i diversi ioni, e sono divise in famiglie, superfamiglie e classi. Questi meccanismi possono dividersi grossolanamente in pompe e trasportatori, in base al fatto che usano direttamente, o no, l’ATP. A questa domanda c’è una risposta più o meno ovvia. Poco prima dell’ischemia funzionava tutto come al solito, nulla lasciava presagire il disastro, e tutte le proteine risiedevano al loro nomale posto fino a che è mancata l’energia necessaria per il trasporto attivo degli ioni. Quando è iniziata a mancare l’energia l’efficienza del trasporto ionico si è ridotta mentre il disordine ionico dei
A questa domanda c’è una risposta più o meno ovvia. Poco prima dell’ischemia funzionava tutto come al solito, nulla lasciava presagire il disastro, e tutte le proteine risiedevano al loro nomale posto fino a che è mancata l’energia necessaria per il trasporto attivo degli ioni. Quando è iniziata a mancare l’energia l’efficienza del trasporto ionico si è ridotta mentre il disordine ionico dei  A questo punto del racconto io mi recherei sul luogo del delitto alla ricerca di qualche indizio e soprattutto di qualche risposta.
A questo punto del racconto io mi recherei sul luogo del delitto alla ricerca di qualche indizio e soprattutto di qualche risposta. Ritornando in ufficio c’è una cosa che non quadra… questo trasportatore passivo dove ha trovato tutta questa energia per espellere una quantità di
Ritornando in ufficio c’è una cosa che non quadra… questo trasportatore passivo dove ha trovato tutta questa energia per espellere una quantità di  Uhmm… Forse calunnie, leggendo bene qua e là i farmaci utilizzati per inibire NCX non sono molto specifici, agiscono anche su altri canali; magari NCX è stato coinvolto in qualcosa di più grande ed è stato usato come capro espiatorio. Improbabile che una proteina così letale possa essere conservata per milioni di anni durante l’evoluzione se non migliori sensibilmente il fitness dell’organismo.
Uhmm… Forse calunnie, leggendo bene qua e là i farmaci utilizzati per inibire NCX non sono molto specifici, agiscono anche su altri canali; magari NCX è stato coinvolto in qualcosa di più grande ed è stato usato come capro espiatorio. Improbabile che una proteina così letale possa essere conservata per milioni di anni durante l’evoluzione se non migliori sensibilmente il fitness dell’organismo. Le cose, da allora, non sono andate molto avanti, le pubblicazioni si sono rincorse tra di loro in un misto di ripetizioni e staccate con farmaci sempre più specifici e potenti. A questi articoli facevano seguito altri che descrivevano dell’effetto di queste sostanze sulla circolazione, ipertensione, inibizione di canali del
Le cose, da allora, non sono andate molto avanti, le pubblicazioni si sono rincorse tra di loro in un misto di ripetizioni e staccate con farmaci sempre più specifici e potenti. A questi articoli facevano seguito altri che descrivevano dell’effetto di queste sostanze sulla circolazione, ipertensione, inibizione di canali del  Analisi su analisi in diverse salse hanno dimostrato che questa proteina è fondamentale per alcuni meccanismi cardiaci e non solo, ma sicuramente esalta anche il danno ischemico al miocardio. E’ una circostanza difficile da spiegare in termini evoluzionistici e non è possibile capirne a fondo il meccanismo esatto.
Analisi su analisi in diverse salse hanno dimostrato che questa proteina è fondamentale per alcuni meccanismi cardiaci e non solo, ma sicuramente esalta anche il danno ischemico al miocardio. E’ una circostanza difficile da spiegare in termini evoluzionistici e non è possibile capirne a fondo il meccanismo esatto.  Una delle osservazioni più ovvie che mi sono state fatte nel tempo si basa sul fatto che tutto quello che si avvia durante l’
Una delle osservazioni più ovvie che mi sono state fatte nel tempo si basa sul fatto che tutto quello che si avvia durante l’ Se dovessi associare questo fattore trascrizionale ad un personaggio di un giallo, potrebbe essere rappresentato senza alcun dubbio da un antipatico ed ambiguo individuo che attira su di sé tutti gli indizi, in modo tale che rappresenti l’assassino nell’immaginario del lettore per buona parte del racconto. In genere queste persone durante il racconto possono trovarsi alternativamente tra i principali sospetti, tra i fiancheggiatori, tra gli innocenti o tra i più improbabili difensori della verità.
Se dovessi associare questo fattore trascrizionale ad un personaggio di un giallo, potrebbe essere rappresentato senza alcun dubbio da un antipatico ed ambiguo individuo che attira su di sé tutti gli indizi, in modo tale che rappresenti l’assassino nell’immaginario del lettore per buona parte del racconto. In genere queste persone durante il racconto possono trovarsi alternativamente tra i principali sospetti, tra i fiancheggiatori, tra gli innocenti o tra i più improbabili difensori della verità. Bene dopo questa velocissima presentazione di questo angelo o diavolo è ora di chiedersi cosa stava facendo subito dopo l’occlusione dell’arteria cerebrale e proprio in quei
Bene dopo questa velocissima presentazione di questo angelo o diavolo è ora di chiedersi cosa stava facendo subito dopo l’occlusione dell’arteria cerebrale e proprio in quei 

 La parola all’accusa
La parola all’accusa La difesa tira fuori il dogma scientifico
La difesa tira fuori il dogma scientifico Allora, per chi non avesse seguito le puntate precedenti, abbiamo introdotto un giallo misterioso dove delle cellule del cervello umano muoiono improvvisamente in seguito ad
Allora, per chi non avesse seguito le puntate precedenti, abbiamo introdotto un giallo misterioso dove delle cellule del cervello umano muoiono improvvisamente in seguito ad  Se dovessimo ricostruire cosa accade negli ultimi istanti di queste cellule, ci potremmo accorgere che le cellule della penombra moriranno entro qualche ora non riescono a gestire i flussi di
Se dovessimo ricostruire cosa accade negli ultimi istanti di queste cellule, ci potremmo accorgere che le cellule della penombra moriranno entro qualche ora non riescono a gestire i flussi di  Un ispettore che si trova in una scena del crimine molto complessa come quella descritta e che ha sentito la ricostruzione del danno analizzerebbe sicuramente tutta una batteria di proteine e di mRNA per capire costa stavano facendo i
Un ispettore che si trova in una scena del crimine molto complessa come quella descritta e che ha sentito la ricostruzione del danno analizzerebbe sicuramente tutta una batteria di proteine e di mRNA per capire costa stavano facendo i 

 Seguendo la storia sulla falsa riga del “giallo”, la prima domanda è come sono morte le cellule? Hanno eseguito un suicidio di massa (apoptosi) oppure sono morte per trauma (necrosi)?
Seguendo la storia sulla falsa riga del “giallo”, la prima domanda è come sono morte le cellule? Hanno eseguito un suicidio di massa (apoptosi) oppure sono morte per trauma (necrosi)? L’investigazione quindi è tutta in salita, non possiamo trarre molte informazioni dal ritrovamento delle vittime se non che siano state uccise da un evento molto traumatico avvenuto diverse ore dopo il ristabilirsi delle condizioni ottimali di circolazione sanguigna (vedi post precedente).
L’investigazione quindi è tutta in salita, non possiamo trarre molte informazioni dal ritrovamento delle vittime se non che siano state uccise da un evento molto traumatico avvenuto diverse ore dopo il ristabilirsi delle condizioni ottimali di circolazione sanguigna (vedi post precedente).

